A cirkadián vérnyomásritmus a szív- és érrendszeri és a vese egészségében és betegségeiben
May 17, 2022
További információért. kapcsolatba lépnitina.xiang@wecistanche.com
Absztrakt: A vérnyomás (BP) cirkadián ritmust követ, reggel ébredéskor emelkedik, éjszakai alvás közben pedig csökken. Beszámoltak arról, hogy a cirkadián BP-ritmus megzavarása a szív- és érrendszeri és a vese kimenetelének romlásával jár, azonban a mögöttes molekuláris mechanizmusok még mindig nem tisztázottak. Ebben az áttekintésben röviden összefoglaltuk a cirkadián BP szabályozás jelenlegi megértését, és terápiás áttekintést adtunk a cirkadián BP ritmus és a szív- és érrendszeri, valamint a vese egészsége és betegségei közötti kapcsolatról.
Kulcsszavak: cirkadián ritmus; vérnyomás; szív- és érrendszeri; vese-

Kattintson a legjobb cistanche-kiegészítő megismeréséhez
1. A cirkadián vérnyomásritmus bevezetése
A cirkadián ritmus egy 24 órás ciklusú endogén bioritmusra utal, amelyet egy belső és periodikus molekuláris óra hajt, amely a viselkedést és a fiziológiai tevékenységeket a külső környezeti változásokhoz igazítja [1,2]. Emlősökben a hipotalamusz suprachiasmaticus magjában (SCN) található master pacemaker gondosan szabályozza a többi szövet perifériás óráit, hogy biztosítsa az összes meglévő óra szinkronizálását [34]. Amint az 1. ábrán látható, az emlősök molekuláris cirkadián órát egy kölcsönhatásos transzkripciós-transzlációs auto-szabályozó visszacsatolási hurok hajtja a mag óragének egy részével, beleértve a Bmall-t (agyi és izom aril szénhidrogén receptor nukleáris transzlokátor-szerű 1), Clock (circadian lokomotoros kimeneti ciklusok kaput), Per1/2/3 (period1/2/3) és Cry1/2 (crypt-tochrome1/2). A BMAL1 és a CLOCK fehérjék együttesen heterodimert alkotnak, hogy kapcsolódjanak az E-box elemeihez az óravezérelt gének (CCG) promoter régióiban, beleértve számos fontos géntszív- és érrendszeriésveseműködés[5,6]. Amikor a PER és CRY fehérjék felhalmozódása teljesen felesleges a citoplazmában, mindkettő a sejtmagba transzlokálódik, ami leállítja a heterodimer aktivátor transzkripcióját [7]. Ezenkívül a nukleáris receptorok ROR (RAR-kapcsolódó árva receptor) aktiválódik, és a REV-ERB (nukleáris receptor alcsalád 1, D csoport) elnyomja a RORE-t (ROR elem), hogy közvetlenül szabályozza a Bmall és Clock transzkripciót [8]. Ezenkívül egy másik, ebbe a hurokba integrált nukleáris receptor PPARy szintén a BMAL1 célgénje, mivel közvetlenül kötődik a PPRE-hez (PPAR válaszelem) a promoterében [9]. Különösen az összes dinamikus, de koordinált PPAR izoforma napi expressziót mutatott különböző időpontokban az egérszövetekben[10]. Becslések szerint a szívben és a vesében található géntranszkriptumok csaknem 10-15 százaléka cirkadián transzkripciós szabályozás alatt áll [11].

Az újabb bizonyítékok azt mutatják, hogy a legtöbb szív- és érrendszeri és vesefunkciós ingadozást evolúciósan a cirkadián óra szabályozza. A szív- és érrendszeri és a vese egészsége szempontjából kulcsfontosságú BP nyilvánvaló cirkadián ritmust mutat éjszakai zuhanásokkal és reggeli hullámzásokkal mind az emberek, mind a rágcsálók esetében [12]. A vérnyomás cirkadián mintázatát számos tényező befolyásolhatja.
Például az éjszaka a tobozmirigyből kiválasztódó melatonin jelentősen csökkentheti az éjszakai vérnyomást és javíthatja az alvást az esszenciális hipertóniában szenvedő betegeknél [13]. A pitvari natriuretikus peptid (ANP) ritmikussága ellentétesnek tűnt a vérnyomás ritmusával, amelyről bebizonyosodott, hogy fontos szabályozó tényező a 24 órás vérnyomásmintázatban, és hatással van a szív- és érrendszerre [14]. A plazma renin-aktivitás (PRA), az angiotenzin-konvertáló enzim (ACE) aktivitása, valamint az Angl-, az aldoszteron- és a pajzsmirigyhormon-koncentráció cirkadián ritmusa szintén hozzájárul a 24 órás vérnyomás-ritmus fenntartásához [15-19]. A hormonokon kívül a vérerek összetevői, például a simaizomsejtek és az endothelsejtek, valamint számos vazoaktív anyag megváltoztathatják a vérnyomás napi változásait. Jellemzően az endothel sejtekből kiválasztott nitrogén-monoxid (NO) modulálja a vaszkuláris tónust és ezáltal a vérnyomást. A termelés NINCS emelkedése reggel, ezt követi a reggeli vérnyomás-emelkedés. Mégis vita tárgyát képezi, hogy az NO napi változása közvetlenül összefügg-e a vérnyomás ritmusával. Az NO-termelés napi oszcillációjának megzavarása szorosan összefügg a vérnyomás változásaival.szív-és érrendszeri betegségek[20]. Ezenkívül az endoteliális NO-szintáz (eNOS) egyike a három NO-szintáz enzimnek, amelyek NO-t termelnek az erekben, és szabályozzák az érrendszeri működést. Állatkísérletekben a foszforilált eNOS (p-eNOS) fiatal egerek ereiben cirkadián ritmust mutatott. A mag óragének az eNOS csatolását is szabályozhatják, és hozzájárulhatnak az endothel funkció és a vérnyomás ritmikusságának fenntartásához [21]. Hasonlóképpen, bár a 3.5-napi ritmusról és az 8-óránkénti változásról számoltak be az emberi keringésben [22], az endotelin 1 (ET-1) plazmában történő szekréciójáról és a vizelettel történő kiválasztódásáról azt is egyértelműen megerősítették, hogy cirkadián ritmikus, és szorosan kapcsolódik a vérnyomás homeosztázisához [23-25]. Az ET-1 receptor antagonisták hatékonynak bizonyultak az esszenciális hipertónia kezelésében, azonban jelentős folyadékretenció
és ödémás mellékhatásokról is beszámoltak [26]. A fentieken kívül számos egyéb endogén tényező is hozzájárul a 24 órás vérnyomás-oszcillációhoz humorális, endokrin, neurális vagy egyéb koordinált szabályozási jeleken keresztül. Ezenkívül egyes betegségek megváltoztathatják a 24 órás vérnyomás ritmusát. Például az obstruktív alvási apnoéban (OSA) szenvedő betegeknél nagyobb valószínűséggel fordul elő nem dipper vérnyomás, ami növeli a kardiovaszkuláris események előfordulását [27].
Exogén szempontból a növekvő tanulmányok kimutatták, hogy az alvási minták jelentős hatással lehetnek a BPnap-éjszaka profilra |28]. Például azok az emberek, akiknél alvászavar vagy cirkadián eltérés a műszakban végzett munka és a szociális jet lag miatt gyakran szenvednek magas vérnyomásban [29], a vérnyomás fáziskésésétől [30], a melatonin szekréciójának rendellenes ritmusától [31] vagy megnövekedett magas érzékenységű C-reaktív fehérjétől. [32]. Továbbá, bár saját tanulmányaink azt mutatták, hogy a vérnyomás napi ritmusát az óra közvetlenebb módon szabályozza, mint a viselkedést, legalábbis alapfeltételek mellett[33,34]. A legutóbbi tanulmány azonban azt találta, hogy a táplálékfelvétel időzítése magával ragadhatja a napi vérnyomásritmust, függetlenül a Bmall-tól és a világos-sötét ciklusoktól [35]. Ezenkívül a vérnyomás ritmusát befolyásolhatja a hőmérséklet, a zaj és sok más környezeti tényező [36-38].

2. Kanonikus óragének és BP szabályozás
Mint fentebb említettük, a vérnyomás cirkadián ritmusát egy bonyolult molekuláris órahálózat vezérli. A rágcsálóktól származó egyre több bizonyíték azt találta, hogy a vérnyomás cirkadián ritmusa egyértelműen megváltoztatható a magóragének genetikai manipulációjával (1. táblázat).
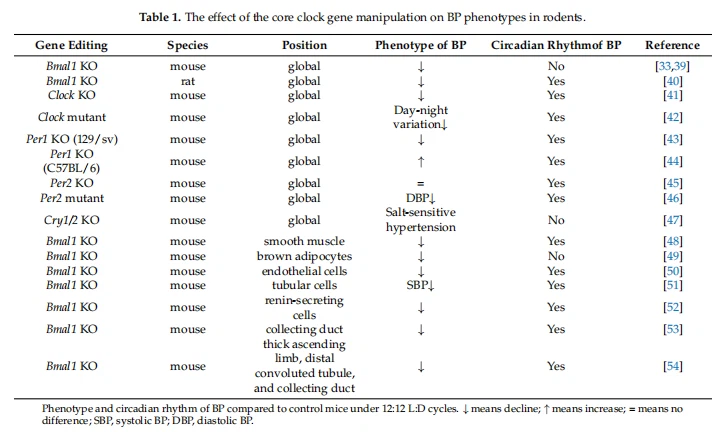
2.1.Bmal1
Számos tanulmány kimutatta, hogy a Bmall-deléciós egerek megváltozott vérnyomást és (vagy) károsodott szív- és érrendszeri és vesefunkciókat mutattak [21,39,48,51,52,54-56]. A vérnyomás napi ingadozásának csökkenését hipotenziós fenotípus kíséretében mind prenatális, mind posztnatális Bmall globális knockout egerekben megerősítették [33,39]. Éppen ellenkezőleg, bár a Bmall knock-out patkányok az artériás nyomás általános csökkenését eredményezték, a vérnyomás ritmusa érintetlen maradt [40]. A fajok közötti különbségek magyarázata lehet. Specifikus kimerülés
A Bmall egerekben a simaizomsejtekből (SM{0}}Cre), de nem a szívizomsejtekből, szignifikánsan elnyomta a BP oszcilláció amplitúdóját és eltolta az akrofázisát [48]. Mechanikailag a BMAL1 szabályozza a Rho-kinase 2 (ROCK2) aktivitásának napszaki változásait azáltal, hogy közvetlenül kötődik a promóteréhez, és a Bmal1 deléció nagymértékben csökkenti a ROCK2 aktivációt, a miozin foszforilációját, majd az érszűkületre adott napi változást. 48]. Chang és munkatársai kimutatták, hogy a Bmall elvesztése a perivaszkuláris zsírszövetben csökkentette a vérnyomást egerekben a nyugalmi fázisban [49]. Sőt, az endothel sejtekben Bmall-depresszióban szenvedő egerek (TEK-Cre) átlagos artériás nyomása is szignifikánsan alacsonyabb volt, azonban a molekuláris mechanizmus még mindig nem tisztázott [50]. Firsov és munkatársai a vese Bmal1-ét illetően a cirkadián BP szabályozásban megerősítették a szisztolés vérnyomás enyhe csökkenését, de nem a diasztolés vérnyomást, mivel az egereknél az intakt cirkadián ritmus hiányzik a Bmall teljes nefronból (Pax8-Cre)[51]. Míg egy másik egérmodellben, ahol a Bmall kimerült a renin-kiválasztó sejtekben (Ren1-Cre), a vérnyomás amplitúdójának csökkenését is megfigyelték, ami sok más veseelváltozással jár, beleértve a cirkadián változásait. a vizelettel történő nátriumkiválasztás ritmusa és a megnövekedett glomeruláris filtrációs sebesség, valamint a plazma aldoszteronszintjének csökkenése [52]. Ezenkívül Pollock és munkatársai kimutatták, hogy a Bmal1 elvesztése a gyűjtőcsatornában (AQP2-Cre) jelentősen csökkenti a vérnyomást férfiakban , de nem nőstény egereket a kontroll egerekhez képest [53]. Gumz és munkatársai kimutatták, hogy az egerek, amelyekből hiányzik a Bmal1 a vastag felszálló végtagban, a disztális, csavarodott tubulusban, és a gyűjtőcsatornasejtek (Ksp-Cre) nyilvánvalóan alacsonyabb bazális szisztolés vérnyomást mutattak a kontrollegerekhez képest [54]. Összességében a Bmal1, különösen a szív- és érrendszeri és a veserendszerben történő expressziója kritikus szerepet játszik a BP homeosztázis és ritmus fenntartásában.
2.2.Per
Legutóbb rágcsálókon végzett tanulmányok sorozata elegánsan tisztázta a Perl fontos szerepét a vérnyomás szabályozásában és az elektrolitkezelésben. A radiotelemetriás felvételek és az Elisa mérések azt mutatták, hogy a Perl-t nem tartalmazó egerek vérnyomása szignifikánsan csökkent, és a vese ET{0}}szintje emelkedett a hím 129/SV egerekben [43]. Azonban a C57BL/6 háttérrel rendelkező nőstény Per1 knockout egerekben nem figyeltek meg megváltozott ET-1szinteket [57]. A magas sótartalmú étrend plusz mineralokortikoid dezoxikortikoszteron-pivalát (HS/DOCP) injekció jelentősen nem merülő magas vérnyomást és vese-nátrium kezelési rendellenességet eredményezett (<10% difference="" between="" active="" and="" inactive="" phase)="" in="" male="" perl="" knockout="" mice[4,58].="" interestingly,="" the="" female="" per1="" knockout="" mice="" appeared="" to="" be="" protective="" against="" non-dipping="" hypertension="" in="" response="" to="" hs/docp="" treatment="" in="" a="" sex-dependent="" manner="" to="" some="" extent="" [57].="" moreover,="" in="" contrast="" to="" the="" c57bl/6="" background,="" male="" per1="" ko="" mice="" on="" a="" 129/sv="" background="" in="" combination="" with="" hs/docp="" challenge="" are="" extraordinarily="" protective="" against="" hypertension="" [59],="" implying="" that="" sex="" hormones="" might="" be="" fundamental="" to="" perl="" medicated="" circadian="" bp="" control.="" the="" complexity="" of="" per1="" in="" circadian="" bp="" control="" may="" need="" further="" investigation.="" in="" accordance="" with="" the="" altered="" bp="" pattern,="" the="" clock="" gene="" per1="" might="" regulate="" the="" transcription="" of="" the="" epithelial="" sodium="" channel(enac),="" sodium-glucose="" linked="" transporter-1(sglt-1),sodium-hydrogen="" exchanger-3(nhe3),="" endothelin-1(et-1),="" which="" are="" responsible="" for="" sodium="" transport="" in="" the="" kidney="" [43,60,61].="" as="" for="" another="" isoform="" of="" gene="" per,="" per2="" mutant="" mice="" showed="" a="" mild="" cardiovascular="" phenotype="" with="" an="" elevated="" 24="" h="" heart="" rate="" as="" well="" as="" decreased="" 24="" h="" diastolic="" bp="" during="" the="" active="" phase="" [46].="" however,="" the="" systolic="" bp="" and="" mean="" arterial="" bp="" displayed="" no="" significant="" difference="" between="" the="" mutant="" and="" control="" mice="" [46].="" in="" addition,="" per2="" mutant="" mice="" resulted="" in="" mild="" attenuation="" of="" 24="" h="" bp="" rhythm,="" heart="" rate,="" and="" locomotor="" activity="" with="" much="" shorter="" circadian="" periods="" than="" wild-type="" mice="" under="" constant-dark="" conditions="" [46].="" collectively,="" the="" clock="" component="" per="" acts="" as="" a="" crucial="" mediator="" in="" the="" circadian="" system="" to="" be="" involved="" in="" bp="">
2.3. Clock and Cry
Beszámoltak arról, hogy a Clock mutáns egerek a Jcl/ICR háttéren csillapított napi vérnyomást és pulzusszámot mutattak [42]. Míg a Clock knockout egerekben az artériás vérnyomás normálisan ritmikus volt, és szignifikánsan alacsonyabb volt, körülbelül 10 Hgmm-es csökkenést a kontrollegerekhez képest, enyhe diabetes insipidus kíséretében és károsodott nátriumkiválasztási ritmusban [41]. Egy másik Cry órajel-komponenssel kapcsolatban Doi et al. leleplezték, hogy a Cryl és a Cry2 egyidejű hiánya egerekben sóérzékeny hipertóniához vezet, ami a mineralokortikoid aldoszteron rendellenesen krónikus túltermelése miatt következik be a rendellenes mellékvese által [47]. A DNS microarray azt is feltárta, hogy egy specifikus Hsd3b6 enzim túlzott expressziója hozzájárulhat a magas mineralokortikoid aldoszteron szintézishez Cry-null egerekben, ami arra utal, hogy az órafüggő nátriumkiválasztás fontos szerepet játszhat a BP cirkadián homeosztázisában [47]. A megváltozott nátriumkiválasztás és a vérnyomás szabályozása közötti ok-okozati összefüggést azonban tovább kell vizsgálni.
Érdemes megemlíteni, hogy a központi óra génmanipulációs modelljein kívül a transzgenikus hipertóniás TGR(mREN2)27 patkányt, amely egy további egér renin gént tartalmaz, és inverz cirkadián BP profilt mutat, szintén általánosan alkalmazták cirkadián BP ritmus vizsgálatokhoz. [62-64].

3. A cirkadián BP ritmus és a szív- és érrendszeri betegségek megzavarása
A vérnyomásritmus az egyik leggyakoribb cirkadián ritmus a szív- és érrendszerben [65]. A vérnyomás ritmusának megzavarását számos nemkívánatos kardiovaszkuláris esemény fő tényezőjének tekintik. Azt találták, hogy az éjszakai vérnyomás csökkenésének minden 5 százalékos csökkenése körülbelül 20 százalékkal növeli a szív- és érrendszeri halálozás kockázatát [66].
A szívinfarktus (Ml) egy akut szívbetegség, amelyet aritmia, sokk vagy szívelégtelenség bonyolíthat, és életveszélyes. A vérnyomás és a szívinfarktus ritmusa között elválaszthatatlan kapcsolat van. A rendellenes cirkadián vérnyomásmintázatok vagy a krónikus magas vérnyomás a szív hemodinamikájának megváltozásához vezethet, és növelheti az MI előfordulását [67]. Számos klinikai tanulmány igazolta, hogy az Ml előfordulási gyakorisága ritmikus, és általában reggel 6:00 és délután 12:00 között szignifikánsan megnövekedett előfordulási arányt figyeltek meg, ami valahogy összhangban van a reggeli vérnyomás-emelkedéssel. Ami a szisztolés vérnyomást illeti, alacsonyabb (<100 mm="" hg)="" in="" the="" post-ml="" period="" increases="" the="" risk="" of="" cardiovascular="" events,="" while="" patients="" with="" elevated="" systolic="" bp="" (="">140 Hgmm) nagyobb a stroke és a kombinált kardiovaszkuláris események kockázata [68]. A nyugalmi szisztolés vérnyomáshoz képest az edzés utáni szisztolés vérnyomás magasabb prediktív értéket adhat az akut MI-re [69]. Ami a diasztolés vérnyomást illeti, az alacsonyabb diasztolés vérnyomású akut szívinfarktusban (AMI) szenvedő betegek<70 mmhg)="" have="" increased="" postoperative="" risks,="" including="" all-cause="" death,="" cardiovascular="" death,="" and="" cardiovascular="" hospitalization.="" moreover,="" wide="" pulse="" pressure="" was="" also="" considered="" a="" predictor="" of="" mi="" [70].="" furthermore,="" several="" core="" clock="" genes="" are="" considered="" important="" components="" in="" regulating="" the="" rhythmic="" pathogenesis="" of="" ml.="" there="" is="" an="" association="" between="" ml="" and="" clock="" and="" arnel(also="" known="" as="" b="" mall)gene="" polymorphisms[71],="" and="" the="" genetic="" variants="" of="" arntl,="" clock,="" and="" per2="" genes="" are="" proved="" to="" be="" related="" to="" circadian="" phenotype(i.e.,="" chronotype="" or="" daytime="" sleepiness)="" in="" patients="" with="">
Megőrzött ejekciós frakcióval járó szívelégtelenség esetén a szisztolés és diasztolés vérnyomás megnövekedett változékonysága a nemkívánatos események számának növekedésével függ össze [73]. Ezzel párhuzamosan a kóros szisztolés vérnyomás és a diasztolés vérnyomás eltéréseket okozhat a szívindikátorokban. A szisztolés vérnyomás növekedésével a bal kamra falvastagsága és a bal kamrai tömegindex is növekszik a magasabb diasztolés vérnyomás mellett; míg a bal kamrai diasztolés funkció funkcionális indexe fordítottan arányos a diasztolés vérnyomás emelkedésével, de irreleváns a szisztolés vérnyomással [74]. Összességében U-alakú kapcsolat van a szisztolés vérnyomás és a szívelégtelenség között, vagyis az alacsonyabb vagy magasabb szisztolés vérnyomás a halálozás és a szívelégtelenség kórházi kezelésének nagyobb kockázatához vezet [75]. Ugyanez a jelenség a diasztolés vérnyomásban [76]. Ezért az MI és a kapcsolódó kardiovaszkuláris események diagnosztizálása során átfogóan figyelembe kell venni a vérnyomás fenotípusát és ritmusát.
Tekintettel az akut kardiovaszkuláris események és a vérnyomás ritmusai közötti szignifikáns korrelációra, szükséges a terápiás stratégiák fejlesztése a cirkadián ritmusváltozás jellemzőinek megfelelően. A gyógyszerbeadási idő optimalizálása mellett arról számoltak be, hogy a kardiovaszkuláris műtétek időpontja befolyásolhatja a szövetek helyreállítását és a szív- és érrendszeri betegségek kimenetelét is. Például, bár a legutóbbi tanulmányok azt mutatták, hogy az aortabillentyű-pótló műtét napszaki változása nem volt jelentős hatással a klinikai kimenetelre, és nem volt klinikailag releváns bioritmusa a szívizom ischaemia-reperfúziós toleranciája szempontjából [7-79]. Montaigne et al. arról számoltak be, hogy a jelentős nemkívánatos kardiális események előfordulási gyakorisága a délutáni sebészeti csoportban szignifikánsan alacsonyabb volt, mint a reggeli csoportban [80]. Még érdekesebb, hogy a nem szívműtéten átesett betegeknél Lavallaz et al. azt találta, hogy az AMI incidenciája az utánkövetés során inkább a délutáni műtéteknél nő [81]. Mindazonáltal a cirkadián óra és a szív- és érrendszeri betegségek közötti kapcsolat jobb megértése segíthet célzottabb és személyre szabottabb kezelési stratégiák kidolgozásában a betegek számára.
4. A cirkadián vérnyomásritmus megzavarása és vesekárosodás
Krónikus vesebetegségrégóta szorosan összefügg az alvászavarral és a magas vérnyomással, és így fokozatosan világszerte egészségügyi problémává vált, amely nagy gazdasági terhet jelent [82,83]. Embereknél a felgyülemlett klinikai bizonyítékok azt mutatták, hogy a 24 órás vérnyomásfelvételek tompított vérnyomásváltozása fokozott kockázattal jár. a végszervkárosodás és a vesefunkció progresszív elvesztése [84 855]. Előreláthatólag a cirkadián vérnyomás változás konzisztenciája tönkrement a krónikus vesebetegség stádiumában 3-5[8]. Ezenkívül a krónikus vesebetegségben szenvedő betegeknél a cirkadián vérnyomásprofil szorosan összefügg a fizikai aktivitás szintjével és a célszerv-károsodás súlyosságával [87]. Ezenkívül a klinikai vizsgálatok kimutatták, hogy a cirkadián vérnyomásprofil összefüggésben áll a krónikus vesebetegségben szenvedő idős veteránok mortalitásával [88]. Eközben a vérnyomás éjszakai csökkenése csaknem csökken glomerulopathiában szenvedő betegeknél, ami a nátrium és a fehérje vizelettel történő kiválasztódásának fokozódását eredményezi az inaktív fázisban [89].
A mai napig nem igazolódott egyértelmű mechanizmus a krónikus vesebetegség és a cirkadián BP ritmus megzavarása között. Rágcsálómodelleken végzett vizsgálatok azt találták, hogy egerekben vagy Sprague-Dawley patkányokban krónikus vesebetegséget kiváltó adeninnel végzett 2-4 hetes kezelés után az állatok szignifikánsan megnövekedett artériás vérnyomást és megzavart nappali-éjszakai eltérést mutatnak [90]. Ezenkívül az adenin által kiváltott krónikus vesebetegségben szenvedő PER2:LUC egerek SCN-je tompított amplitúdó ritmust mutatott a központi cirkadián órájukban, biolumineszcenciával mérve. Eközben a krónikus vesebetegségben szenvedő egerekből származó veseexplantátumok megváltozott PER2:LUC ritmusokat fejeztek ki szignifikánsan hosszabb ideig a kontrollegerekhez képest [91]. Másrészt az adenin-kezelés hatására a Clock mutáns egerek szignifikánsan magasabb vérnyomást és rosszabb veseműködést mutattak, mint a kontrollegerek, ami arra utal, hogy a cirkadián BP-zavar fokozza a krónikus vesebetegségre való hajlamot [91]. Azonban a közelmúltban végzett saját tanulmányunk azt találta, hogy a születés utáni Bmall-deléció egerekben megvédte a vesefibrózist a Gli2 transzkripció elnyomásával, ami a Bmall magóra gén kiemelkedő szerepét biztosítja a tubulointerstitialis fibrózisban [92]. Mindazonáltal több erőfeszítést kell tenni egy másik nézőpontból a cirkadián vérnyomászavar és a krónikus vesebetegségek közötti kapcsolat további tisztázása érdekében.

5. A magas vérnyomás elleni gyógyszerek kronoterápiája
A megváltozott nappali-éjszakai oszcilláció a vérnyomásban a szív- és érrendszeri betegségek magas morbiditásával és mortalitásával, valamint a vesekárosodás fokozott progressziójával jár együtt. Megjegyzendő, hogy a nem merülő magas vérnyomás gyakran megfigyelhető a krónikus vesebetegség klinikai kimenetelében, és a kardiovaszkuláris események fokozott kockázatával jár [93]. Míg a vérnyomás túlzott cirkadián ingadozása a nephropathia fokozott kockázatával is összefüggésbe hozható [94,95] Így a vérnyomáscsökkentő gyógyszerek alkalmazása, beleértve az angiotenzin-konvertáló enzim gátlókat (ACEI), az angiotenzin II receptor blokkolókat (ARB) és mások számos szív- és érrendszeri és vesebetegség megelőzésében és kezelésében alapvetőek. Ezen magas vérnyomás elleni gyógyszerek ésszerű és hatékony beadási idejét számos klinikai vizsgálatban és állatkísérletben is feltárták, és beszámoltak róla.
5.1.ACEI
Klinikai vizsgálatok kimutatták, hogy a hosszú hatástartamú lipofil ACEI trandolapril lefekvés előtti adagolása biztonságosabb és hatékonyabb módszer a reggeli vérnyomás szabályozására hipertóniás betegeknél, mint a reggeli adagolású csoportban [96]. A kaptopril és a hidroklorotiazid kombinációs gyógyszere enyhén hatékonyabb volt az éjszakai vérnyomás csökkentésében 13, közepesen súlyos magas vérnyomásban szenvedő férfibetegnél 3 héten keresztül[97]. Ezenkívül a lefekvés előtti spirapril a reggelinél hatékonyabban csökkentette az alvási vérnyomást, ami összefüggésbe hozható az éjszakai RAAS aktivációval [98]. Ezen túlmenően, az esti enalapril-kezelés tovább csökkenti az éjszakai vérnyomást, majd a napközbeni lassú növekedést egy randomizált keresztezett elrendezésben [99]. Továbbá lizinopril beadása 10.{10}} órakor. sokkal hasznosabbnak bizonyult [100]. A quinapril esetében az esti adagolás hasonlóan előnyösebb vérnyomáscsökkentő hatást eredményezett, míg a reggeli adagolás kisebb csökkenést jelentett az éjszakai vérnyomásban [101]. Vannak azonban példák az ellenkezőjére is, egy 10 hipertóniás alany bevonásával végzett egy-vak keresztezett vizsgálatban, amelyről beszámoltak arról, hogy a benazepril reggeli adagolása tartósabb vérnyomáscsökkentő hatást fejt ki, mint az esti adagolás [102]. Sőt, bár a hemodinamika jobbnak tűnt a ramipril gyógyszer esti bevétele után, a ramipril vérnyomáscsökkentő hatása április közepén megközelítőleg hasonlónak tűnt a reggeli és az esti adagolás között egy keresztezett vizsgálatban, amelyben magas vérnyomásban szenvedő betegek vettek részt [103,104].
5.2.ARB
Az ARB-k egyre népszerűbbek a magas vérnyomás kezelésében, rendkívül hatékonyak és jól tolerálhatók. A valzartán lefekvés előtti beadása, szemben az ébredéskor, rendkívül szignifikáns, átlagosan 6%-os növekedést eredményezett a nappali-éjszakai vérnyomás-különbségben, ami a nem érzékeny betegek számának 73%-os relatív csökkenését jelentette. dipping hypertonia [105,106]. Továbbá azt találták, hogy az amlodipin és valzartán kombinációs terápiát lehetőleg lefekvés előtt kell beadni a kontrollált betegek többségének, akiknél további kardiovaszkuláris események előfordulása csökkenhet [107]. Azonban azoknál az alanyoknál, akiknél a megfelelő vérnyomáscsökkentő hatás elérése érdekében kombinált gyógyszeres kezelésre volt szükség, az amlodipin és a valzartán együttes alkalmazása hatékonyan csökkentette a vérnyomást a teljes 24 órában, függetlenül az adagolási időtől, összehasonlítva bármely más értékelt terápiával [107]. A vizsgálatok azt is kimutatták, hogy a lefekvéskor adott telmizartán javította az alvásidőhöz viszonyított vérnyomáscsökkenést és az éjszakai vérnyomás szabályozását az ébredés utáni adagoláshoz képest [108]. Az olmezartánról, egy másik 1-es típusú angiotenzin ⅡI receptor blokkolóról kimutatták, hogy megtartja az éjszakai vérnyomásesést, valószínűleg azáltal, hogy fokozza a nappali nátriumkiválasztást, hogy a cirkadián vérnyomásritmus normalizálása révén enyhítse a szív- és veseterhelést [109-111]. Bár a bizonyítékok azt mutatják, hogy az olmezartán lefekvés előtti beadása szignifikánsan hatékonyabban csökkentette az éjszakai vérnyomást, mint a reggeli adagolás [112], néhány vizsgálatban ellentmondásos megfigyelésekről is beszámoltak [113].
5.3. Egyéb magas vérnyomás elleni gyógyszerek
Számos prospektív vizsgálatról számoltak be, amelyek a szív- és érrendszeri betegségek másodlagos megelőzésén túlmenően tisztázták az alacsony dózisú aszpirin védőhatását olyan magas vérnyomásban szenvedő betegeknél, akiket csak lefekvés előtt adnak be [114-118]. Hasonlóképpen összefoglaltuk az alacsony dózisú aszpirinnel kezelt hipertóniás egerekre kifejtett párhuzamos időfüggő vérnyomáscsökkentő hatást [119], amely jótékony megközelítést jelenthet a hipertóniás alanyok napi vérnyomás-szabályozásának megoldásában. Ezenkívül a nifedipint vérnyomáscsökkentő szerként is jelölik. A nifedipin-kezelés utáni vérnyomáscsökkenés szignifikánsan nagyobb volt lefekvés előtti adagolás esetén, mint a reggeli lenyelés, valamint hatékonyan csökkentette az ödéma előfordulását és a mellékhatások összes számát, összehasonlítva a nifedipin ébredéskor történő bevételével [120-122].
Összességében, bár egyre több bizonyíték bizonyítja, hogy a jelenlegi magas vérnyomás elleni gyógyszerek lefekvés előtti adagolása hatékonyabb lenne a vérnyomás csökkentésében, azonban számos következetlenség is mutatkozik. Valójában a legutóbbi Hygia Chronother-apy Trialban, amely az elalvás és az ébredés utáni vérnyomáscsökkentő kezelés hatásait vizsgálta a szív- és érrendszeri kockázatra egy nagy, 19 804 résztvevő betegből álló csoportban, bár az au-thorok azt állították, hogy a rutinszerű lefekvés előtti fogyasztás több Egynél több vérnyomáscsökkentő gyógyszer a vérnyomás javulását és a nemkívánatos kardiovaszkuláris események előfordulásának csökkenését eredményezheti [123], ebben a vizsgálatban csak egy populációból vettek részt betegek, a vérnyomás csökkenése viszonylag csekély volt, és úgy tűnt, hogy nem végeztek megfelelően randomizált, kontrollált vizsgálatot ez a nagy próba [124]. Ezenkívül egy magas vérnyomással összefüggő krónikus vesebetegségben szenvedő betegekkel végzett kísérletben Rahman et al. szintén nem figyeltek meg különbséget a lefekvés előtti és a reggeli vérnyomáscsökkentő kezelés között a vérnyomás kontrollon [125]. Ezek az ellentmondások tükrözhetik a kohorsz- vagy gyógyszerkiválasztás különbségeit, vagy a vérnyomás-monitoring módszertanának eltéréseit. Azonban előfordulhat, hogy fel kell hívni a figyelmet az egyetlen optimális időpont ajánlásának korlátaira egy teljes populáció számára, anélkül, hogy aggódnának a kronodiagnózis és a vérnyomáscsökkentő gyógyszereknek a vérnyomás cirkadián amplitúdójára és fázisára gyakorolt hatásai miatt. Néhány, de nem minden vérnyomáscsökkentő gyógyszer befolyásolja a vérnyomás cirkadián amplitúdóját [126]. Mindazonáltal további alapos feltárásra van szükség a vérnyomáscsökkentő gyógyszerek kronoterápiájához. Dokumentálták a személyre szabott kronoterápia érdemeit, amelyek a kronodiagnózisért felelősek [127].
6. Következtetések és perspektívák
Egyre több bizonyíték utal arra, hogy a vérnyomás cirkadián ritmusának fenntartása erősen összefügg a szív- és érrendszeri és a vese homeosztázisával, számos magas vérnyomás elleni gyógyszer egyértelműen cirkadián időfüggő hatékonyságot mutatott, és a magas vérnyomás, valamint a kapcsolódó szív- és érrendszeri és vesebetegségek kezelésének kronoterápiás értékelése szükséges. számos tanulmánynál figyelembe vették. Az ezen a területen végzett további kutatásoknak azonban még hangsúlyt kell helyezniük az időfüggő adagolás pontos farmakodinamikájára és farmakokinetikájára, olyan új vegyületek alkalmazásával, amelyek modulálják a cirkadián időzítési rendszert, hogy kiválóan megelőzzék a magas vérnyomás, valamint a kapcsolódó kardiovaszkuláris és krónikus vesebetegségek kialakulását és progresszióját. amely értékes és költség-haszon megközelítést biztosít a vérnyomás szabályozásához és a kronoterápia lehetséges érdemeihez, valamint hozzáadott szisztematikus védelmet.
Ezenkívül a cirkadián BP szabályozás és a szív- és érrendszeri, valamint a vesefunkciók közötti molekuláris kapcsolat még kevésbé ismert. Az RNS-seq elemzés kimutatta, hogy a szív és a vese az első öt jelölt közül kettő, valamint amáj, tüdő és barna zsír a nyilvánvaló cirkadián szabályozást követően. A szívben és vesében található sejtösszetevők és molekuláris hálózat összetettsége azonban nagyrészt a mechanizmus feltárását teszi lehetővé. A szívben és vesében a cirkadián gének szövet- vagy sejtspecifikus kimerülésének további vizsgálata jobb megértést biztosíthat a vérnyomás ritmusa, valamint a szív- és érrendszeri, valamint a vesefunkció közötti kapcsolatról, és utat nyithat a szív- és érrendszeri és vesebetegségek kialakulásának megelőzésére.





