A komplementaktivitást C3 glomerulopathiában az IgG-faktor H fúziós fehérjék szabályozzák Properdin célzódoménekkel és anélkül
Mar 16, 2022
Kapcsolatba lépni:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Alyssa C. Gilmore, Yuchun Zhang, H. Terence Cook', Deborah P. Lavin, Suresh Katti, YiWang2, Krista K. Johnson, SungKwon Kim² és Matthew C. Pickering
„Gyulladásos Betegségek Központja, Imperial College London, Egyesült Királyság; and²Alexion Pharmaceuticals, New Haven, Connecticut, USA
C3 glomerulopathiaA komplement C3 felhalmozódása jellemzi a glomerulusokban. Az okok közé tartoznak, de nem kizárólagosan, a H faktor rendellenességei, amely a komplement alternatív útvonalának fő negatív szabályozója. H-faktor-hiányos (Cfh-/-) egerekben C3 fejlődik kiglomerulopathiaa plazma C3-szintjének csökkenésével együtt. Ezzel a modellel felmértük a H faktor alternatív útvonal szabályozó doménjét (FH1-5) tartalmazó két fúziós fehérje hatékonyságát.
vagy egy nem célzó egér immunglobulinhoz (IgG-FH1-5) vagy egy egér-propindin elleni antitesthez (Anti-P-FH1-5) kapcsolódik. Mindkét fehérje egyenértékű mértékben növelte a plazma C3-at és csökkentette a glomeruláris C3-lerakódást, ami arra utal, hogy az FH1-5-hoz nem volt szükség a megfelelő célzásra ahhoz, hogy megváltoztassa a C3-aktivációt sem a plazmában, sem a glomerulusokban. Az IgG-FH1-5 beadását követően a plazma C3-szintje időlegesen korrelált a B-faktor szintjének változásaival, míg a plazma C5-szintje a plazma megfelelődinszintjének változásaival. Nevezetesen a plazma növekedése
A C5 és a propertydin szintje hosszabb ideig fennmaradt, mint a C3 és a B faktor növekedése. Cfh-/- egerekben az IgG-FH1-5 csökkentette a vesekárosodást a felgyorsult szérum nephrotoxikus nephritis során. Így adataink azt mutatják, hogy az IgG-FH1-5 helyreállította a keringési alternatív útvonal aktivitását és csökkentette a glomeruláris C3 lerakódást Cfh-/- egerekben, és hogy a plazma megfelelődin szintje a C5 konvertáz aktivitás érzékeny markere H faktor hiány esetén. Az immunglobulinnal konjugált FH1-5 fehérje viszonylag hosszú plazma felezési ideje révén a C3 potenciális terápiája lehet.glomerulopathia.

A Cistanche segíthet a glomerulopathiában
Fordítási nyilatkozat
C3 glomerulopathia(C3G) egy vesebetegség, amelyet a C3 komplement rendellenes felhalmozódása jellemez a glomerulusokban és a glomeruláris károsodás. Ennek oka a komplement alternatív útvonalának ellenőrizetlen aktiválása. Fúziós fehérjék, amelyek az alternatív útvonal-szabályozó, a H-faktor (FH) funkcionális doménjeiből állnak, antitesthez kapcsolva, helyreállították a komplement szabályozást, és csökkentették a glomeruláris C3-at egy C3G egérmodellben. A nem célzó antitest-konjugáció viszonylag hosszú fúziós fehérje plazma felezési időt eredményezett, és ez, vagy hasonló konjugációs módszerek felhasználhatók az FH funkció fokozására a C3G terápiájában.
C3 glomerulopathia(C3G) egy komplement-mediált vesebetegség, amelyet a glomerulusokban a C3 rendellenes mennyisége jellemez.1 Veseelégtelenségig fejlődhet, és nincs végleges kezelés.2 A C3G a komplement alternatív útvonalának (AP) abnormális aktiválódásával jár. Az AP aktiválása a C3bBb (C3 konvertáz) termelődését eredményezi, egy enzim, amely a C3-at hasítja. Egy másik C3b molekula hozzáadása után a keletkező C3bBbC3b komplex (C5 konvertáz) képes hasítani a C5 komplementet. Irányíthatatlan
Az AP aktiválódása a C3G-ben összefüggésbe hozható a keringő C3, C5, B faktor (FB) és propertydin csökkenésével. A kontrollálatlan AP aktiváció okai közé tartozik a komplement szabályozók funkcióváltozásainak elvesztése és a komplement aktivátorok funkcióváltozásának növekedése.2 A kulcsfontosságú negatív AP szabályozó a H faktor (FH), és az FH hiánya emberben, sertésben és egerben a C3G-hez kapcsolódik. 3 C3 nephritis faktor, az AP C3 konvertázt stabilizáló antitest gyakori a C3G-ben.4 A C3 nefritikus faktor önmagában a C3 (properdin-független C3 nefritikus faktor) vagy a C3 és C5 (properdin- függő C3 nephritis faktor).5,6
Bár a megfelelődin-hiány nem javította a plazma C3-szintjét, a C5-szint emelkedett, ami arra utal, hogy a megfelelődin szükséges a C5, de nem a C3-konvertáz aktivitásához.8,9

Egér10 vagy humán FH11,12 beadása Cfh–/– egereknek csökkentette a glomeruláris C3 festődést és megnövelte a keringő C3 szintet. Azok a konstrukciók, amelyek csak az FH szabályozó és célzó doménjeit (mini-FH molekulák) tartalmazzák, szintén hatékonyak ebben a modellben.13 Más megközelítések magukban foglalják azokat a fehérjéket is, amelyek a komplement aktiváció helyeit célozzák meg. Ezek közé tartozik a TT30,14, amely az FH (FH1-5) komplement szabályozó doménjeit tartalmazza a komplement receptor 2 komplementkötő doménjeihez kapcsolva, valamint homodimer FH molekulák, 15 olyan mini-FH molekulák, amelyek komplementkötő domént tartalmaznak. H-faktorral rokon fehérje 1.
Mivel a C3G-ben a komplement C3 aktiváció gátlásának terápiás hasznosságát vizsgálják,2 fontos megérteni a glomeruláris C3 lerakódás kinetikáját és kapcsolatát az AP aktivációval mind a glomerulusokban, mind a keringésben. Az immunkomplex által közvetített glomerulonephritis modelljeiben a glomeruláris C3c a komplement aktiváció megakadályozását követő 24 órán belül kiürült, míg a glomeruláris C3d hetekig fennmaradt.16 Hasonlóképpen, a Cfh–/– egerekben az exogén FH a glomeruláris C3c festődés csökkenését eredményezi 24 órán belül. , míg a glomeruláris C3d változatlan marad.11
Ebben a tanulmányban két új, komplement szabályozó aktivitással rendelkező fúziós fehérje hatékonyságát vizsgáltuk Cfh–/– egérmodellben a C3G-ben. A fehérjék tartalmazták az egér FH szabályozó doménjét (FH1-5), amelyet egér Ig-hez konjugáltak a biológiai felezési idő meghosszabbítása érdekében. Az egyik fúziós fehérje, az IgG-FH1-5, egy nem célpont egér monoklonális antitesthez volt konjugálva. A másik, az anti-P-FH1-5, az egérpropindin elleni monoklonális antitesthez volt konjugálva. Ezt annak a hipotézisnek a tesztelésére tették, hogy ennek a fúziós fehérjének a komplementaktivációs helyekre történő megcélzása a megfelelődin-lerakódással való kölcsönhatás révén fokozza a szöveti komplement szabályozását. Adataink azt mutatják, hogy mind a non-targetting (IgG-FH1-5), mind a propertydin-targeting (anti-P-FH1-5) fehérjék helyreállították a plazma és a glomeruláris C3 szabályozást Cfh–/– egerekben. Időbeli vizsgálatok azt mutatták, hogy a C3 és FB szintek helyreállítása a keringésben lévő fúziós fehérjék szintjét tükrözte. Ezzel szemben a plazma C5 növekedése megmaradt, miután a fúziós fehérjék kiürültek a keringésből. Kimutattuk, hogy az IgG-FH1-5 enyhítette a glomeruláris károsodást a felgyorsult szérum nephrotoxikus nephritis során Cfh–/– egerekben.

A cistanche kezelheti a vesebetegséget, javíthatja a veseműködést
EREDMÉNYEK
Fúziós fehérjék előállítása és az aktivitás in vitro és in vivo értékelése A fúziós fehérjéket úgy hozták létre, hogy az egér FH (FH1-5) első 5 rövid konszenzus ismétlődő (SCR) doménjét összekapcsolták vagy egy egér elleni megfelelő antitesttel (anti). -P-FH1-5) vagy nem célzó Ig-domént tartalmazó antitest (IgG-FH1- 5, S1 kiegészítő ábra). A fehérjék aktivitását AP-specifikus hemolitikus vizsgálattal értékeltük (1a. ábra). Az anti-P-FH1-5 és az IgG-FH1-5 dózisfüggő módon gátolta a hemolízist, és az anti-P-FH1-5 hatásosabb volt. Az anti-properdin (anti-P) szintén dózisfüggő módon csökkentette a hemolízist, de az IgG-kontrollnak nem volt hatása. A fehérjék ekvimoláris injekciója után Cfh–/– egerekbe az IgG-FH1-5 fehérje az injekció beadása után 11 napig, míg az anti-P-FH1-5 4 nappal az injekció beadása után volt kimutatható. injekció (S2 kiegészítő ábra). Annak megállapítására, hogy az IgG-FH1-5 és az anti-P-FH1-5 visszaállíthatja-e a plazma AP szabályozását Cfh–/– egerekben, először megmértük a plazma C3-szintjét a fúziós fehérjék injekciója után (1b. ábra). . Az IgG-FH1-5 vagy az anti-P-FH1-5 beadása szignifikánsan növelte a plazma C3-értékét az injekció beadása után 24 órával, kisebb mértékben pedig 96 órával (1b. ábra). Ezek az adatok azt mutatták, hogy mind az IgG-FH1-5, mind az anti-P-FH1-5 ideiglenesen helyreállíthatja a plazma AP szabályozását Cfh–/– egerekben. Ezt követően ezeknek a változásoknak a részletes elemzését végeztük el, nemcsak a plazma C3-ban, hanem a plazma C5-ében és az alternatív útvonalú fehérjékben, az FB-ben és a megfelelőben is. Cfh–/– egerekben az IgG-FH1-5 és az anti-P-FH1-5 beadása után a keringő C5- és megfelelődinszint emelkedése tovább tart, mint a C3 és FB növekedése.
Összehasonlítottuk a C3, C5, FB és propertydin változásainak kinetikáját oly módon, hogy akár 27 napos időközönként mértük a fehérjéket akár az IgG-FH1-5, akár az anti-P-FH1-5 egyszeri injekció után. 2. ábra). Az IgG-FH1-5 beadása után a C3, C5, FB és propertydin csúcsértéke az injekció beadása utáni 1. napon következett be. Az idő, amíg ezek a változások a kezelés előtti szintre estek, eltérő. A kezelés előtti szintre való visszatérés az 1. és 4. nap között következett be az FB esetében, a 7. és a 11. nap között a C3 esetében, és a 14. és 21. nap között mind a megfelelő, mind a C5 esetében (2a, c, e és g ábra). Az anti-P-FH1-5 beadása után a C3 csúcsszintek az 1. napon következtek be, de a 4. és 7. nap között a kezelés előtti szintre csökkentek (2b. ábra). A C5 csúcsszint a 4. napon volt, és a 7. és 11. nap között tért vissza a kezelés előtti szintre (2d. ábra). A FB csúcsemelkedése az 1. napon következett be, és az 1. és 4. nap között a kezelés előtti szintre esett (2f ábra). Ahogy az várható volt, a szabad plazma megfelelődin kimerült az anti-P-FH1-5 vagy az anti-P injekció beadása után (2h ábra). A szabad plazmaproperdin szintje az anti-P-FH{50}} után 7 napig, az anti-P után pedig 14 napig alacsony maradt (2h ábra). Bár mindkét fúziós fehérje átmenetileg helyreállította a plazma AP szabályozását, a C3, FB és C5 szintek javulásának időtartama a plazmában való kimutatásuk időtartamát tükrözte, ami rövidebb volt az anti-P-FH1-5 esetében (S2 kiegészítő ábra) . Összefoglalva, a C3 és az FB szintjében bekövetkezett változások bármelyik fehérje injekciója után rövidebbek voltak, mint a C5 és a propidin szintjében. Ezek az adatok arra utalnak, hogy a plazma FB a C3 konvertáz aktivitás érzékeny markere ebben a helyzetben, míg a megfelelődin a C5 konvertáz aktivitás markere. Nevezetesen, az anti-P injekció után a C5 emelkedett a 24. és 96. órában, valamint a 7. napon.
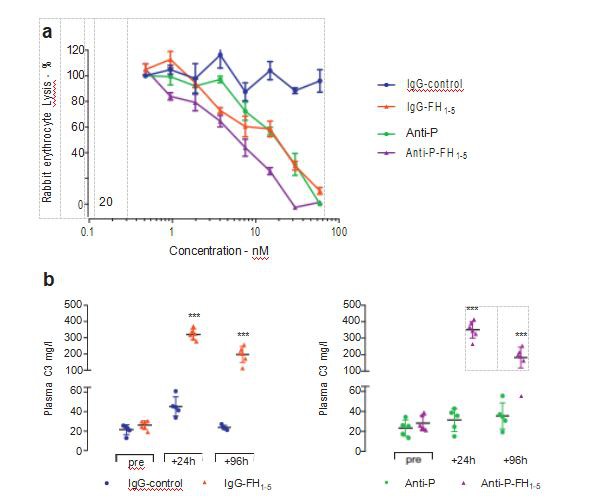
1. ábra| (a) Alternatív útvonal-függő hemolízis vizsgálat kiegészítése. Az antitesteket 2-szeres hígításokban titráltuk 60 nM-tól 0,5 nM-ig. Az IgG-FH1-5, az anti-P-FH1-5 és az anti-P reagensek dózisfüggő módon csökkentették a nyúl eritrocita hemolízisét. Nem alkalmaztunk gátlást az IgG-kontroll fehérjével. A vízszintes oszlopok az átlagértékeket, a hibasávok pedig az SD-t jelölik. (b) Plazma komplement C3 Cfh–/– egerekben fúziós fehérjék injekciója után. A C3 plazmaszintet az IgG-FH1-5 (piros háromszögek, n ¼ 5) beadása előtt és 24 órával és 96 órával azután mértük. Anti-P–FH1-5 (lila háromszögek, n ¼ 6), Anti -P (zöld pontok, n ¼ 5) és IgG-kontroll (kék pontok, n ¼ 5). A vízszintes oszlopok az átlagértékeket, a bajuszok pedig az SD-t jelölik. ***P # 0,001 az előkezelési értékhez képest, és a Bonferroni többszörös összehasonlítási teszttel végzett 2-módú ANOVA-ból származik. FH, H faktor; P, megfelelődin.
(2d. ábra). Amint arról beszámoltunk, a 8,9 azt jelzi, hogy a C5-konvertáz a megfelelődintől függ Cfh–/– egerekben.
Az IgG-FH1-5 és az anti-P-FH1-5 csökkentette a glomeruláris C3c-t, de nem változtatta meg a C3d festődést Cfh–/– egerekben
Ezt követően értékeltük az IgG-FH1-5 és az anti-P-FH1-5 hatását a glomeruláris C3b/iC3b/C3c, C3d, propertydin és FH-rokon (FHR) fehérjékre. Az IgG-FH1-5 injekció után 96 órával a glomeruláris C3b/iC3b/C3c festődés csökkent, de a glomeruláris C3d (3a. ábra) és FHR festődés (3b. ábra) nem. A glomeruláris C3b/iC3b/C3c változatlan maradt sem IgG-kontrollal, sem anti-P-vel. A kezeletlen Cfh–/– egerekben9 a glomeruláris megfelelő festődés rendellenes lineáris mintázata 96 órával az IgG kontroll után is megmaradt. Az anti-P-vel vagy IgG-FH1-5-val injektált Cfh–/– egerekben a glomeruláris property-szint szinte kimutathatatlan volt 96 órával (3b. ábra). Az anti-P-FH1-5 injekció váratlanul szemcsés glomeruláris festődést eredményezett anti-properdin, anti-FH/FHR és anti-IgG antitestek felhasználásával (3b. ábra). Ez a megállapítás arra utalt, hogy az anti-P-FH1-5 fehérje lerakódott a glomerulusokban. Az anti-P-FH1-5 fehérje vad típusú egerekbe való injekciója glomeruláris festődést eredményezett anti-properdin, anti-FH/FHR és anti-IgG antitestekkel 96 óra elteltével (S3 kiegészítő ábra), ami azt jelzi, hogy ez A reagens kölcsönhatásba lép a normál glomerulusokkal. Feltételeztük azonban, hogy az anti-P-FH1-5 fehérje kölcsönhatásba léphet a Cfh–/– egerekben már meglévő glomeruláris megfelelőjével is. Amikor a reagenst befecskendeztük Cfh–/– egerekbe, amelyeket anti-P-vel előkezeltek a glomeruláris properdin eltávolítására, csökkent a szemcsés festődési mintázat anti-properdin, anti-FH/FHR és anti-IgG antitestek használatával ( Kiegészítő S4) ábra). Ezek a megfigyelések azt mutatják, hogy az anti-P-FH1-5 fehérje glomeruláris kölcsönhatása Cfh–/– egerekben részben a glomeruláris megfelelődintől függ.

Az IgG-FH1-5 javította a vesekárosodást a felgyorsult szérum nephrotoxikus nephritis során Cfh–/– egerekben
A C3G-ben szenvedő betegeknél akut vesekárosodás alakulhat ki interkurrens fertőzésekkel összefüggésben. Például az FHR5 nefropátia esetén a vesefunkció elvesztése synpharyngitises makroszkópos hematuria epizódjaihoz kapcsolódik.17 A C3G-betegeknél a mögöttes C3 szabályozási zavar valószínűleg fokozott komplement-mediált vesekárosodáshoz vezet egy olyan trigger után, amely vesegyulladást eredményez. Ennek modellezésére felgyorsult szérum nephrotoxikus nephritist indukáltunk, amely egy immunkomplex

2. ábra| A plazma komplement profil időbeli lefutása IgG-FH1-5 és anti-P-FH1-5 injektált Cfh–/– egerekben. Plazma C3 (a,b), C5 (c,d), FB (e,f) és propertydin (P; g,h) a kísérlet kezdetétől az egyszeri IgG-FH{{1{{21) injekciót követő 27. napig }}}} (a,c,e,g; piros háromszögek, n ¼ 5) vagy anti-P-FH1-5 (b,d,f,h; lila háromszögek, n ¼ 6). A kontrollok közé tartozott az anti-P (zöld pontok, n ¼ 5) és egy izotípusnak megfelelő monoklonális antitest (IgG-kontroll; kék pontok, n ¼ 5). A vízszintes oszlopok az átlagértékeket, a bajuszok pedig az SD-t jelölik. *P # 0.05, **P # 0,01, ***P # 0,001 az előkezelési értékhez képest, és a Bonferroni többszörös összehasonlító teszttel végzett 2-módú varianciaanalízisből származik. FB, B faktor; FH, H faktor.
glomerulonephritis modell, amely magában foglalja a komplement és az Fc receptor által közvetített útvonalakat,18,19 a Cfh–/– egerekben. Korábban kimutattuk, hogy a Cfh–/– egerek ebben a helyzetben túlérzékenyek a vesekárosodásra7, és feltételeztük, hogy az FH1-5 fehérje az AP szabályozásának fokozásával javíthatja a komplement által közvetített vesekárosodást ebben a modellben. Mivel adataink azt mutatták, hogy az anti-P-FH1-5 fehérje normál glomerulusokban rakódott le, IgG-FH1-5-t alkalmaztunk felgyorsult szérum nephrotoxikus nephritis során. Huszonnégy órával a juhok nefrotoxikus szérumának injekciója előtt az egerek vagy IgG-kontroll (n ¼ 7) vagy IgG-FH1-5 (n ¼ 8) ip injekciót kaptak. A kísérleti protokollt a 4a. ábra mutatja be. Az egereket 6 nappal a juh-nefrotoxikus szérum beadása után selejteztük le. A glomeruláris patológia mindhárom szövettani mérőszáma (súlyossági pontszám, teljes sejtszám és makrofágszám) szignifikánsan alacsonyabb volt az IgG-FH1-5 csoportban (4b. ábra). A tubulointerstitialis sérülés is alacsonyabb volt az IgG-FH1-5 csoportban (4b. ábra). A szérum karbamid szintje jelentősen megemelkedett

3. ábra| Glomeruláris komplement immunfestés Cfh–/– egerekben 96 órával az IgG-FH1-5 vagy az anti-P-FH1-5 injekció után. (a) Reprezentatív képek a glomeruláris C3b/iC3b/C3c és C3d mennyiségi meghatározásával együtt a 4 kísérleti csoportban: IgG-FH1-5 (piros háromszögek, n ¼ 5), anti-P-FH1-5 (lila háromszögek, n ¼ 6), anti-P (zöld pontok, n ¼ 5) és IgG-kontroll (kék pontok, n ¼ 5). A plazmaC3 szintje az 1. ábrán látható szemcseppek idején. (b) Az adatpontok medián értékeket, a whiskerek pedig egy interkvartilis tartományt jelölnek. A Kruskal-Wallis tesztből származó P értékek Dunn többszörös összehasonlítás teszttel. (b) A glomeruláris IgG, FHR és festés reprezentatív képei a 4 kísérleti csoportban. Bar ¼ 100 mm. AFU, tetszőleges fluoreszcens egységek; FH, H faktor; P, megfelelődin. A kép megtekintésének optimalizálásához tekintse meg a cikk online változatát a címenwww.kidney-international.org.
az IgG-kontroll csoportban, de a szérum albumin és a vizelet albumin-kreatinin arány változásai nem különböztek (4b. ábra). Ahogy az várható volt, a glomeruláris C3b/iC3b/C3c szignifikánsan csökkent az IgG-FH1-5 csoportban (4b. ábra), de a glomeruláris egér IgG (4b. ábra) és a birka IgG (az adatok nincsenek feltüntetve) nem különbözött a csoportok között. .
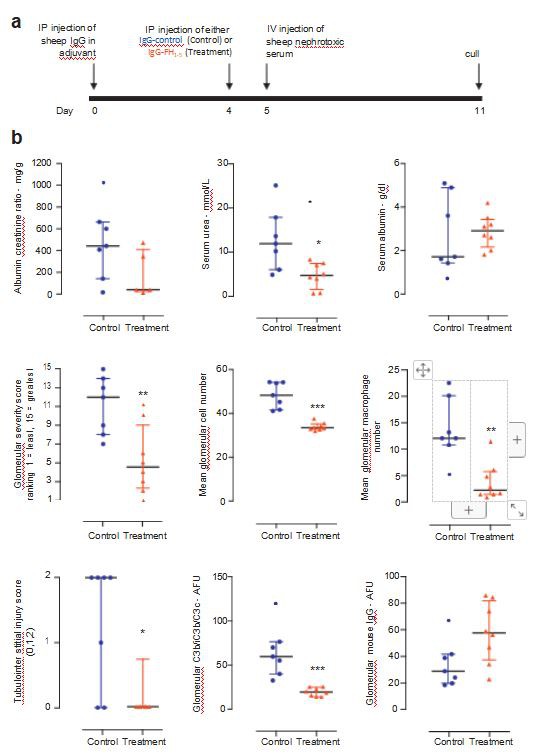
4. ábra| Az IgG-FH1-5 előkezelés javította a vesekárosodást a felgyorsult szérum nephrotoxikus nephritis során Cfh–/– egerekben. (a) A gyorsított szérum nephrotoxikus nephritis protokoll vázlata. A juh-IgG-vel előimmunizált egerek vagy IgG-FH1-5-t (kezelési csoport, n ¼ 8) vagy IgG-kontrollt (kontrollcsoport, n ¼ 7) kaptak 24 órával a birka nefrotoxikus szérum beadása előtt. (b) Vesefunkció és szövettan 6 nappal a felgyorsult szérum nephrotoxikus nephritis indukálása után IgG-FH1-5 (kezelés; piros háromszögek, n ¼ 8) vagy IgG-kontroll (kontroll; kék körök, n) egerekben ¼ 7). A vízszintes oszlopok a medián értékeket, a whiskerek pedig egy interkvartilis tartományt jelölnek. *P # 0.05, **P # 0,01, ***P # 0,001 a kontrollhoz képest, és a Mann-Whitney tesztből származik. FH, H faktor; P, megfelelődin.
VITA
Mind az IgG-FH1-5, mind az anti-P-FH1-5 normalizálta a C3, FB és C5 szintet Cfh–/– egerekben. Ez a megállapítás összhangban van azzal a ténnyel, hogy az egér FH komplement szabályozó doménjei az 1-5 SCR doméneken belül helyezkednek el (egy C3b-kötő hely és a C3b I-es faktor által közvetített hasításának kofaktoraktivitása).20 Felületfelismerő domének, amelyek befolyásolják a heparinhoz és az endothel sejtekhez való kötődést, és tartalmaznak egy második C3b-kötő helyet, jelen vannak az SCR doméneken belül 18-tól
20 (FH18-20), és ezért nincsenek jelen a fúziós fehérjékben.20 Mindazonáltal mindkét fehérje csökkentette a glomeruláris iC3b/C3b/C3c-t, ami azt jelzi, hogy az FH18-20 nem szükséges ebben a beállításban. Ez a megállapítás összhangban van azokkal a korábbi adatokkal, amelyek azt mutatják, hogy az 1–15. SCR doménből álló mutáns FH-fehérjét expresszáló Cfh–/– egerekben (Cfh–/– .FHD16-20) nem alakult ki rendellenes C3 glomeruláris lerakódás.21,22 A Cfh–/–.FH D16-20 állatok azonban nem tudták szabályozni a C3 aktivációt a vese endotéliumában, és thromboticus microangiopathia alakult ki. Lehetséges, hogy a felszíni célzó FH18-20 domének hiánya miatt az FH1-5-ot tartalmazó fúziós fehérjék beadása FH hiány esetén thromboticus microangiopathiára való fogékonyságot eredményezhet. Az is lehetséges, hogy a fúziós fehérjék dimer szerkezete alatt megnövekedett C3b-kötési aviditás elegendő ahhoz, hogy kompenzálja a felületet célzó FH18-20 domének hiányát. A C3b felszíni felismerését azonban az FH konformációs változásai is befolyásolják.23 A Streptococcus pneumoniae FH-kötő fehérje (PspCN, amely az SCR 9-es domént köti) FH konformációs változást vált ki, és az FH-PspCN komplex megnövelte a C3b kötődését és fokozott bomlásgyorsító aktivitás. Az FH20 C3d-kötő helye nem látható az FH-ban, de az FH-PspCN komplexben szabaddá válik. Ez megmagyarázhatja, hogy az FH19-20 miért lép kölcsönhatásba a C3d felülettel, de az FH nem.24,25 Feltételezzük, hogy ágenseink a konformációs változásokon keresztül hatékonyan kölcsönhatásba léphetnek mind a folyékony fázissal, mind a felületi C3b-vel. Nevezetesen, mind az IgG-FH1-5, mind az anti-P-FH1-5 megvédte a vörösvértesteket a lízistől egy AP-függő hemolízis vizsgálatban.
Egyik fúziós fehérje sem csökkentette a glomeruláris C3d festődést, talán a glomeruláris C3d perzisztens természete miatt. Kísérleti immunkomplex nephritisben a glomeruláris C3c a komplementaktiváció megszűnését követő 24 órán belül feloldódott, de a C3d hetekig fennmaradt.16 Ezenkívül a glomeruláris C3d perzisztens lupus nephritisben.26 Ez valószínűleg a glomeruláris felületekkel való kovalens kölcsönhatását tükrözi. A humán FH ismételt injekciói Cfh–/– egerekben a glomeruláris C3d csökkenését mutatták 10 nap alatt.11 Valószínű, hogy az IgG-FH1-5 ismételt adagolása csökkentheti a glomeruláris C3d mennyiségét ebben a modellben. A glomeruláris FHR festődésben sem volt változás. Keveset tudunk az egér FHR fehérjék funkcióiról, de képesek kölcsönhatásba lépni a C3b27, 28 és C3d fehérjékkel is.27 Valójában mind az FHR-A, mind az FHR-B látszólagos affinitása a C3d-hez erősebb, mint az FH-é.27 Feltételezzük, hogy a glomeruláris FHR fehérjék valószínűleg csak a C3d eltávolítása után válnak ki a glomerulusokból. Ebben az összefüggésben figyelemre méltó, hogy a humán C3G-ben a H-faktorral rokon 5-ös fehérje a glomeruláris C3d-vel társul.29
Az anti-P-FH1-5 fehérje a vártnak megfelelően csökkentette a szabad plazmaproperdin szintjét, mivel ennek a fúziós fehérjének az antiproperdin része egyetlen injekció után 8 napig blokkolhatja az AP aktivitást (aproperdin kimerülése miatt).30 adataink azt mutatták, hogy az FH1-5 hatékonysága a plazma C3-szintjének növelésében és a glomeruláris C3b/iC3b/C3c festődés csökkentésében összehasonlítható volt a 2 fúziós fehérje között (azaz független volt a megfelelő célzástól). Ezenkívül az abnormális glomeruláris megfelelő festődés jelentősen csökkent akár anti-P, akár IgG-FH1-5 beadása után. Nyilvánvaló, hogy a C3d- és FHR-fehérjékkel ellentétben a glomerulus megfelelője a C3-szabályozás helyreállítása után könnyen kiürül. Az anti-P-FH1-5 fehérje beadása után megváltozott a glomeruláris megfelelődin mintázata, de ezt bonyolította az a megfigyelés, hogy mind a Cfh–/–, mind a vad típusú glomerulusokban kimutattuk ennek a fúziós fehérjének a lerakódását. Ez részben a glomeruláris megfelelődinnel való kölcsönhatásnak köszönhető, de a vad típusú glomerulusokban való lerakódás azt jelezte, hogy részben teljesen független a glomeruláris komplementtől, és valószínűleg a fúziós fehérje fizikai-kémiai tulajdonságaival függ össze.
Kinetikai adataink új eredményeket mutattak be az FB, C5 és propertydin időbeli változásaival kapcsolatban, amelyek a Cfh–/– egerekben a C3 növekedésével járnak a fúziós fehérjék injekciója után. Az FB szintje gyorsan emelkedett az injekció után
és visszatért a kiindulási szintre egy olyan időpontban, amikor mind a C5, mind a megfelelődin szintje emelkedett maradt. A Cfh–/– egerekben a properdinszint a kiinduláskor csökkent, majd az IgG-FH1-5 injekciót követően a normál szintre emelkedett (20 mg/ml30), és ezen a szinten maradt legalább 14 napig. Hasonló időbeli lefutást figyeltek meg a plazma C5-szintjének emelkedése. Meglepő módon az IgG-FH1-5 a 11. napon többnyire hiányzott a keringésből, ami azt jelzi, hogy a Cfh–/– egerekben a C5 konvertáz képződése lassabb, mint a C3 konvertázé (mivel a C3 szintjei visszatértek a kiindulási értékre 7 és 11 nap). A plazma C5 szintje növekedett az anti-P kezelés után, és tovább nőtt az anti-P-FH1-5 fehérje hatására. Ennélfogva mind a propertydin-célzás, mind az FH1-5 hatásai hozzájárultak a megnövekedett C5-szinthez, és azt jelzik, hogy a C5-konvertáz részben propertydin-függő Cfh–/– egerekben. Ez a megállapítás összhangban van a C5 szabályozási zavar enyhülésével olyan egerekben, ahol az FH és a megfelelődin kombinált hiánya van.8,9 A keringő megfelelődin szintje csökkenthető a C3G-ben, és úgy tűnik, hogy korrelál a felszíni C5 konvertáz aktivitással, ellentétben akár a plazma C5-tel, akár az oldható C5b{val. {30}}.31,32 Adataink alátámasztják a bensőséges kapcsolatot a propertydin szintje és a C5-konvertáz aktivitása között, és alátámasztják a property-szintek használatát a folyamatban lévő glomeruláris C5-aktiváció biomarkereként.
Nevezetesen, az IgG-FH1-5 fehérje egyetlen injekció után 11 napig is kimutatható volt a keringésben. Ez sokkal hosszabb, mint amit korábban a konjugálatlan egér FH1-5 fehérjére vonatkozóan közöltünk, amely 24 órán belül kikerült a keringésből.14 Ez a megállapítás arra utal, hogy az IgG-FH{ hosszabb plazma felezési ideje A {9}} fehérje az antitest-konjugációból származik. Az IgG-FH1-5 fehérje plazma felezési ideje is hosszabb volt, mint amit korábban a teljes hosszúságú FH esetében megfigyeltünk.10,11 Például a humán FH egyetlen injekció után 96 órával távozott a keringésből. Cfh–/– egerekben.11 Az IgG-FH1-5 fehérje hatékonyságát a komplement szabályozásban igazoló adatainkkal együtt úgy gondoljuk, hogy az FH1-5 fehérje konjugációja a farmakokinetikai profiljának meghosszabbítása érdekében potenciális terápiás hatású. segédprogram a C3G-ben.
Összefoglalva, megmutatjuk, hogy a felületfelismerő domének hiánya ellenére az FH1-5 fúziós fehérjék hatékonyan csökkentették a glomeruláris C3 aktivációt és helyreállították a plazma komplement szabályozását FH-hiány esetén. Nem volt nyilvánvaló előny az FH1-5 domének anti-properdinnel való konjugálásában, és az IgG-FH1-5 fehérje csökkentette a vesekárosodást kísérleti nephritisben. A terápiás felhasználásra szánt FH nagyléptékű készítményeinek előállítása kihívásaival ellentétben az antitest-alapú terápiák nagy léptékű előállítása jól megalapozott, ami az IgG-FH-t{10}} vonzó potenciális terápiás hatásúvá teszi a C3G számára.
MÓD
Fúziós fehérjék
IgG-FH1-5. Az első 5 egér FH SCR tartomány (mFH1-5) összekapcsolva
egy nem célzó IgG1 egér Ig-hez (egér monoklonális antitest ellen termelt anti-idiotípusos antitest).
Anti-P-FH1-5. Az egér FH1-5 egér anti-properdin antitesttel (anti-P) kapcsolva,30 W. Song, Pennsylvania Egyetem biztosította Alexionnak).
Vezérlők. A kontrollok az izotípushoz illesztett, nem célzó egér Ig (IgG-kontroll) és az egér anti-properdin (anti-P) voltak (S1 kiegészítő ábra). A fehérjéket pVEK vektorok és Expi293 sejtek (Thermo Fisher Scientific, Waltham, MA) felhasználásával állítottuk elő, protein A-val tisztítottuk (MabSelect SuRe, Cytiva, Marlborough, MA).
AP-specifikus hemolitikus vizsgálat
A 20%-os normál egérszérumot 60 nM-ról 0,5 nM-ra titrálva nyúl eritrocitákkal (15 106 sejt/ml) inkubáltuk 37 C-on 30 percig. A hem felszabadulást spektrofotometriásan határoztuk meg (optikai sűrűség 415 nm); A 100 százalékos lízis szérum volt inhibitor nélkül.
Plazma FB és FH
A plazmát etilén-diamin-tetraecetsavat tartalmazó csövekbe gyűjtött vér centrifugálásával nyertük (Sarstedt, Nordrhein-Westfalen, Németország). A fehérjéket kapilláris elektroforézises immunoassay-vel mértük (WES, ProteinSimple, San Jose, CA). Az alkalmazott antitestek a poliklonális anti-egér FH antitest (Alexion Pharmaceuticals, Boston, MA) és az anti-egér FB antitest (Abcam, Cambridge, Egyesült Királyság); WES anti-nyúl detektáló modult (ProteinSimple, San Jose, CA) használtunk. A kemilumineszcens jeleket Compass for SW szoftverrel (ProteinSimple, 5-ös verzió.{6}}.1) elemeztük, csúcsterületként határoztuk meg, és a vizsgálati kontrollhoz normalizáltuk.
Egerek
Minden egeret meghatározott patogénmentes körülmények között tartottunk; Az eljárásokat az intézményi irányelvek szerint végezték, és az Egyesült Királyság Belügyminisztériuma hagyta jóvá. A C57BL/6 vad típusú egereket a Jackson Laboratory-tól (Bar Harbor, ME) vásároltuk, és a Cfh–/– egereket a korábban leírtak szerint állítottuk elő.7 Az egereket koruk és nemük szerint egyeztettük; ekvimoláris dózisú fehérjéket ip injekcióval adtunk be (1 mg anti-properdin és IgG-kontroll; 1,4 mg IgG-FH1-5 és anti-P-FH1-5). A felgyorsult szérum nephrotoxikus nephritist birka nefrotoxikus szérum iv. injekciójával váltottuk ki juhok IgG-vel előimmunizált egerekbe.7 A fúziós fehérjék beadását 24 órával a juh nefrotoxikus szérum indukciója előtt végeztük (4a. ábra).
C3, C5 és szabad propidin A plazma C3 mérését enzimhez kötött immunszorbens vizsgálattal végeztük.14 A plazma „mentes” propridin- és C5-szintjét elektrokemilumineszcenciás immunoassay-k segítségével (Meso Scale Discovery [MSD], Meso Scale Diagnostics, Rockville, MD) mértük az antitesttel. - Properdin vagy egyedi anti-egér C5 bevonattal nagy kötőképességű MSD lemezeken. A kötött "szabad" properdint és C5-öt anti-properdinnel (W. Song) vagy biotinilált monoklonális anti-C5-tel (Alexion) sztreptavidin-SULFO-val kombinálva (MSD, Meso Scale Diagnostics) mutattuk ki. A kemilumineszcens jelet egy SECTOR S 6000 képalkotó (MSD, Meso Scale Diagnostics) segítségével vettük fel, és az MSD Discovery Workbench szoftverrel (Meso Scale) elemeztük.
Diagnosztika, 4-es verzió.{1}}.12.1). Standardként rekombináns egér-propidint és C5-öt használtunk.
Vesefunkció és szövettan
A hematuria és proteinuria értékelését Hema-Combistix (Bayer, Reading, Egyesült Királyság) alkalmazásával végeztük; A plazma karbamid szintjét megmértük, és a veseszövetet a korábban leírtak szerint dolgoztuk fel.9 A vizelet kreatinint spot vizeletmintákból határoztuk meg a Creatinine Companion Protocol assay (#1012; Excell, Philadelphia, PA) és spot vizelet/ A plazma albumint enzimhez kötött immunszorbens vizsgálattal (#E99-134; Bethyl Laboratories, Montgomery, TX) mérték. A periodikus sav-Schiff-festett vesemetszeteket vak módszerrel értékelték, és a glomeruláris és tubulointerstitialis sérülés súlyossága szerint rangsorolták (0 [nincs], 1 [enyhe], 2 [közepes]). Metszetenként tíz glomerulust értékeltünk, hogy meghatározzuk az átlagos glomeruláris sejtszámot. Az immunfluoreszcenciás festést 5- mm-es kriometszeteken végeztük, amelyeket Vectashield táptalajjal és DAPI-val szereltek fel (Vector Laboratories, Burlingame, CA). A használt antitestek a következők voltak: fluoreszcein-izotiocianát (FITC) konjugált poliklonális kecske anti-egér C3b/C3c/iC3b (1:200; #55500; MP Biomedical, Santa Ana, CA)9; Fügelánc-specifikus FITC-konjugált poliklonális kecske anti-egér IgG (1:400; #F5387; Sigma-Aldrich, St. Louis, MO); FITC-konjugált monoklonális egér anti-kecske/birka IgG (1:100; #F5137; Sigma-Aldrich); vagy FITC-konjugált kecske anti-humán propidin (1:50; #GAHu/PPD/FITC, Nordic Immuno logic Laboratories, Koppenhága, Dánia).9 Biotinilált kecske anti-egér C3d (1:10; # BAF2655; R&D Systems , Minneapolis, MN) biotinnal blokkolt metszeteken (Biotin Blocking System; Agilent Dako, Santa Clara, CA), streptavidin AF488 másodlagos antitesttel (1:200; #S-32354; Thermo Fisher Scientific) alkalmazták. Az FH-t tisztított patkány anti-egér CD16/CD{52}}blokkolt metszetekben (1:100; BD Biosciences, Franklin Lakes, NJ) kecske anti-humán FH-val (1:1000; #A312; Quidel, San Diego) tettük láthatóvá. , CA) és monoklonális anti-kecske IgG-FITC másodlagos antitest (1:100; klón GT-34; F4891; Sigma-Aldrich). A glomeruláris makrofágokat FITC-konjugált patkány anti-egér CD68 (FA{69}} klón GTX43518; GeneTex, Irvine, CA) segítségével azonosítottuk. A kvantitatív immunfluoreszcencia analízist Leica DM4B optikai mikroszkóppal, Leica DFC700T digitális kamerával (Leica Microsystems, Wetzlar, Németország) és Image-Pro Plus szoftverrel (Media Cybernetics, Rockville, MD, 7-es verzió) kapcsoltuk. Metszetenként tíz glomerulust vizsgáltunk, és az átlagos intenzitást tetszőleges fluoreszcens egységekben fejeztük ki.
Statisztikai analízis
A statisztikai elemzéshez a GraphPad Prism 8-as verzióját.{1}} (GraphPad, San Diego, CA) használtuk. Ismételt mérésű 2-módszeres varianciaanalízist a Bonferroni többszörös összehasonlító teszttel (tényezők az idő és a kezelés) használtuk az időbeli lefolyás-analízishez. Több csoport összehasonlításakor Kruskal-Wallis és Dunn többszörös összehasonlítás tesztet, 2 csoportnál Mann-Whitney tesztet alkalmaztunk.
KÖZZÉTÉTEL
Az MCP tanácsadói díjakat kapott az Alexion, a ChemoCentryx, a Novartis, a Gyroscope és az Achillion Pharmaceuticals cégtől. A HTC tanácsadói díjakat kapott az Alexiontól, a Novartistól, az Auriniától és az Achillion Pharmaceuticalstól. YZ, YW, KKJ és SK-K az Alexion Pharmaceuticals alkalmazottai. SK az Alexion Pharmaceuticals korábbi alkalmazottja, jelenleg a Gemini Pharmaceuticals alkalmazottja. A többi szerző nem nyilatkozott egymással versengő érdekekről.
KÖSZÖNETNYILVÁNÍTÁS
Az MCP a Wellcome Trust Senior Fellow a klinikai tudományok területén (a támogatási szám: 212252/Z/18/Z), és ez az ösztöndíj az ACG-t és a DPL-t támogatja. Az YZ-t, SK-t, YW-t, KKJ-t és SK-K-t az Alexion Pharmaceuticals finanszírozta.
KIEGÉSZÍTŐ ANYAG
Kiegészítő fájl (PDF)
S1 ábra. Az ebben a vizsgálatban használt Fusionprotein.IgG-FH1-5 tartalmazza az egér H-faktor (FH1-5) első 5 doménjét, egy nem célzó egér Ig-hez kapcsolva. Az Anti-P-FH1-5 mFH1-5-ból áll, amely egy semlegesítő egér-antiegér-propridin-antitesthez kapcsolódik (anti-P; lásd: Miwa et al.30). A kontroll fehérjék közé tartozott az izotípushoz illeszkedő, nem célzó egér Ig (IgG-kontroll) és a neutralizáló egér anti-egér megfelelő antitest (Anti-P). S2 ábra. WES blot analízis az FH1-5 kimutatására FH-hiányos egerek plazmamintáiban, amelyekbe (A) IgG-FH1-5 vagy (B) Anti-P-FH1-5 injekciót adtak. A 94-kDaIgheavychainlinkedtomouseFH1-5 (HC-FH1-5) az IgG-FH1-5 injekció beadása után 11 nappal és az anti-P-FH1-5 fehérje injekciója után legfeljebb 4 nappal (piros dobozok) kimutatható ).A kontrollok közé tartozik a vad típusú egerek plazmája, ahol a teljes hosszúságú H-faktor fehérjét detektálták (FH, fekete dobozok, C1 sáv) és nem injektált FH-hiányos egerek, ahol nincs FH (fekete dobozok, C2 sáv). Ahogy az várható volt, az FHnorFH1-5 sem mutatható ki az Anti-P-vel vagy IgG-kontrollal injektált egerek plazmamintáiban.
S3 ábra. Glomeruláris komplement immunfestés 96 órával az IgG-kontroll vagy anti-P-FH1-5 injekció beadása után vad típusú egerekben. Reprezentatív glomeruláris képek láthatók (sáv ¼ 100 mm).
S4 ábra. A megfelelődin szerepe az anti-P-FH1-5 lerakódásában FH-hiányos egerek glomerulusaiban. A Cfh–/– egerekbe vagy IgG-kontrollt vagy anti-P-t (1. kezelés) fecskendeztek, majd 24-órával később IgG-kontrollt vagy anti-P-FH-t1-5 (2. kezelés). Az állatokat az első kezelés után 120 órával levágtuk, és megvizsgáltuk a glomeruláris festést IgG-re, megfelelődinre és FH/FHR-re. Reprezentatív képek láthatók. Az anti-P injekció jelentősen csökkentette a propertydin (1. sor, 2. oszlop), de az FH/FHR (változatlan marad) vagy az IgG (hiányzik) festődést nem. Az anti-P-FH{20}}órákkal az IgG-kontroll utáni beadása anti-IgG, anti-FH/FHR és anti-P antitestekkel szemcsés festődést eredményezett, amint az anti-P-FH injekció beadása után látható. 1-5 egyedül (lásd 3b. ábra). Ez a szemcsés festődés csökkent, amikor az anti-P-FH1-5 injekciót megelőzte az anti-P injekció, amely kimeríti mind a keringést (lásd 1h. ábra), mind a glomerulárist (lásd a 3b. ábrát). A glomeruláris festődés anti-IgG-vel csak az anti-P-FH-t1-5 injektált egereknél volt nyilvánvaló (3. sor, 3. és 4. oszlop), és szignifikánsan alacsonyabb volt azokban az egerekben, amelyek anti-P-FH-t kaptak1-5 megelőzi az anti-P. Arra a következtetésre jutottunk, hogy az anti-P-FH1-5 lerakódása a Cfh–/– egerek glomerulusaiban részben a propertydintől függ. A vízszintes oszlopok a medián értékeket, a whiskerek pedig az interkvartilis tartományt jelölik. A P-értéket a Mann-Whitney tesztből származtattuk. Rúd ¼ 100 mm.
IRODALOM
1.FakhouriF, Frémeaux-Bacchi V, Noöl LH, et al C glomerulopathy∶ anew dassification. Nat Rev Nephrol.20106:494-499.
2 SmithRH.AppeG8.BlomAMet aLC3gkomeripathia – a ritka komplement-vezérelt valódi betegség megértése. Nat ReyNephrol.201915129-143
3. Pickering MC, Cook HT. Transzlációs mini áttekintés sorozat a H komplement faktorról: H komplement faktorral kapcsolatos vesebetegségek újszerű betekintések emberektől és állatoktól. Cin Exp Immunol.2008;151:210-230.
4. Daha MR Fearon DT Austen KF, C3nechritic faktor (C3NeF)∶a folyadékfázis és a sejthez kötött alternatív útvonal konvertáz stabilizálása. J Immunol 1976;116:1-7.
5. Mollnes TE, Ng YC, Peters DK, egy nefritikus faktor hatása a C3-ra és a komplement terminális útvonalára in vivo és in vitro. Oin Exp Immunol. 1986;65:73-79.
6. Nq YC, Peters DK. G3 nefritikus faktor (C3NeF): az alternatív útvonal C3 konvertáz sejthez kötött és folyadékfázisú stabilizálásának disszociációja. Cn Exp Imunol.19865:450-457.
7. Pickering MC, Cook HT, Warren J és munkatársai Az ellenőrizetlen C3 aktiváció membranoproliferatív glomerulonephritist okoz H komplement faktor hiányos egerekben. Nat Genert.2002:31;424-428.
8. Lesher AM, Zhou L, Kimura Y és mtsai. A H-faktor mutációja és a megfelelődin-hiány kombinációja súlyos C3 glomerulonephritist okoz. J Am Soc Nephrol. 2013;24:53–65.
9. Ruseva MM, Veron KA, Lesher AM et al. A megfelelődin elvesztése súlyosbítja a H faktor hiányából eredő C3 glomerulopathiát. J Am Soc Nephrol. 2013;24:43-52.
10. Paixao-Cavalcante D, Hanson S, Botto M és mtsai. A H faktor elősegíti a GBM-hez kötött iC3b kiürülését azáltal, hogy szabályozza a C3 aktiválását a folyadékfázisban. Mol Immunol.2009;46:1942-1950.
11Fakhouri F, de Jorge EG. Brune F és munkatársai A humán komplement H-faktorral történő kezelés gyorsan visszafordítja a vese komplement lerakódását H-faktor-hiányos egerekben. Vese Int.2010:78:279-286.
12. Michelfelder S, Parsons J, Bohlender Ll és munkatársai Moss által termelt, glikozilációra optimalizált humán H faktor komplementrendellenességek terápiás alkalmazására. JAm Soc Nephrol.201728:1462-1474.
13. Nichols EM, Barbour TD, Pappworth Y és munkatársai Egy kiterjesztett mini-komplement H-faktor molekula javítja a kísérleti C3 glomerulopathiát. Kidney Int. 201588:1314-1322.
14. Ruseva MM, Peng T, Laser MA, et al. Célzott komplement gátlás hatékonysága kísérleti C3 glomerulopathiában. J Am Soc Nephrol. 2016;27:405-416.
15. Yang Y, Denton H, Davies OR és munkatársai Egy szerkesztett komplement H faktor konstrukció C3 glomerulopathia kezelésére. J Am Soc Nephrol. 2018;29:1649-1661.
16. Schulze M, Pruchno CJ, Burns M és mtsai. A glomeruláris C3-klokalizáció folyamatos immunlerakódás-képződést és komplement aktivációt jelez kísérleti glomerulonephritisben. Am J PatholL. 1993:142179-187.
17. Athanasiou Y, Voskarides K Gale DP és munkatársai CFHRS mutációkkal összefüggő családi C3 glomerulopathia 91 beteg klinikai jellemzői 16 törzskönyvben. CTn JAm Soc Nephrol.20116:1436-1446.
18. Kaneko Y, Nimmer动hn F, Madaio MP, et al. A nephrotoxikus nephritis patológiáját és védelmét a specifikus Fc receptorok szelektív bevonása határozza meg. J Exp Med.2006;203:789-797.
19. Sheerin NS, Springall T, Carroll MC és mtsai. Antiglomeruláris alapmembrán elleni védelem (GBM-mediált nephritis C3-és C4-hiányos egerekben. C Exp Immunol. 1997;110:403-409.
20. Cheng ZZ Hellwae J, Seeberger H et al. Egér és humán komplement faktor felületfelismerési és C3b-kötési tulajdonságainak összehasonlítása H.Mol Immunol.2006;43.972-979.
21dp ikra EG. Macor P.Paixao-Caakante D. et al A tipikus hemolitikus urémiás szindróma kialakulása a C5 komplementtől függ.J Am Soc Nephrol.2011;22:137-145.
22.Pdkering MC, de Jorge EG.Martinez-Barricarte Ry és munkatársai Spontán hemolitikus urémiás szindróma, amelyet a H komplement faktor vált ki, felületfelismerő domének hiányában. J Exp Med.2007;204:1249-1256.
23Herbert AP. Mike E, Chen ZAet al. Komplementelkerülés a befogott H faktor fokozásával: következmények az önfelületek komplementtől való védelmére.J Immunol. 2015;195:4986-4998.
24. Goicoechea de Jorge E Caesar JJ, Malik TH, et al. A komplement H-faktorral rokon fehérjék dimerizációja modulálja a komplement aktivációt. Proc Natl Acad Sci US A.2013;110:4685-4690.
25. Schmidt CQ, Bai H Lin Z és mtsai. Egyedülálló hármas célzási tulajdonságokkal rendelkező minimalizált immuninhibitor racionális tervezése. J Immunol. 2013;190:5712-5721.
26. Wilson HR, Medjera-Thomas NR, Gilmore AC, et al. A glomeruláris membrán-támadás komplex nem megbízható markere a folyamatos C5 aktivációnak lupus nephritisben. Kidney Int. 2019.{4}}.
27. Antonioli AH White J, Crawford F, et al. A komplement alternatív útvonalának modulálása rágcsáló H-faktorral rokon fehérjék által. J Immunol. 2018;200:316-326.
28. Cserhalmi M, CsincsiALMezei Z, et al. Az egéreredetű H-faktorral rokon FHR-B fehérje elősegíti a komplement aktiválását. Front Immunol.20178:1145.
29. Medjeral-Thomas NR, Moffett H, Lomax-Browne HJ és munkatársai A glomeruláris komplement faktor H-val kapcsolatos protein 5 (FHR5) nagymértékben elterjedt a C3 glomerulopathiában, és a vesekárosodáshoz kapcsolódik Kdney Int Ren. 2019;4:1387-1400.
30. Miwa T., Sato S., Gullipalli D. és munkatársai. Az alternatív útvonal és az anafilatoxin receptorok blokkolása javítja a vese ischaemia-reperfúziós károsodását a bomlást gyorsító faktor és a CD59 kettős kiütéses egerekben. J Immunol. 2013;190:3552-3559.
31. Corillo F, Bravo Garcia-Morato M, Nozal P és munkatársai A szérum megfelelődin fogyasztása a C5 konvertáz diszreguláció biomarkereként C3 glomerulopathiában. Clin Exp Immunol.2016;184:118-125.8. Lesher AM, Zhou L Kimura Y és munkatársai. A H-faktor mutáció és a megfelelődin-hiány kombinációja súlyos C3-as glomerulonephritist okoz.JAm Soc Nephrol.2013;2453-65.
32. zhang Y, Nester OM Martin B.et al A C3 glomerulopathia komplement biomarker profiljának meghatározása. Clin J Am Soc Nephvol.20149:186-1882.
