Betegségmodellezés veseorganoidokkal
Sep 01, 2023
Absztrakt:Vesebetegségekgyakran hiányoznak az optimális kezelések, ami évente milliók halálát okozza. Így megfelelő modellrendszerek kidolgozása a tanulmányozáshozemberi vesebetegségrendkívül fontos. A legígéretesebb humán vesemodellek közé tartoznak az organoidok vagy kis, szervre emlékeztető szöveti csoportok, amelyek ember által indukált pluripotens őssejtekből (hiPSC) származnak. Ezek azonban inkább az első trimeszterhez hasonlítanakmagzati vesemint egy felnőtt vese. Ezért új stratégiákra van szükség érettségük előmozdításához. Nagy lehetőségek rejlenek bennük a betegség modellezésében és végső soron a kisegítő terápiában, ha elérik az érettségetfelnőtt vese. Ebben az áttekintésben a vese organoidok jelenlegi állapotát tárgyaljuk az emberi veséhez való hasonlóságuk és az eddigi betegségek modellezési rendszerként való felhasználása szempontjából. Ezután megvitatjuk a lehetséges előrelépési utakata vese érettségea felnőtt veséhez illeszkedő organoidok a pontosabb emberi betegségek modellezése érdekében.
Kulcsszavak: organoidok;vese; fejlesztés; metanephros; ureterikus; csatorna; Forgács; nefrológia; betegség-modellezés

KATTINTSON IDE, HA SZEREZZEN CISTANCHE-T CKD-KEZELÉSEKRE
1. Bemutatkozás
Egészen a közelmúltig az emberi betegségeket a következő két módon modellezték: állatokkal vagy kétdimenziós sejtkultúrával. Az állatmodellek lehetővé teszik a betegségek lefolyásának és a gyógyszerfejlesztésnek a tanulmányozását egész szervezetekben, de nem veszik figyelembe az emberi genetikai és anatómiai felépítést. Másrészt az emberi sejtkultúra lehetővé teszi a tudósok számára, hogy tanulmányozzák az emberre jellemző betegségek mechanizmusait és értékeljék a kezeléseket nagy és precíz molekuláris mélységben. A sejtkultúra azonban nem foglalja össze egy szerv összetett háromdimenziós szerkezetét és fiziológiáját.
Az emberi organoidok az emberi szervek leegyszerűsített változatai, valósághű háromdimenziós mikroanatómiával és szervszintű funkciókkal (pl. könnytermelés a lakteális organoidokban és szőrnövekedés a bőrorganoidokban) [1,2]. Önszerveződési folyamatok révén in vitro szövetsejtekből vagy pluripotens őssejtekből származnak. A Takahashi és Yamanaka által 2008-ban feltalált indukált pluripotens őssejtek (iPSC) a legnépszerűbb sejtek az organoidképzésben [3]. Ennek oka az iPSC-k számos lenyűgöző előnye. Először is, korlátlan megújuló sejtforrást biztosítanak, és többféle sejttípusra képesek differenciálódni. Ennél is fontosabb, hogy a betegek mögöttes genetikai összetételét képviselik. Így a betegektől származó humán iPSC-k (hiPSC-k) felhasználhatók a betegségek organoidokon keresztül történő egyéni szintű tanulmányozására, lehetővé téve a személyre szabott orvoslás fejlődését. A mai napig különféle emberi szervek, például a szív és az agy organoid modelljeit használták a betegségek tanulmányozására. Ebben az áttekintésben a vese organoidokra fogunk összpontosítani, és megvitatjuk, hogyan használhatók fel az emberi vese és a kapcsolódó betegségek modellezésére, a gyógyszertoxicitás szűrésére, és esetleg a veseműködés kiegészítésére.

A vesebetegség a világ népességének 10%-át érinti [4]. Annak ellenére, hogy azonosították a vesebetegség számos formájának genetikai okát, nem állnak rendelkezésre optimális terápiák ezek kezelésére. Ez a szerencsétlen helyzet az emberi vesebetegséget célzott terápiás fejlesztés érdekében összefoglaló in vitro modellrendszerek hiányát tükrözi. A veseorganoidok emberi alapú, személyre szabható, 3-D kutatási platformot kínálnak a genetikai vesebetegségek, vesekárosodás és gyógyszertoxicitás vizsgálatára. Amellett, hogy modellező rendszerként szolgálhat, egy veseorganoid magában hordozza a transzplantációs gyógyászat előmozdításának lehetőségét. Így ahhoz, hogy mindkét területen a lehető legjobban kiaknázhassuk, a veseorganoidnak hasonlítania kell a felnőtt emberi vese szerkezetére és működésére. Itt áttekintjük a pluripotens sejtből származó emberi veseorganoid jelenlegi állapotát, lehetséges felhasználásait és a fejlesztésre szoruló területeket.
2. Az emberi vese kontra vese organoidok
A HiPSC-k proxyként szolgálnak az embrionális PSC-k számára. Így a hiPSC-kből veseorganoid kialakítása az emberi embrionális vesefejlődés replikációját vonja maga után. Az alábbiakban megvizsgáljuk, hogyan fejlődik ki a vese organoidja, és összehasonlítjuk az emberi vesével.
2.1. Az emberi vese fejlődése
A vért három különböző fázisban szűrik az embrionális fejlődés során. Az első fázisban a pronephros nevű szerkezet fejlődik ki a 4-hetes emberi embrióban, és körülbelül az 5. hétig dolgozza fel a vért a nyaki régióban [5]. Ezután a mesonephros az embrió mellkasi részén képződik, és megszűri a vért az embrionális fejlődés 5. hetétől körülbelül a 10. hétig. Míg a mesonephros a vért szűri, a végső szűrőrendszer, amely végül afelnőtt vese, kialakulni kezd (1. ábra). A következő két részből áll: a metanephric mesenchyma és az ureter bimbó. A metanephric mesenchyma a nefron minden részét képezi, kivéve a gyűjtőcsatornát, míg az ureterbimbó a gyűjtőcsatornát. Ezek a struktúrák egy kölcsönös indukciós cikluson mennek keresztül, amelyben a metanephric mesenchyma és az ureter bimbója serkenti egymás növekedését, és összeolvadnak, létrehozva a metanephros nevű struktúrát. Az újonnan képződött metanephroi a csípőágaktól a kismedencei régióig szűri a vért. Ugyanakkor az ureterbimbó kettéágazik és tovább ágazik, és sok gyűjtőcsatornát képez a vesén belül [6,7]. Ezt követően ezek az összeolvadt metanefrikus struktúrák felemelkednek az embrió hasi régiójába, ahogy az fejlődik, és vérellátást hoz létre a primitív aortából. Ezeket a folyamatokat az 1. ábra foglalja össze. Fontos megjegyezni, hogy a metanephric mesenchyma és az ureter bimbósejtek primitívek, és így fenntartják a multipotens potenciált, míg a felnőttkori differenciált vesesejtek saját származásukhoz kötődnek [8].
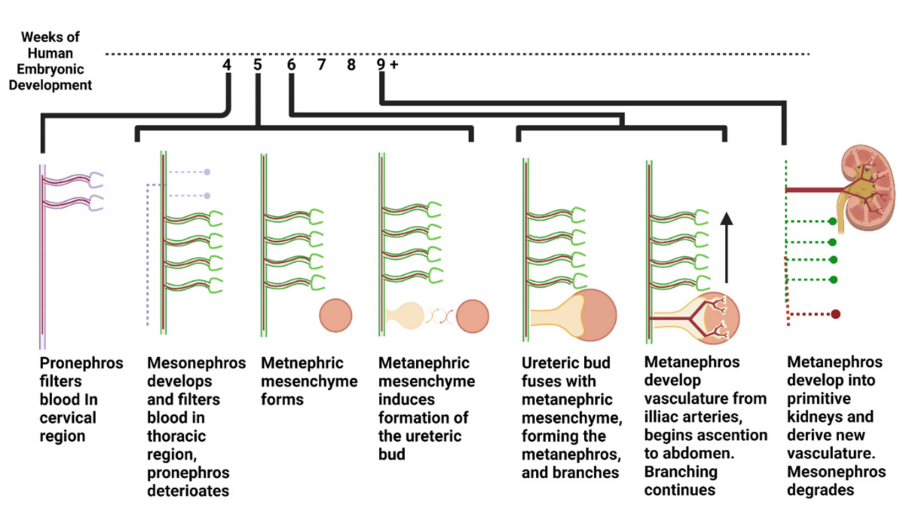
1. ábra: Az emberi húgyúti rendszer fejlődése a 4. héttől a 9. hétig az anyaméhben.
2.2. Protokollok a vese organoidok előállításához
A vese organoidok szöveti eredetű differenciált sejtekből vagy pluripotens őssejtekből képződhetnek. Ahhoz, hogy szöveti eredetű sejtekből veseorganoidot hozzunk létre, a differenciált felnőtt sejteket háromdimenziós térben ex vivo rendezhetjük el, hogy utánozzuk az emberi szervek felépítését [9]. A szövetből származó differenciált sejtek organoid protokolljait máshol tárgyalják. Ebben az áttekintésben az őssejtből származó veseorganoidokra fogunk összpontosítani. E rendszerek létrehozásához a tudósok pluripotens őssejteket tenyészthetnek vese-specifikus endogén morfogének és extracelluláris komponensek jelenlétében. Az őssejtek ezután veseszerű struktúrákká alakulhatnak, utánozva az embrionális vesefejlődést. A szervek, például a bél, a felnőtt szövetben endogén őssejt-populációkat tartalmaznak, amelyekkel a tudósok organoidokat hozhatnak létre [10]. Mivel azonban nincs egyértelmű bizonyíték arra vonatkozóan, hogy egy felnőtt emberi vese tartalmazna őssejtrést, az őssejtből származó veseorganoidokat pluripotens őssejtekből (akár embrionális, akár hiPSC-ből) kell előállítani [11].

Az őssejtekből származó vese organoidok a következő két kategóriába sorolhatók: nephron progenitor (NP) organoidok és ureter bimbó (UB) organoidok. Mindkét típusú organoid jól bevált betegségmodell. Az NP organoidok a metanefris mesenchymához hasonlítanak, amely multipotens NP sejteket tartalmaz. Valójában egyetlen metanefris mesenchymalis sejt a nefron összes hámsejtjét eredményezheti, kivéve a gyűjtőcsatornát [8]. A hiPSC-eredetű NP-organoidok előállításának módszerei közé tartozik a 2D tenyésztés, majd ezt követő aggregációval egy porózus transzwell lemezen (pl. Takasato és mtsai (2016), Morizane és mtsai (2015)) vagy a 3D tenyésztést hidrogélben (pl. Freedman et al. (2015)) [12–14]. Ezek az organoidok glomeruláris és tubuláris struktúrákat fejlesztenek ki. A Takasato és Morizane által a két legnépszerűbb NP protokollból származó NP organoidokat Wu és munkatársai egy kiterjedt omikai elemzésben hasonlították össze. (2018) [15]. Azt találták, hogy míg a Takasato protokoll körülbelül 11% podocitaszerű sejtet és 21% off-target sejtet termel organoidonként, a Morizan protokoll körülbelül 28,5% podocitaszerű sejtet és 14,3% off-target sejtet [15]. Úgy tűnik, hogy a Takasato-féle organoidok is kis mennyiségű UB-szerű régiót fejlesztenek, de túlnyomórészt a metanefris mesenchymát imitálják, így NP organoidok közé sorolják őket [12]. Továbbá Morizane és mtsai. (2015) és Takasato et al. (2016) protokollokból hiányzik az extracelluláris hidrogél környezet, amely jelen van Freedman és munkatársai (2015) munkájában [14]. Garreta et al. (2019) azzal érvelnek, hogy a hidrogél jelenléte az organoidok képződésében javítja a vese szerkezetének kialakulását, és fokozza a korai IM markerek, a hátsó IM markerek és az elülső IM markerek termelődését [16].
Ellentétben az NP organoidokkal, az UB organoidok az ureterbimbót imitálják, amely a gyűjtőcsatorna rendszert eredményezi. Az UB-organoidok előállításának módszereit újabban fejlesztették ki, és magukban foglalják az embriótest tenyésztését és az azt követő aggregációt alacsony tapadású kutakba [17]. Ezek az organoidok csőszerű és gyűjtőcsatorna szerkezetűek. Végül az NP és az UB organoidokat is kombinálták, hogy magasabb rendű társkultúra struktúrákat hozzanak létre a felnőtt ember összefoglalására.vese fenotípusok[17]. A legnépszerűbb protokollok avese organoidképződését az alábbi 2. ábra foglalja össze [12–14,17–19].

2. ábra: A legnépszerűbb szervesanyag-képződési protokollok összefoglalása
2.3. Hogyan halmozódnak fel: Vese organoidok vs. emberi vesék
A fent ismertetett protokollok elsősorban a hiPSC-k organoidokká történő önszerveződését foglalják magukban. Utánozzák a magzati állapotokat, hogy a hiPSC-ket vese-specifikus vonalakká differenciálják, és vese-specifikus struktúrákat alakítsanak ki. Az első magzati állapot, amelyet replikálnak, a primitív csíkjelzés. A primitív csík az embrió egy része, amely a három csíraréteg szétválása előtt fejlődik ki. A legtöbb protokoll ezt a WNT jelző agonista CHIR használatával teszi. Ezután az NP-vonal származtatásához a posterior-intermediate mezodermát (PIM), az UB-vonalhoz pedig az anterior-intermediate mezodermát (AIM) kell indukálni [17]. Érdekes módon Takasato et al. (2015) azt találták, hogy minél hosszabb ideig tart a CHIR-kezelés, annál inkább fejlődött ki a posterior-szerű mezoderma, míg minél rövidebb a periódus, annál inkább fejlődött ki az anterior-szerű mezoderma [20]. Így a megnövekedett WNT jelátviteli időtartam több glomeruláris és proximális struktúra kialakulásához, a csökkent WNT jelátviteli időtartam pedig több disztális struktúra kialakulásához vezet.
Az NP protokoll befejezésekor glomeruláris és tubuláris régiókkal rendelkező organoidok fejlődnek ki. Azonban éretlenek. Tanulmányok kimutatták, hogy a hiPSC-eredetű veseorganoidok az első trimeszterben lévő magzatot utánozzák [20]. Az egyik legkiterjedtebb elemzést ebben a témában Subramanian et al. (2019), aki az RNS-seq segítségével hasonlította össze a vese organoidokat a 8-hetes, 17-hetes és a felnőtt emberi vesékkel. Arra a következtetésre jutottak, hogy a vese organoidjai jobban hasonlítanak az emberi vesékhez a magzat 8. és 17. hetében, mint a felnőtt vesékben [21]. Ezenkívül a vese organoidjai primitív multipotens markerek, például SIX{10}} festődést mutatnak az egész vesében, míg a felnőttkori differenciált emberi vese nem expresszál ilyen markereket [22]. Ezért ahhoz, hogy a veseorganoidot a felnőtt emberi vese proxyjaként használhassuk a betegségek tanulmányozására, előre kell haladnia a terhességi korban.
A vese organoidjai nemcsak jobban utánozhatják a korai metanephrost, mint a megfelelő felnőtt emberi vese, de még jobban is hasonlíthatnak a mesonephrosra, mint a metanephrosra, ha a morfogén koncentrációját nem megfelelően szabályozzák [23]. Ezekkel az aggályokkal foglalkozva Tsujimoto et al. (2020) a hiPSC in vitro differenciálódását vizsgálta mezonefrás NP-k, metanephric NP-k és UB-sejtekké [24]. Ez a tanulmány több olyan tényezőt azonosított, amelyek megkülönböztetik ezt a három származást, és így alkalmazhatók e három különálló rendszer jövőbeli tanulmányozására [24]. Az organoidok érésének további kulcsfontosságú előrelépései közé tartozik az NP-UB kölcsönhatások és a vaszkularizáció. A legfigyelemreméltóbb tanulmányok közül néhányat Taguchi és Nishinakamura (2017), valamint Tsujimoto et al. (2020) [17,24]. Ezek a vizsgálatok MM-UB együtt tenyésztett organoidokat hoztak létre, és egerekbe ültették át őket, ahol vaszkularizálták őket. Ezeknek a metanefrikus magasabb rendű struktúráknak a létrehozása jelentősen javította az őssejt-eredetű veseszerkezet hasonlóságát a tényleges emberi vesékhez. Azonban még ezek a fejlett rendszerek sem voltak képesek összefoglalni a kiterjedtebb UB elágazást, amely a második és az utolsó trimeszterben in vivo történik [24]. Ezek az eredmények alátámasztják az érett endogén vesefunkciók és kölcsönhatások megismétlésének szükségességét, amelyek a jelenlegi organoidokból hiányoznak, mint például a folyadékáramlás.
3. Veseorganoidok mint modellrendszerek
A vese organoidjainak hasonlósága az emberi vesékhez teszi őket alkalmassá betegségek modellezésére és gyógyszerszűrésre. Egy hónapnál rövidebb idő alatt készülhetnek el, személyre szabva, és tömegesen gyárthatók [12–14,17–19]. Ezenkívül in vitro tenyészthetők, vagy egerekbe, patkányokba vagy csirke tojásokba átültethetők, hogy teljes in vivo modelleket hozzanak létre. Az alábbiakban megvizsgáljuk a veseorganoidokkal végezhető elemzéseket, valamint a veseorganoidok jelenlegi és jövőbeni felhasználását az orvosbiológiai kutatásban.
3.1. Vese organoid elemzése
3.1.1. In vitro vizsgálatok
Különféle fiziológiai, molekuláris és funkcionális vizsgálatokat lehet végezni a veseorganoidokon. Ami a molekuláris vizsgálatokat illeti, különböző transzkriptomikai elemzéseket végeztek sikeresen veseorganoidokban [25]. Például Takasato et al. (2015) RNS-t vontak ki organoidokból, és RNS-szekvenálást és qRTPCR-elemzést végeztek [20].
Mások, mint például Wu et al. (2018) magizolálást és snRNS szekvenálást végeztek a DropSeg scRNS szekvenálás mellett veseorganoidokban. Az RNS-szinteken kívül különféle fehérjeszinteket is számszerűsítettek és összehasonlítottak a vese organoid lizátumából immunblot segítségével (pl. Cruz és mtsai, 2017; Morais és mtsai, 2022) [26,27]. Ezenkívül rutinszerűen végeztek immuncitokémiai elemzést vese organoidokban, hogy megvizsgálják a specifikus nefronstruktúrákat. Ezt gyakran egész organoid festésként hajtják végre; alternatív módon szövetmetszeteket is használnak a szondázáshoz (pl. Takasato és mtsai, 2015; Cruz és mtsai, 2017) (20, 26). Ezek a vizsgálatok feltárták, hogy a vese organoidjai glomerulusokat, proximális tubulusokat, disztális tubulusokat, bazális membránokat és gyűjtőcsatorna elrendezése (20, 27]). Az alábbi 3. ábra példát mutat be paraffinba ágyazott és metszett emberi vese organoidokra, amelyeket Takasato és munkatársai (2016) protokolljával hoztak létre. tubulus marker fehérjék, és folyamatos glomeruláristól distalis tubulus nephronikus struktúrákat mutatnak. A struktúrák mellett a vese organoidjainak is van érrendszere, azonban ez korlátozott, gyorsan visszafejlődik, és nem úgy szerveződik, mint egy tipikus vesében (28]).
Több funkcionális vizsgálat is elvégezhető veseorganoidokban. Például amint azt Freedman és mtsai. (2022) szerint a vese organoidokat pulse-chase vizsgálatnak vethetik alá, ahol különféle flfluoreszcens molekulákat adhatnak a tápközeghez, mielőtt új fluoreszcens közeggel helyettesítenék [29]. Ezután az organoidokat elemezni lehet e molekulák felvételére, és a kapott információk felhasználhatók a felhalmozódásra, duzzadásra, szűrésre, endokrinre vagy sérülésre vonatkozó információk megállapítására [29]. Az organoid platformokon végzett vizsgálat egyik problémája azonban az, hogy a molekulákat kívülről is be lehet juttatni a zárt csőszerű struktúrákba, nem pedig az apikális felületen keresztül, ahogyan az in vivo történne. Ennélfogva a flfluoreszcens molekulák felszívódhatnak a külső bazolaterális membránról, mivel nincs mód annak szabályozására, hogy ezek a molekulák hová kerüljenek, ha nagymértékben bekerülnek a közegbe. Ezenkívül a molekulák transzportja korlátozható az organoidokon belüli diffúzióval, ami eltérő felhalmozódási tendenciákat hozhat létre ugyanazon organoidon belül.
Ezenkívül a vese helyreállítása organoid platformokon is értékelhető, így betekintést nyerhetünk a vesekárosodás visszafordítási mechanizmusaiba és a genetikai alapokba, amelyek hajlamosíthatják a betegeket vesebetegségre. Például olyan tanulmányok, mint Gupta et al. (2022) olyan génpályákat vizsgáltak, amelyek a ciszplatinnak, a vesekárosodás molekulájának egyszeri vagy többszöri expozíciója esetén felfelé alakultak vese organoid platformokon [30]. Végül a cisztaképződést organoidokban is elemezhetjük a policisztás vesebetegség (PKD) vizsgálata céljából a cAMP aktiváción keresztül [26]. A ciszták ezután mérhetők, számszerűsíthetők, és az emberi vese ciszták proxykájaként kezelhetők.

3.1.2. In vivo elemzés
Az in vitro veseorganoidok modellrendszerként való alkalmazásának jelentős hátránya, hogy nincs kölcsönhatásuk a szervezet többi részével. Számos olyan körülmény, amely a test távoli részeit érinti, hatással lehet a vesére, és fordítva. Például a vérnyomás változásai drasztikusan megváltoztathatják a glomeruláris nyomást, amit a vese szabályozhat. Az in vitro organoid rendszerek azonban nem veszik figyelembe ezeket a szisztémás kölcsönhatásokat. Így olyan transzplantációs megközelítéseket fedeztek fel, amelyek emberi eredetű veseorganoidokat tartalmaznak egerekben, patkányokban és csirke tojásokban. Az ilyen vizsgálatokban az emberi és állati szöveteket a humán nukleáris antigén immunfestéssel vagy az Y-kromoszóma leolvasásával a kombinált genom-referenciához igazítják [21]. Ezenkívül az organoidok átültethetők állványon (pl. selyemen) keresztül, hogy magasabb szintű szerkezeti integritást biztosítsanak [31]. Ez a megközelítés megkönnyítheti az organoid-szövet-specifikus elemzéseket a transzplantáció után.
A veseorganoidok átültetésének egyik fő előnye, hogy lehetővé teszi az organoidok érrendszerét, érlelését és még a vizelet szűrését is. Van den Berg et al. (2018) kimutatták, hogy egerekbe történő szubkapszuláris vesetranszplantációt követően a vese organoid glomerulusai és tubulusai jelentősen megérnek [32]. Egy másik tanulmányban Subramanian et al. (2019) kimutatták, hogy a hiPSC-eredetű organoidok egerekbe történő transzplantációja a tubulusok proximális és disztális érésének növekedéséhez, valamint az organoidon belüli nem célsejtpopulációk jelenlétének csökkenéséhez vezet [21]. Ennél is fontosabb, hogy a transzplantáció után a veseorganoidok képesek ellátni a vese végső funkcióját, vérszűrőt. Az egerekben végzett szubkután transzplantációt követően a vese organoidjai vizeletszűrő struktúrákat hoztak létre, amit a FITC-vel jelölt dextrán átvitele bizonyít [33]. Így a transzplantáció nemcsak egy veseorganoid mutációjának hatásainak vizsgálatát teszi lehetővé in vivo, hanem javítja az organoid emberi veséhez való hasonlóságát, és valamelyest funkcionális rendszerré teszi.
Míg immunhiányos egereket gyakran használnak hiPSC veseorganoid transzplantációra, más gazdákat, például csirke chorioallantoic membránokat (CAM) is alkalmaztak. A CAM természetesen immunhiányos, és elősegíti az organoid vaszkularizációját [16]. Azonban hiányoznak belőle a tipikus emlős szervrendszerek, így a vese organoidjai elszakadnak a többi rendszertől, ellentétben az egerekkel. A gazdaszervezettel kapcsolatos kudarcok ellenére az emberből származó veseorganoidokkal végzett kiméragenerálás lehetővé teszi az emberi vesebetegség kiterjedt in vivo vizsgálatát egy rendkívül hatásos platformon.
3.2. Eddig végzett betegségmodellező vizsgálatok
3.2.1. Veseorganoidok mint genetikai betegségek modelljei
A vese organoidokat a tubuláris és glomeruláris genetikai vesebetegségek tanulmányozására használták [26, 34, 35]. Emberben a legjelentősebb tubuláris betegségek közé tartozik a gyermekkori policisztás vesebetegség (PKD), amely a fibrocisztás gén (PKHD1) autoszomális recesszív mutációiból származik, és a felnőttkori PKD, amely a policisztin autoszomális domináns mutációiból ered-1 és -2 gének [36–38]. Ezeket a mutációkat mesterségesen be lehet vinni a hiPSC-kbe génszerkesztő technológiákkal, például a CRISPR-Cas 9 rendszerrel. A szerkesztett hiPSC-k ezt követően PKD-modellező humán vese organoidokká növeszthetők, és fehérjefestéssel és RNS-profilozással elemezhetők. Például Freedman et al. (2015) és Cruz et al. (2017) a CRISPR/Cas9 rendszer segítségével kiütötték a policisztin géneket a hiPSC vonalakból, majd olyan organoidokat hoztak létre, amelyek utánozzák a beteg betegekben in vivo talált cisztás fenotípust [14,26]. Ezek a vizsgálatok azt mutatják, hogy a vese organoidok könnyen megfigyelhető, betegségreleváns platformként használhatók a PKD tanulmányozására. Ezenkívül a betegektől származó sejtvonalakból készült organoidok betekintést engednek a beteg-specifikus mutációkba és a betegség kialakulásának valószínűségébe. Például Low és mtsai. (2019) PKHD1 mutációval rendelkező betegekből származó veseorganoidokat fejlesztettek ki, és vad típusú organoidokkal hasonlították össze [39]. A beteg organoidok szignifikánsan több cisztaképződést mutattak, így bizonyítva a veseorganoidok azon képességét, hogy a genotípus alapján előre jelezzék a betegség manifesztációját [39]. Egy másik tanulmányban Hernandez és mtsai. (2021) olyan betegektől származtatták a hiPSC-ket, akiknél a gumós sclerosis komplex-2 gén mutációi mutatkoztak, ami hajlamossá teszi a beteget a vese daganat kialakulására [40]. Ezután a CRISPR/Cas9 rendszerrel korrigálták a páciens mutációját. Az ezekből a korrigált izogén mutáns vonalakból származó vese organoidok csökkent cisztaképződést és helyreállított génpályákat mutattak a beteg organoidokhoz képest, bizonyítva ezzel a vese organoidok hasznosságát az izogén szervszerű rendszerekben előforduló specifikus mutációk downstream funkcionális hatásainak tanulmányozásában.
A kutatók betegektől származó organoidokat is használtak, hogy betekintést nyerjenek a glomerulust érintő genetikai betegségekbe. Például Hale és mtsai. (2018) az NPHS1 (nephrin) génre összpontosított, amely mutáció esetén hibás podocita lábfolyamat kialakulását és szivárgó vizeletszűrést indukál, ami vesebetegséghez vezet [34]. Hale et al. (2018) betegektől származó mutáns NPHS1 hiPSC-ket használtak olyan vese organoidok származtatására, amelyek modellezték ezeket a hibás podocita lábfolyamatokat, beleértve a podocita-specifikus fehérjék, a nephrin és a podocin csökkent szintjét [34]. Hasonlóképpen Freedman et al. (2015) kiütötte a PODXL glomeruláris gént a hiPSC-kben, és azt találta, hogy az organoidok hibás podocita-podocita architektúrát mutatnak [14].
A veseorganoidok egyik nagyrészt kiaknázatlan lehetősége az embrionális és magzati rendellenességek modellezési képessége. Jelenleg a kutatók arra törekszenek, hogy a felnőtt emberi vesét a veseorganoiddal modellezzék. Jelenlegi első és második trimeszteri állapotában azonban a veseorganoid felhasználható a fejlődési vesehibák tanulmányozására [41]. A húgyúti rendszer fejlődési rendellenességei, mint például a vese diszplázia, a legelterjedtebb és legsúlyosabb fejlődési rendellenességek közé tartoznak [42]. Mivel ezek közül a betegségek közül sok már 11 hetes korban kimutatható, a veseorganoidok különösen alkalmasak a veleszületett vesekárosodás tanulmányozására. Nemcsak metanefris első és második trimeszterhez hasonló veseorganoidok állnak rendelkezésünkre, hanem primitív mezonefrikus vese sejtvonalaink is (pl. Tsujimoto et al., 2020) az embrionális és magzati rendellenességek tanulmányozására [24]. Mivel kevés rendszer teszi lehetővé a fejlődő emberi vese tanulmányozását és manipulálását, a veseorganoid óriási potenciált tesz lehetővé magzati genetikai, toxikológiai és fejlődési vizsgálatokhoz.
3.2.2. Veseorganoidok mint más betegségek modelljei
A genetikai betegségek mellett a veseorganoidokat az emberi rendszerek vírusfertőzésre, rákra és sérülésekre adott válaszának tanulmányozására is használták. Például Jansen és mtsai. (2021) vese organoid platformot használtak a vírusos SARS-CoV-2 emberi vesére gyakorolt hatásának értékelésére [43]. Ez a csoport felfedezte, hogy a SARS-CoV-2 fertőzés fokozott kollagén-I expresszióhoz vezet az emberi vese organoidjaiban, így mechanikus magyarázatot ad a vesekárosodásra és -fibrózisra, amely gyakran kíséri a hosszan tartó COVID súlyos eseteit-19 [ 43]. A rákkutatással kapcsolatban Hernandez et al. (2021) veseorganoidokat ültettek át immunhiányos patkányokba, hogy ritka, genetikailag befolyásolt vese daganatokat modellezzenek. Itt a betegektől származó organoidokon daganatszerű elváltozások alakultak ki, így összefoglalva a humán vese daganatait [40]. Ezen túlmenően vese organoid alapú daganatmodelleket használtak félig funkcionális, emberi eredetű struktúrákként, valamint teszteltek gyógyszereket és nanorészecskék alapú terápiákat. Végül a közelmúltban végzett vizsgálatok kimutatták, hogy a veseorganoidok felhasználhatók a vesekárosodásra adott válasz tesztelésére. Például Prezpiorski et al. (2022) kimutatták, hogy a vese organoidok az oxidatív károsodás markereit termelik és fokozzák a sérülés markerek expresszióját azáltal, hogy a vese organoidjainak hemin sérülésmolekulát adnak a bioszenzorral együtt [44].
3.2.3. Veseorganoidok a gyógyszerértékelésben
A betegségekbe való betekintés mellett a veseorganoidokat a gyógyszerek szűrésére is alkalmazták. A veseorganoidokat különösen a gyógyszer okozta vesekárosodás (DIKI) tanulmányozására használták, amely az akut vesekárosodás vezető oka [45]. A ciszplatin mellékhatásainak értékelése során Czerniecki et al. (2018) kimutatták, hogy a veseorganoidok nagy áteresztőképességű modellként hasznosak az új gyógyszerek tesztelésében a humán genetika sokféle skálájában [46].
Mások, mint például Wu et al. (2018) magizolálást és snRNS szekvenálást végeztek a DropSeg scRNS szekvenálás mellett veseorganoidokban. Az RNS-szinteken kívül különféle fehérjeszinteket is számszerűsítettek és összehasonlítottak a vese organoid lizátumából immunblot segítségével (pl. Cruz és mtsai, 2017; Morais és mtsai, 2022) [26,27]. Ezenkívül rutinszerűen végeztek immuncitokémiai elemzést vese organoidokban, hogy megvizsgálják a specifikus nefronstruktúrákat. Ezt gyakran egész organoid festésként hajtják végre; alternatív módon szövetmetszeteket is használnak a szondázáshoz (pl. Takasato és mtsai, 2015; Cruz és mtsai, 2017) (20, 26). Ezek a vizsgálatok feltárták, hogy a vese organoidjai glomerulusokat, proximális tubulusokat, disztális tubulusokat, bazális membránokat és gyűjtőcsatorna elrendezése (20, 27]). Az alábbi 3. ábra példát mutat be paraffinba ágyazott és metszett emberi vese organoidokra, amelyeket Takasato és munkatársai (2016) protokolljával hoztak létre. tubulus marker fehérjéket és folyamatos glomeruláristól distalis tubulus nephronikus struktúrákat mutat. A struktúrák mellett a vese organoidjainak is van érrendszere, azonban ez korlátozott, gyorsan visszafejlődik és nem szerveződik úgy, mint egy tipikus vesében (28]).

4. ábra: A veseorganoidok betegségmodellezési módszereinek összefoglalása. A vese organoidok felhasználási módjainak összefoglalása di






