Madin-Darby szarvasmarhavese (MDBK) sejtek in vitro fertőzése Eimeria Acervulina sporozoitákkal: A paraziták sejtinváziójának és replikációjának kvantitatív elemzése valós idejű polimeráz láncreakció (PCR) segítségével
Mar 17, 2022
Absztrakt
A baromfi kokcidiózisa jelentős gazdasági veszteségeket okoz az állattenyésztési ágazatnak. Az Eimeria paraziták felelősek ezért a betegségért. Globális szinten az E. acervulina és az E. tenella a leggyakoribb Eimeria spp. a brojlerek megfertőzése. Az E. tenellát általában fertőzési modellként használják in vivo és in vitro vizsgálatokban. Másrészt az E. acervulinát alig vizsgálták in vitro körülmények között. Az E. tenella fertőzés jól bevált és széles körben használt in vitro modellje a Madin Darby szarvasmarhavesesejtvonal (MDBK); azonban keveset tudunk arról, hogy az MDBK sejtek alkalmasak-e gazdasejtként E. acervulina számára. Az MDBK egyrétegű sejteket két különböző dózissal, 5×104 és 2×105 E. acervulina sporozoitákkal fertőztük meg, és a tenyészeteket a fertőzés után 24 és 96 órával (hpi) értékeltük. Összehasonlításképpen egy azonos fertőzési vizsgálatot végeztünk E. tenella sporozoitákkal. A paraziták szaporodásának felmérése érdekében valós idejű kvantitatív PCR segítségével számszerűsítettük az E. acervulina SCAR marker és az E. tenella ITS-1 gén DNS-másolatok számát. Azt találtuk, hogy az E. acervulina kópiák száma szignifikánsan megnőtt 24 hpi mellett az E. tenellához képest (p<0.05). after="" 96="" hpi,="" e.="" acervulina="" gene="" copies="" were="" considerably="" reduced="" while="" e.="" tenella="" continued="" to="" multiply=""><0.05). our="" results="" show="" that="" mdbk="" monolayers="" could="" be="" used="" for="" in vitro="" research="" aimed="" to="" study="" e.="" acervulina="" sporozoite="" cell="" invasion.="" nevertheless,="" modifications="" of="" in vitro="" cultivation="" appear="" necessary="" to="" allow="" qualitative="" and="" quantitative="" studies="" over="" longer="" periods="" of="" parasite="">
Kulcsszavak:kokcidiózis; Eimeria acervulina; Eimeria tenella; Baromfi; MDBK sejtek; Vese

A CISTANCHE JAVÍTJA A VESE-/VESEBETEGSÉGET
Bevezetés
A kokcidiózis gazdaságilag fontos betegség a baromfiiparban (Blake et al. 2020). A betegséget az Eimeria nemzetségbe tartozó apicomplexan paraziták okozzák. A fertőzés spórás oociszták szájon át történő lenyelésével történik. A gazdaszervezetbe kerülve az oociszták sporozoitákat szabadítanak fel, amelyek behatolnak a bélhámsejtekbe. A gazdasejteken belül a sporozoiták aszexuális és szexuális szaporodási ciklusokon mennek keresztül. Ezáltal oociszták képződnek, és ennek következtében a széklettel ürülnek ki. A fertőzött állatok súlycsökkenést, hasmenést, alacsony tojástermelést okozhatnak, és a betegség bizonyos esetekben végzetes is lehet (López-Osorio et al 2020). Hét Eimeria faj (E. acervulina, E. brunetti, E. maxima, E. mitis, E. necatrix, E. praecox és E. tenella) felelős a madárkokcidiózisért világszerte. Az oociszták morfológiája, patológiája és a betegség súlyossága gyakori megkülönböztető tényezők e fajok között. A hét Eimeria közül az E. acervulina, az E. tenella és az E. maxima a legelterjedtebb a brojlertelepeken (Jordan et al 2018; Moraes et al 2015; Györke et al 2013). A három faj közül az E. tenella magas patogenitású, míg az E. acervulina és az E. maxima mérsékelt patogenitást mutat (López-Osorio et al. 2020). A patogenitásbeli eltérések ellenére a mérsékelten patogén Eimeria spp. mint például az E. acervulina fokozhatja a betegség súlyosságát társfertőzés során (Hiob et al. 2017). Az állatmodellek értékes elemei a fertőzéskutatásnak. A kokcidián parazitákkal végzett in vitro vizsgálatok azonban hozzájárulhatnak a betegség sejtszintű megértéséhez (Marugán-Hernández és mtsai 2020, Bussite és mtsai 2018, Thabet et al. 2017). Ezen túlmenően hasznos eszközök lehetnek a jövőbeli terápiák alapadatainak biztosítására (Thabet et al. 2017; Khalafalla et al. 2011). A nem madár sejtvonalakban való növekedési képességének köszönhetően (Marugán-Hernández és mtsai 2020; Thabet és mtsai 2017) az E. tenellát széles körben alkalmazták modellszervezetként in vitro kutatásokban (Marugán-Hernández et al. 2020). Thabet és mtsai 2019, 2017; Khalafalla és mtsai 2011), és jelentős erőfeszítések irányultak az E. tenella in vitro és in vivo kutatására, beleértve a molekuláris megközelítések, például a valós idejű kvantitatív PCR (RT-qPCR) alkalmazását. (Marugán-Hernández és mtsai 2020; Thabet et al. 2019, 2017; Hiob és mtsai 2017; Raj és mtsai 2013). Más Eimeria fajok, köztük az E. acervulina esetében kevesebb erőfeszítésről számoltak be (Naciri-Bontemps 1976; Itagaki et al. 1974; Strout és mtsai 1965; Hiob és mtsai 2017). A tanulmány célja az E. acervulina sporozoiták in vitro inváziójának és replikációjának értékelése volt MDBK sejt monorétegekben valós idejű kvantitatív PCR segítségével.

A CISTANCHE JAVÍTJA A VESE/VESEDIALÍZIS
Anyagok és metódusok
E. acervulina és E. tenella oociszták átjutása OocisztákAz E. acervulina és az E. tenella törzsét külön passzáltuk egészséges 11-naposcsibékben Eckert és munkatársai által módosított módszer szerint. (1995). A spórás oocisztákat összegyűjtöttük, és további felhasználásig 4%-os kálium-dikromát oldatban tároltuk 4 fokon.Az oociszták tisztítása és excisztációjaMindkét Eimeria faj oocisztáját megtisztítottuk a 4%-os kálium-dikromát oldatból. Ezt követően a sporozoitákat a Rentería-Solís és munkatársai által leírt módosított módszer szerint gerjesztettük és tisztítottuk. (2020).SejttenyésztésMadin-Darby szarvasmarhavese(MDBK) egyrétegű rétegeket (DSMZ, Braunschweig, Németország) használtunk fertőzési modellként. MDBK sejteket oltottunk be (2 × 105 sejt/lyuk) 24-lyukú lemezekre Dulbecco's Modified Eagle's Medium (DMEM) táptalajjal, amelyet 10 százalék borjúmagzati szérummal (FBS), 100 NE penicillinnel, 100 ug/ml sztreptomicinnel és 2,5 ug/ml amfotericinnel, és 37 fokon inkubáltuk 5 százalékos CO2 légkörben, amíg el nem értek a 80 százalékos összefolyást.MDBK sejtek fertőzése Eimeria sporozoitákkalA konfluens MDBK egyrétegű rétegeket E. acervulina sporozoitákkal oltottuk be. Előzetes vizsgálatokat végeztünk annak érdekében, hogy a fertőzési dózist a különböző fertőzési arányok (MOI) alapján (parazita:sejt) válasszam ki: {{0}}.25, 0.5, 1.{101} {9}}, 1.5 és 5.{12}} (Taha et al. nem publikált adatok). A fertőzéshez két külön dózist választottunk ki: 5×104 (MOI: 0,25) vagy 2×105 sporozoitát/lyuk (MOI: 0,5). A fertőzésnek kitett tenyészeteket ezután 2% FBS-t, 100 NE penicillint, 100 ug/ml sztreptomicint és 2,5 ug/ml amfotericint tartalmazó DMEM táptalajban 41 fokon inkubáltuk. Két különböző inkubációs időt alkalmaztak: a fertőzés utáni 24 órával (hpi) és a 96 hpi-vel. Az E. tenella sporozoitákkal azonos fertőzési dózisokat és inkubációs időket határoztunk meg. Minden kísérlet tartalmazott egy negatív kontrollt, amely nem fertőzött MDBK monolayereket (NC-fertőzetlen sejteket) tartalmazott. Minden vizsgálatot három párhuzamosban végeztünk. 24 hpi után a sejteket háromszor mostuk steril PBS-sel (pH 7,2), és új táptalajt adtunk a 96 hpi-s csoporthoz, míg a 24 hpi-s tenyészeteket leállítottuk. A monorétegeket az egyes inkubációs periódusok végén tripszineztük (24 hpi vagy 96 hpi).
DNS kivonás és valós idejű kvantitatív polimeráz láncreakció (RT-qPCR)A tripszinnel kezelt sejtekből a DNS-t DNeasy Blood & Tissue kit (Qiagen, Hilden, Németország) segítségével vontuk ki a gyártó protokollja szerint. RT-qPCR-t végeztünk az E. acervulina szekvenciával jellemzett amplifikált régió (SCAR) marker Ac-R01-1731 és az E. tenella belső átírt 1. spacer riboszomális DNS (ITS-1) gén másolatainak mennyiségi meghatározására. a parazita replikációjának korrelációja. Az RT-qPCR vizsgálatokat Blake és munkatársai által leírt módszerek szerint végeztük. (2008) és Kawahara et al. (2008), illetve némi módosítással. Röviden, egy 20 µl térfogatú reakció 10 µl SYBR Green® mesterkeveréket (Thermo Scientific, Dreieich, Németország), 500 nM forward és reverse primert (1. táblázat), 2 µl DNS templátot és 7 µl nukleázmentes vizet tartalmazott. Minden egyes vizsgálathoz nukleázmentes vizet tartalmazó, nem templát kontrollt (NTC) adtunk. Az RT qPCR reakciókat három párhuzamosban amplifikáltuk, és egy Bio-Rad CFX Connect Real-Time PCR Detection System rendszeren (Bio-Rad, Feldkirchen, Németország) hajtottuk végre. Az RT-qPCR körülmények 95 fokosak voltak 5 percig, majd 40 ciklus 95 fokos 30 másodpercig. A lágyítást 59,8 fokon és 58 fokon 20 másodpercig végeztük az E. acervulina és az E. tenella esetében, majd egy 20 másodperces meghosszabbítási ciklus következett 72 fokon. A disszociációs görbe létrehozásához olvadási görbe programot alkalmaztunk, amely 60 és 95 fok közötti hőmérséklet-tartományt tartalmazott. Végül az E. acervulina és az E. tenella standard görbéit a genomiális DNS sorozathígításával, illetve a klónozott ITS-1 génfragmensek sorozathígításával generáltuk (Thabet et al. 2015 szerint).

Statisztikai analízis
D'Agostino-Pearson and Shapiro–Wilk normality tests were used to determine the normal distribution of data. A two-way ANOVA test was used for comparison of reproduction considering time points, infection doses, and Eimeria species. Differences were considered statistically significant when p>0.05. Az összes statisztikai elemzést GraphPad Prism 9 szoftverrel (San Diego, CA, USA) végeztük.
Eredmények és vita
Az E. acervulina SCAR marker és az E. tenella ITS-1 gén génmásolatait sikeresen amplifikáltuk és RT-qPCR-rel detektáltuk minden reakcióban. 24 hpi-s inkubációs periódus után az 5×104 sporozoita adag alkalmazása után észlelt kópiák száma szignifikánsan magasabb volt (p{5}},0002) az E. acervulina esetében (1,88×105±5,56×104), mint az E. tenella (3,60× 104±5,37× 103 ) esetében (1. ábra). Hasonlóan szignifikánsan magasabb (p=0,0002) kópiaszámot kaptunk E. acervulina (4,82×105±8,50×104 ), mint E. tenella (1,27×105±9,32×103 ) 24 hpi után. 2×105 sporozoiták alkalmazása (1. ábra). Ezzel szemben 96 hpi-vel az 5 × 104 sporozoitával történt fertőzést követően az E. acervulina fertőzött tenyészetekben a kópiaszám szignifikánsan (p=0,0044) alacsonyabb volt (6,96 × 103 ± 3,87 × 103), mint az E. tenella (1,24 × 105 ± 1,01 × 105). Hasonlóképpen, a nagyobb dózisú, 2×105 sporozoitok, amelyeket egyrétegű rétegekkel inkubáltak hosszabb ideig, 96 hpi, szignifikánsan (p{58}},0044) kisebb mennyiségű E. acervulina kópiát (3,35×104±1,53×104) eredményezett összehasonlítás az E. tenellával (4,98× 105±1,28× 105 ) (1. ábra).
Teszteltük az E. acervulina azon képességét, hogy behatoljon az MDBK egyrétegű rétegeibe, és ezt követően 24 és 96 hpi felett szaporodjon. Korábbi kísérletek az E. acervulina tenyészet értékelésére változó eredményekkel történtek. Strout és mtsai. (1965) különböző elsődleges (csirkeembrió) fertőzöttekveseés fibroblasztok) és állandó sejtvonalak (egér fibroblasztok, HeLa sejtek). Strout és mtsai. (1965) minden sejtvonalban felismerhető sejtfertőzésről számoltak be 24 hpi-nél. Érdekes módon egyetlen tesztelt sejtmodellben sem figyeltek meg parazita növekedést 24 hpi-nél hosszabb periódusokban (Strout et al. 1965), ami összhangban van a génszám csökkenésével kapcsolatos megfigyeléseinkkel.
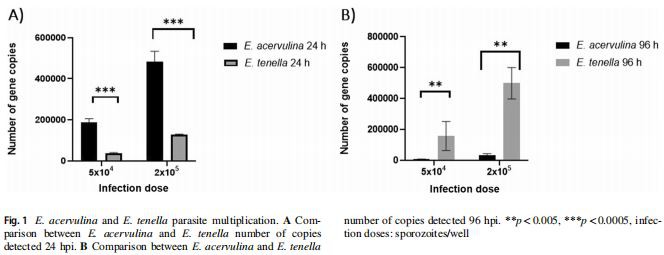
másolatok 96 hpi. Naciri-Bontemps (1976) beszámolt az E. acervulina növekedéséről csirkébenvese93 hpi-ig, és oocisztaképződést figyeltek meg a merozoiták beoltása után. Legjobb tudomásunk szerint azonban ezeket a megállapításokat későbbi publikációk nem erősítették meg. Csak egy cikk jelent meg az E. acervulina sporozoitákkal fertőzött MDBK egyrétegű rétegekről (Talebi 2001). Röviden, a szerző korábban hiperimmun csirke vagy nyúl antiszérummal kezelt MDBK sejteket E. acervulina sporozoitákkal 24 hpi-ig tette ki. A tenyészeteket megfestettük, és az intracelluláris sporozoitákat mikroszkóposan megszámoltuk. Sajnos a tanulmány csak az antiszérum által okozott parazita gátlás százalékos arányát mutatja be (Talebi 2001), így nem lehet könnyen következtetéseket levonni a fertőzés hatékonyságára vonatkozóan ebben a modellben. Tudomásunk szerint további kísérletekről nem számoltak be az MDBK-sejtek E. acervulina fertőzési modelljeként való felhasználására. Strout et al. (1965) 24 hpi-nél figyeltük meg a parazita szaporodási csúcsot, később pedig egy határozott csökkenést, amelyet az alacsony példányszám jellemez 96 hpi-nél. Strout és mtsai. (1965) és Naciri-Bontemps (1976) kvalitatív adatokról számoltak be, amelyek csak mikroszkópos elemzésből származnak. Az RT-qPCR azonban pontosabb és érzékenyebb módszer a paraziták szaporodásának értékelésére. Valójában az RT-qPCR-t manapság általánosan használják kvantitatív értékelésre, és sikeresen bevezették a kokcidiák szaporodásának felmérésére (pl. Marugán-Hernández és mtsai 2020, Rentería Solís et al. 2020, Thabet et al. 2019, Bussiere et al. 2018, Hiob és társai 2017, Thabet és társai 2017, Raj és társai 2013, Khalafalla és társai 2011)
Az elektronmikroszkópia azonban értékes adatokkal szolgálhat az E. acervulina intracelluláris fejlődésének elemzéséhez MDBK sejtekben. Ezért fontolóra kell venni az E. acervulina további in vitro vizsgálatait. Elméletileg a madársejtvonalak előnyösebbek a csirke Eimeria in vitro fertőzési modelljeként, mivel a természetes gazdaszervezetből származnak, és reprezentatívabb betekintést engedhetnek a parazita és a gazdaszervezet közötti kölcsönhatásokba, mint az emlős eredetű sejttenyészetek. A baromfi kokcidiózis kutatására alkalmas csirke sejttenyészetek többsége azonban elsődleges sejtvonal (Bussiere et al. 2018, Strout et al. 1965; Naciri-Bontemps 1976). Az elsődleges sejtek számos korláttal rendelkeznek az állandó tenyészetekhez képest. Az egyik a friss állati szövetek általános igénye a laboratóriumi kísérletek megkezdéséhez, ami összefügghet a szennyeződés kockázatával (Verma et al. 2020). Ezenkívül az elsődleges sejtek megszerzéséhez állatokat kell feláldozni, ami ellentétes az etikai megfontolásokkal. Végül az elsődleges sejtvonalak szabványosítása nehézségekkel hozható összefüggésbe.

A CISTANCHE JAVÍTJA A VESE/VESE FERTŐZÉSÉT
Ezért az immortalizált sejtvonalak használata általános gyakorlat a madárkokcidiák in vitro tenyésztésével foglalkozó legtöbb kutatócsoportban. Általában az emlős eredetű állandó tenyészeteket választják, mivel kereskedelmi forrásokból könnyen beszerezhetők, és olyan eszközöket, mint például antitestek, markerek, publikált protokollok, genomiális szekvenciák stb. állapítanak meg, míg a ritkábban használt csirke sejtvonalak esetében ez nem mindig igaz. . Az MDBK sejtek egy szarvasmarha eredetű állandó vonal, amelyet in vitro modellként használnak számos alkalmazáshoz. Az MDBK sejtek jól megalapozottak az E. tenella in vitro vizsgálatokhoz (Marugán-Hernández és mtsai 2020, Rentería-Solís és mtsai 2020, Thabet és mtsai 2019, Bussiere et al. 2018, Thabet és mtsai 2017, Khalafalla et al. al. 2011). Marugán-Hernández et al. (2020) például átfogó leírást végzett az E. tenella intracelluláris fejlődéséről MDBK sejtekben. Ebben a tanulmányban a szerzők RT-qPCR és reverz transzkriptáz, valós idejű PCR segítségével követték nyomon az E. tenella transzgénikus törzseinek sejtosztódását és fejlődési szakaszát.
Célunk az E. acervulina szaporodásának számszerűsítése volt MDBK sejtekben PCR technológiával. Jelenlegi ismereteink szerint ilyen adatok korábban nem jelentek meg. A morfológiai elemzést kísérletünkben nem vettük figyelembe. Azonban többször is kimutatták (Marugán-Hernández és mtsai 2020, Thabet és mtsai 2017 és Raj és mtsai 2013), hogy a génkópiaszám növekedése valójában a merogónia során bekövetkező szaporodással függ össze. Az ivartalan szaporodás ezen fázisán túli fejlődés meglehetősen valószínűtlen a kísérletünkben megadott feltételek mellett. Megállapítottuk, hogy az E. tenellához képest az E. acervulina sporozoiták behatolnak a sejtbe és gyorsabban szaporodnak az első 24 hpi alatt. A génkópiák száma azonban jelentősen, 96 hpi-vel csökken, ami az E. acervulina parazita szaporodásának dinamikáját mutatja, amely határozottan különbözik az E. tenellaétól. Így valószínűnek tűnik, hogy a különböző Eimeria fajok eltérően viselkednek az in vitro tenyészetben, és az E. tenelláról, mint az egyetlen megalapozott modellszervezetről levont általános következtetéseket óvatosan kell levonni. További időpontok hozzáadása hasznos lehet az in vitro szorzás dinamikájának részletesebb értékeléséhez. További technikák alkalmazhatók annak tisztázására, hogy mi történik ebben az időszakban, és hogy ezekből az eredményekből származhatnak-e a jövőbeli terápiák gyakorlati alkalmazásai.
Ennek ellenére sikeres volt a parazita invázió ebben a sejtvonalban. Ezért az MDBK sejteket tovább lehetne használni fertőzési modellként az E. acervulina sporozoita sejtinvázióhoz. Ezenkívül az RT-qPCR és más érzékeny eszközök használata javasolt. Ennél is fontosabb, hogy ez a sejtvonal támogatja az E. tenella fertőzést is. Ez a két Eimeria faj összehasonlító vizsgálataira fordítható. További részletes kvantitatív és kvalitatív elemzéseket kell végezni annak felmérésére, hogy az MDBK tenyészet alkalmas-e in vitro mátrixként az E. acervulina és más Eimeria csirke fajok fejlődési szakaszaira. támogatás; köszönettel tartozunk M. Fritschének, B. Schneidewindnek és R. Schumachernek (Lipcsei Egyetem Parazitológiai Intézete) állattartóként nyújtott kiváló segítségükért. Köszönet továbbá R. Zhangnak (Southwest Minzu University Állat- és Állatorvostudományi Főiskolája) a laboratóriumi munkák során nyújtott értékes segítségéért. A szerzők köszönetet mondanak továbbá R. Schmäschkének (Lipcsei Egyetem Parazitológiai Intézete) az állatengedélyek elkészítésében végzett értékes munkájáért.

