A vese interkalált sejtjei fagocitizálnak és savanyítják az internalizált uropatogén Escherichia colit
Feb 28, 2022
VeseAz interkalált sejtek részt vesznek a sav-bázis homeosztázisban a vakuoláris ATPáz expresszióján keresztül. Itt hat emberi interkalált sejtaltípusról számolunk be, beleértve az egysejt-transzkriptomiából azonosított hibrid fő interkalált sejteket. A fagoszóma érése olyan biológiai folyamat, amely a biológiai útelemzés rangsorában növekszik az uropatogén Escherichia coli expozíciót követően két interkalált sejtaltípusban. Az egér valós idejű konfokális mikroszkópos megjelenítésevese-Escherichia colit vagy pHrodo Green E. coli BioParticles-t expresszáló zöld fluoreszcens fehérjével perfundált tubulusok azt mutatják, hogy az interkalált sejtek aktívan fagocitizálják a baktériumokat, majd savanyítják a fagolizoszómákat. Ezenkívül az interkalált sejtek fokozott vakuoláris ATPáz-expressziót mutatnak az in vivo kísérleti UTI-t követően. Összességében az interkalált sejtek olyan transzkripciós választ mutatnak, amely elősegíti avesevédelmet nyújt, elnyeli a baktériumokat és megsavanyítja az internalizált baktériumokat. Az interkalált sejtek olyan hámsejtet képviselnek, amely professzionális fagociták, például makrofágok jellemzőivel rendelkezik.
Kulcsszavak:vesebetegség;veseszövet;vesesejtek;vese; vese-
A vesegyűjtő tubulus a sav-bázis szabályozás végpontja 1 . A gyűjtőtubulus fősejtekből és interkalált sejtekből (IC-k) áll. A fősejtek (PC-k) a só- és vízfelszívódást közvetítik, és a citoplazmatikus akvaporin 2 (AQP2) 2 jellemzi őket. Az IC-k segítenek fenntartani a sav-bázis homeosztázist, és három leírt altípusuk van: A típusú (A-IC), B típusú (B-IC) és nonA-nonB 2,3 . Az A-IC-k protonokat szekretálnak az apikális vakuoláris H-ATPázon (V-ATPáz) keresztül, és a hidrogén-karbonátot a bazilar klorid/bikarbonát (Cl − /HCO 3 ) transzporter, anioncserélő 1 (AE1/3. sáv/SLC4A1) 1,4 útján regenerálják. A B-IC-k HCO 3 -ot szekretálnak egy apikális Cl - /HCO 3 transzporteren, a pendrinen (SLC26A4) keresztül, és expresszálják a bazolaterális V-ATPáz 2,3-at. A rágcsáló nonA–nonB IC-k apikális pendrint és V-ATPázt tartalmaznak, de nincs AE1, és a gyűjtőcsatornában és az összekötő tubulusban (CNT) azonosították őket3. Egyre több bizonyíték támasztja alá az IC-k veleszületett immunszerepét, valamint hagyományos pH-szabályozási funkciójukat. Először is, a legtöbb tíz független beteg disztálisvese-A tubuláris acidózisról, az IC diszfunkcióval jellemezhető állapotról számoltak be, amelynek anamnézisében UTI szerepel5. Másodszor, az uropatogén Escherichia coli (UPEC), a férfiaknál az akut pyelo-nephritis 70 százalékában, míg a nők 80 százalékában izolált organizmus, szelektíven az IC-k citoplazmájában lokalizálódik 6,7. Harmadszor, megállapítottuk, hogy az IC-k antimikrobiális peptideket (AMP) expresszálnak, például a ribonukleáz 7-et (RNASE7) 8–11. Ezek az AMP-k közvetlen hatást fejtenek ki számos kórokozó ellen, beleértve a baktériumokat is, a kiinduláskor és/vagy a fertőzésre adott válaszként8–11. Negyedszer, mi és mások egymástól függetlenül beszámoltunk arról, hogy a rendellenes IC-fejlődésű egerek fokozott érzékenységet mutatnak a húgyúti fertőzésekre (UTI) és/vagy a pyelonephritisre12,13. Ötödször, az IC-k érzékelik és közvetítik a gyulladást 14 . Végül kimutattuk a veleszületett immungén-expressziót izolált egér IC-kben 15,16

A CISTANCHE JAVÍTJA A VESE/VESE MŰKÖDÉSÉT
Fontos megérteni, hogy az IC-k hogyan védik meg a húgyúti rendszert a fertőzésekkel szemben, mivel gyakran találkozunk húgyúti fertőzésekkel. A nők több mint 50 százaléka tapasztal húgyúti fertőzést élete során, és a húgyúti fertőzések az összes orvosi látogatás 1–6 százalékát teszik ki 17 . Amikor a baktériumok felszállnak aveseami pyelonephritist eredményez, a lehetséges szövődmények közé tartozik a magas vérnyomás, krónikusvesebetegség, és urosepsis 18,19 . Becslések szerint évente 250000 pyelonephritises eset fordul elő az Egyesült Államokban 17 . A több gyógyszerrel szembeni rezisztencia kritikus kihívásként jelenik meg a húgyúti fertőzések és más fertőzések kezelésében 20 . Ezért azok a mechanizmusok, amelyeket az IC-k a felszálló uropatogének elleni védekezésre használnak, terápiás célpontok lehetnek, amelyeket ki lehet használni a fejlesztésre.vese- specifikus pyelonephritis terápia. Mivel a legtöbb IC-vizsgálat állatmodelleket foglal magában, az emberi IC-k jobb megértésére lesz szükség ahhoz, hogy az alapvető tudományos tanulmányokat a jobb klinikai ellátás irányába tereljék.
Mert aveseEgy összetett szerv, az mRNS-profilokat nehéz lehet értelmezni. Például a nefron regionális specializációval rendelkezik, különböző tubuláris szegmensekkel és sejtaltípusokkal. Azveseendoteliális, epiteliális, intersticiális és toborzott gyulladásos sejteket tartalmaz, amelyek mindegyike eltérő biológiai funkciókkal és génexpressziós mintákkal rendelkezik. Az egysejtes RNS-szekvenálás (scRNA-seq) egy gyorsan fejlődő módszertant képvisel a különböző sejttípusok azonosítására és profilálására a kiinduláskor vagy a stresszorokra adott válaszként 21 . Itt bemutatjuk scRNA-seq technológia segítségével, hogy az emberveseAz IC-k hat különböző részhalmazból állnak, amelyek három A-IC-t, egy hibrid IC–PC-t, egy nonA–nonB IC-t és egy B-IC-t tartalmaznak. Az RNS-sebesség-analízis azt mutatta, hogy az UPEC-expozíció hatására a PC-kről az A-IC részhalmazok felé eltolódik a transzkripció. Az ingenuity Pathway Analysis kimutatta, hogy a fagoszóma érése a kulcsfontosságú biológiai út az A-IC alcsoportban az UPEC expozíció után. Ezen az útvonalon belül a V-ATPázok a kulcsfontosságú résztvevők. Intravitális mikroszkóppal vizualizáltuk az IC-k in vivo UPEC-felvételét, és megerősítettük az ezekben az IC-kben internalizált UPEC savasodást. Végül egy egér UTI modell a V-ATPáz (Atp6v1b1) mRNS expressziójának növekedését mutatta. Ez a tanulmány megadja az alapot a V-ATPázt expresszáló hámsejtek bakteriális fagocitákként történő feltárásához és terápiás kezeléséhez.
Eredmények
A humán IC-ket mágnesesen aktivált sejtválogatással (MACS) lehet dúsítani hízósejt/őssejt növekedési faktor receptorral (CD117/c-KIT) bevont mágneses gyöngyökkel. Emberiveseszövet, elsősorban a normál szegélyekrőlvesetömeges reszekciók, 2–4- mm-es darabokra boncolták, majd a Cooperative Human Tissue Network [https://www.chtn.org] által a Dulbecco's Modified Eagle Medium (DMEM) jégen elhelyezett laboratóriumunkba helyeztük. A c-KIT-et sejtfelszíni markerként értékeltük az emberi IC-k szétválogatására, mivel a c-KIT-et sikeresen alkalmazták erre a célra egerekben22. A c-KIT expresszió a humán IC-kre lokalizálódik azon a felismerésen alapulva, hogy a c-KIT és a humán IC-marker V-ATPáz, B1 alegység (ATP6V1B1 gén) ugyanazokat a sejteket jelölte meg az emberben.veseszakasz (Kiegészítő 1. ábra) 22,23 . Mágneses válogatást követően, amely magában foglalta a CD45 plusz immunsejtek és az elhalt sejtek eltávolítását; a c-KIT-pozitív feltételezett IC-k feldúsulását az ATP6V1B1 mRNS expressziója igazolta, amely 8-12--szeresére nőtt c-Kit-pozitív sejtekben a c-KIT-negatív sejtekhez képest. Mind az SLC4A1, mind az SLC26A4 változóan dúsított IC-kben, bizonyítva, hogy mind az A-IC, mind a B-IC dúsítás lehetséges ezzel a módszerrel (2. kiegészítő ábra). A tanulmányban használt veseszövet hátterét az 1. kiegészítő táblázat mutatja be.
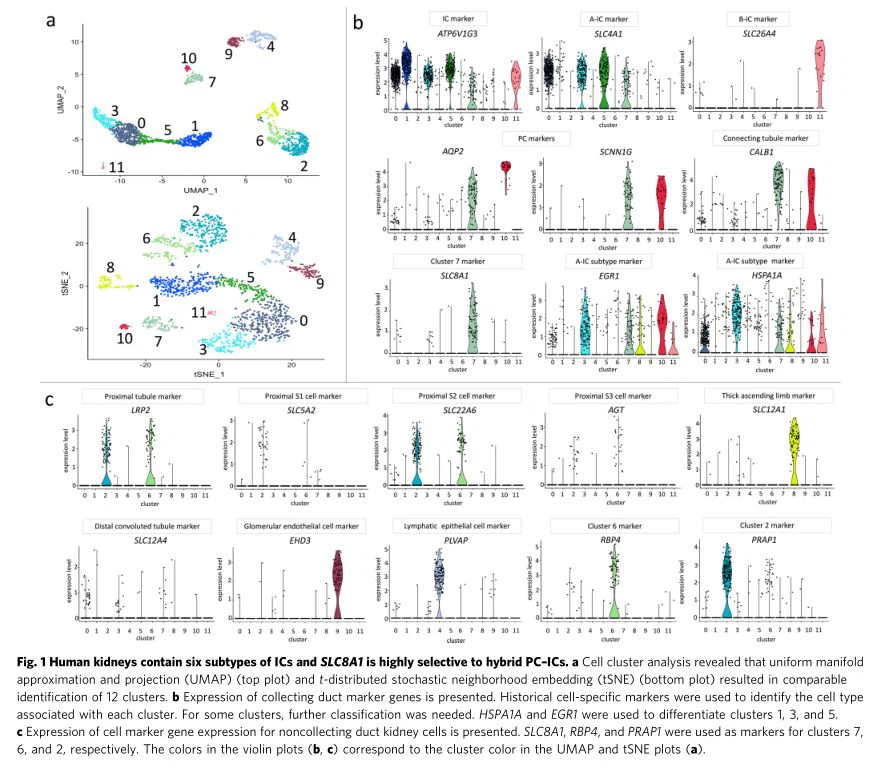
Az integrált klaszteranalízis hat IC altípust azonosított.Az ScRNA-seq 1861 disszociációval fejeződött bevesesejteket, amelyeket a fent leírtak szerint dúsítottak IC-kkel. A dúsított IC-ket egyetlen normál margóról kaptukvesetömeges reszekció. A minőség-ellenőrzési (QC) szűrést 859 UPEC-nek in vitro 1 órán át, és 1002 sejten 1 órán át sóoldattal kezeltük. A Seurat-funkció elemzése 12 klasztert azonosított a szétválogatott sejtpreparátumban (1a. ábra). Az egyes klasztereken belüli kilenc leginkább konzervált markert a kiegészítő ábrákon mutatjuk be. 3–14. Összességében az IC altípusok az 1861 sejt 1066-át (57 százalékát) tették ki. A klaszterek közül hat IC altípust képviselt. Pontosabban, három A-IC, egy B-IC, egy nonA–nonB-IC és egy hibrid PC–IC altípust találtunk.VeseChen és munkatársai által javasolt hámsejt-nómenklatúra, a korábban sejttípusú markereknek vagy a 12 klaszter egyikét megkülönböztető konzervált markereket használtak az egyes klaszterek sejttípusának meghatározásához (2. kiegészítő táblázat). , 1b, c, 2. ábra) 24–28.
Az A-IC altípus és a hibrid PC-IC fehérje expressziója korrelál az scRNS-seq eredményekkel. Megerősítettük a legfontosabb scRNA-seq megállapításokat, nevezetesen, hogy az SLC8A1 (más néven Na plus /Ca plus cserélő 1 (NCX1)) a hibrid PC–IC-k markere, és hogy a hősokk-fehérje család A (Hsp70) 1A tagja (HSPA1A) a korai növekedési válasz 1 (EGR1) mellett olyan markerek, amelyek meg tudják különböztetni az A-IC altípusokat (3. ábra). Mert a normál margóit használtukveserákreszekciók során validáltuk, hogy az SLC8A1, HSPA1A és EGR1veseAz expressziós mintázatok megegyeztek a normálban látottakkalveseszövet a Humán Protein Atlaszból, amely elérhető a http://www.proteinatlas.org webhelyről (15. kiegészítő ábra) 29
A korábban egérben kimutatott duktusejt-altípus markerprofilok összegyűjtéseveseA sejtek nagyrészt érintetlenek maradnak az emberbenvesesejteket. Mivel fontos lesz a jövőbeli egérmodell-eredményeket összefüggésbe hozni a humán patofiziológiával, értékeltük a korábban Chen és munkatársai által végzett scRNS-seq vizsgálatok során azonosított egér-gyűjtő duktusejt-markerek humán IC expresszióját. 22 és Ransick et al. 30 . Az eredmények pontdiagramját a 4. ábra mutatja be. Az egér-gyűjtő duktusejt-típusú markerek többnyire konzerváltak a humán gyűjtőcsatorna sejtekben.
Az A-IC A altípus relatív százalékos aránya nő 1 órás UPEC-expozícióval. A klasztereken belüli sejtek százalékos aránya konzisztens volt az expozíciós típusok között, kivéve az A-IC altípus A/klaszter 0, amely 16,2-ről 20,1 százalékra nőtt, és az A-IC C altípus/klaszter 5, amely 9,4-ről csökkent. 6,6 százalékra, sóoldattal szemben az UPEC-expozícióval, P =0,03 (1. táblázat).
A hibrid PC–IC sejtek az 1 órás UPEC expozíció hatására megváltoztatják RNS sebességüket a PC-ktől az A-IC felé. A közelmúltban átírt nem illesztett pre-mRNS-ek relatív mennyisége az érett illesztett mRNS-hez viszonyítva felhasználható az mRNS abundancia változásának kiszámítására, amelyet mRNS sebességnek nevezünk31. Az egysejtű vizsgálatokban kapott pozitív mRNS-sebesség azt jelzi, hogy a gének felszabályozása zajlik, míg a negatív mRNS-sebesség a gének leszabályozását jelenti31. Az RNS sebességi iránya arra következtet, hogy egy sejt mRNS expressziós pályával rendelkezik egy másik sejttípus felé 31,32. Az UPEC-expozícióra adott mRNS-sebesség az 5. ábrán látható. Fontos, hogy a hibrid PC-IC-k az UPEC hatására megváltoztatják RNS-sebességüket a PC-ktől az IC-k felé. Ezenkívül az IC-k fenntartják transzkripciós aktivitásukat, míg a transzkripciós aktivitás minimális lesz másoknálvesesejttípusok.
A vese veleszületett immunprofilja néhány korai egysejtes expressziós változást mutat 1 órás UPEC-expozíciót követően.A kiválasztott veleszületett immungének scRNS-seq expressziós mintázatait az UPEC és a sóoldat 1 órás expozícióját követően mutatjuk be a kiegészítő ábrákon. A kulcsfontosságú eredmények közé tartozik az AMP adrenomedullin (ADM) magas expressziója az A-IC A és B altípusában, a hibrid PC–IC és a B-IC. A PC-k a kiinduláskor nem expresszálnak adrenomedullint, de szignifikánsan megnövelték az expressziót az UPEC-expozíció hatására. A citokin-indukálható SH2-tartalmú fehérje (CISH) és az 1-es autointegrációs faktor (BANF1) expressziója szignifikánsan indukálódik a nonA–nonB IC-kben az UPEC expozíciót követően. Az interleukin 18-at (IL18), a galectin 3-at (LGALS3), a béta-defenzin 1-et (DEFB1) és a CD24 jelátalakítót, a lipocalin 2/neutrofil zselatinázzal asszociált lipokalint (LCN2/NGAL) csak azonosították
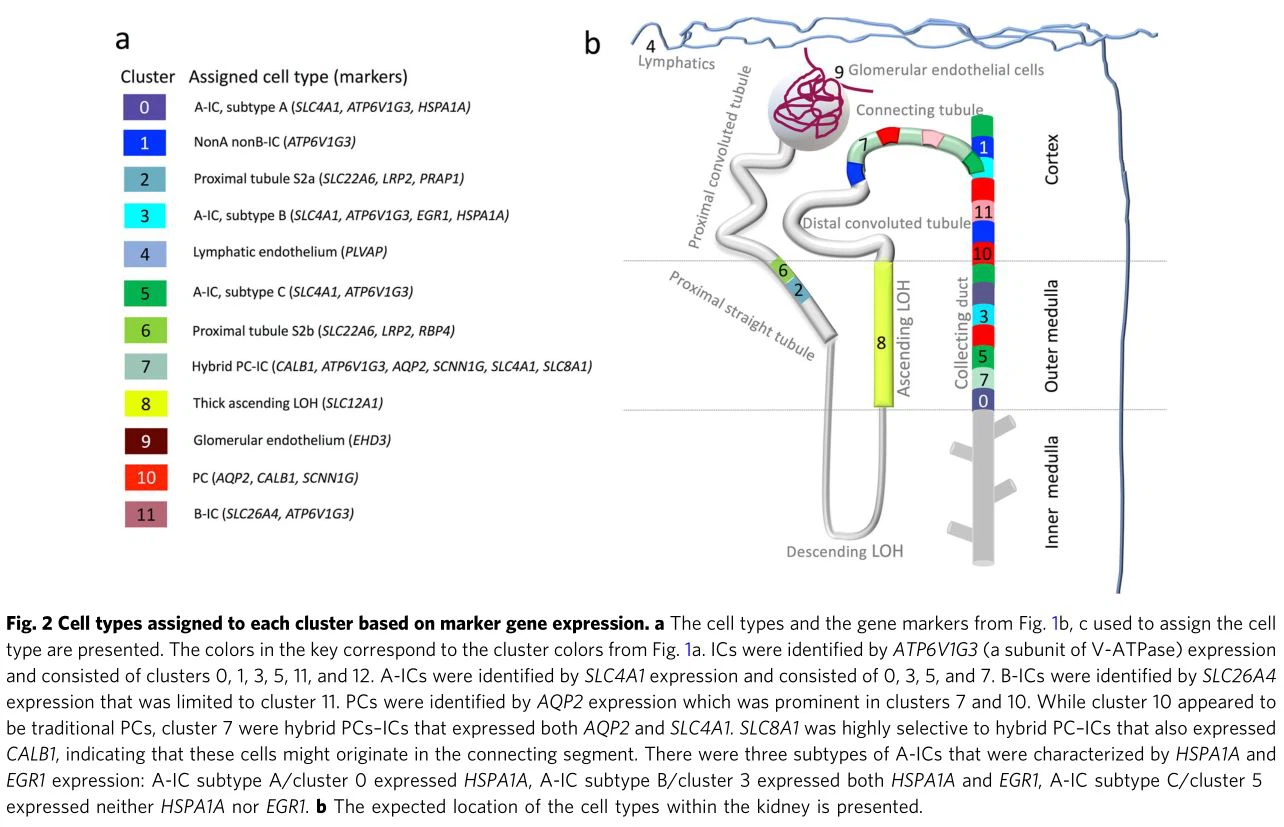
hibrid PC–IC-kben és csak minimális toll-like receptor 4 mRNS expresszió volt jelen. Nem azonosítottuk a ribo-nukleáz 7 (RNASE7) expresszióját az scRNS-seq-en. Kiértékeltük az RNASE7 mRNS expresszióját mágnesesen rendezett, összegyűjtött IC-ben és nem IC-benvesesejteket. Az RNASE7 mRNS expresszióját négyből egy IC-ben azonosítottákvese(Kiegészítő 18. ábra).
A fagoszóma érésének biológiai folyamata 1 órán át UPEC-nek kitett IC-kkel jár.Az egyes klaszterekhez kapcsolódó tíz vezető biológiai útvonalat p-érték szerint rangsoroltuk, a találékonysági útelemzés alapján. Három gyűjtőcsatornához rendelt klaszter: A-IC altípus A/klaszter 0, A-IC B altípus/ 3. klaszter és A-IC C altípus/5. klaszter eltérő biológiai folyamatokat mutatott az UPEC-expozíciót követően a sóoldattal összehasonlítva (3. ábra). 6a–c). Az UPEC-nek és sóoldatnak kitett sejtekben a fagoszómaérés volt a legrangosabb funkció az A-IC C altípusban/5-ös klaszterben, az A-IC altípusban az 5-ös klaszterben a másodikról az első helyre került az A-IC altípusban/klaszterben 0 és a negyedikről a harmadikra. Az A-IC B altípusban/ 3. klaszterben. A fennmaradó gyűjtőcsatorna-sejt-altípusok (19. kiegészítő ábra) egyike sem tartalmazta a tíz legfontosabb kapcsolódó útvonalat, amely eltérne az UPEC-expozíciót követően a sóoldattól. A 3. kiegészítő táblázat tartalmazza azt a génexpressziós profilt, amely a fagoszómaérési rangsort eredményezte az A-IC A-altípusra/klaszterre 0.
Az IC Atp6v1b1 mRNS expressziója növekszik válaszul akísérleti pyelonephritis in vivo.Az Ingenuity fagoszóma érési útvonala kiemelte, hogy a V-ATPáz részt vesz az IC-kben (3. kiegészítő táblázat). Annak meghatározására, hogy a V-ATPáz aktiválódik-e az UPEC expozíció hatására, egér UTI-modellt használtunk. Egy órával a transzuretrális UPEC vs sóoldat beoltás után "IC riporter" egereket, amelyek tdTomato (tdT, egy vörös fluoreszcens fehérje variáns) expressziót mutatnak az IC-kben, elaltatták, és az IC-ket feldúsították a disszociált egerekből.vesesejtek. A dúsított IC-k magasabb Atp6v1b1 mRNS-expressziót mutattak UPEC-oltású egerekben, mint a sóoldat-kontroll (6d. ábra).
Az IC-k in vivo fagocitizálják az UPEC-et.Módszertant dolgoztunk ki egy szingli perfundálásáravesetubulus UPEC-vel egy élő egérben, sértetlenvese.Zöld fluoreszcens fehérjét (GFP) expresszáló UPEC aggregátumokat mikroperfundáltunk az „IC reporter” egerek egyetlen vesetubulus lumenébe, amelyek tubulusokon keresztül áramlanak, szelektíven tapadnak a luminális felülethez, és az IC-k internalizálják őket (7. ábra) az intravitális mikroszkópia során.
Az IC-k az UPEC-et tartalmazó fagolizoszómákat in vivo savanyítják ésin vitro.A tubulusokat pHrodo Green E. coli biorészecskékkel is átperfundáltuk, amelyek csak savanyításkor fluoreszkálnak. Ezeknek a biorészecskéknek a felvételét és fluoreszcenciáját csak az intravitális mikroszkópia során tettük láthatóvá IC-kben (8. ábra). Az Imaris szegmentációs analízis azt mutatta, hogy a zöld fluoreszcencia idővel szignifikánsan megnőtt a tdT plusz IC-kben a pHrodo Green E. coli BioParticles-szel perfundált 2 tubuluson belül a kontroll tdT plusz tubulushoz képest (9a, b ábra). Ha a fluoreszcenciát celluláris alapon értékeltük, 12/16 (75%) tdT plusz sejt zöld fluoreszcenciájának növekedését mutatta az idő múlásával a pHrodo Green E. coli BioParticles-szel végzett tubuláris perfúziót követően (9b. ábra). Az egyes sejtekből származó lineáris regressziós eredményeket a 4. kiegészítő táblázat tartalmazza. A PHrodo Green E. coli BioParticles fagocitózisának és IC-k általi savasodásának élő in vivo intravitális képalkotási eredményeit in vitro áramlási citometriás vizsgálattal validáltuk. Egérvese sejt„IC-riporter” egerekből származó szuszpenzió, amelyben az IC-k (CD45-tdT plusz) endogén módon expresszálják a tdT-t, pHrodo Green E. coli BioParticles hatásának tették ki, szemben a pusztán tápközeget tartalmazó sejtekkel. A sejtszuszpenzióban lévő CD45 plusz rezidens immunsejteket pozitív kontrollként, a CD45 − tdT − (non-ICs) sejteket negatív kontrollként kapuztuk. Egyedül a médiát hasonlítjuk össze
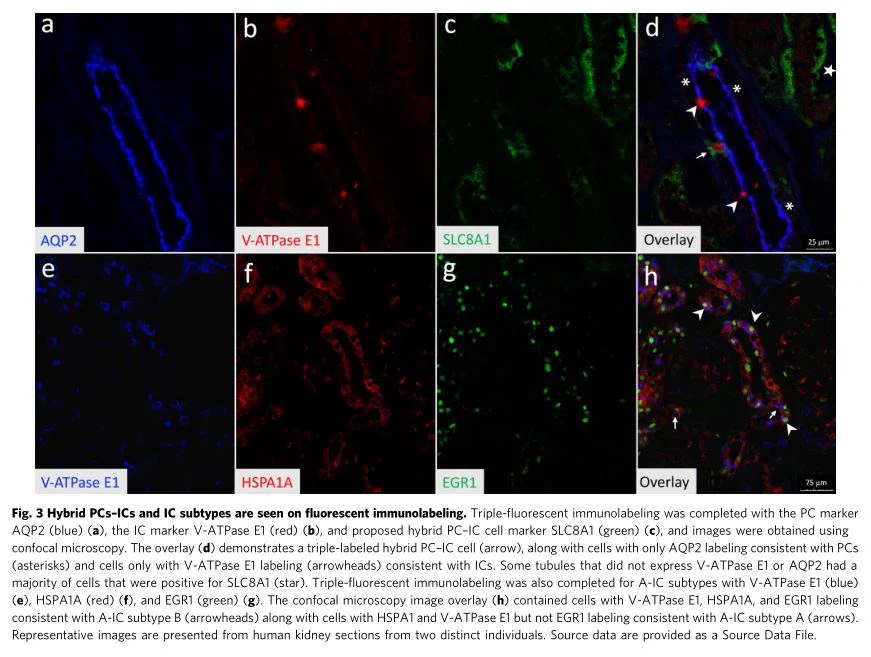
a biorészecskék expozíciója, a biorészecskék megszerzésére és savasodásra utaló zöld fluoreszcencia {{0}},7-ről 62,8 százalékra nőtt a CD45 plusz sejtekben. Ez a megállapítás azt mutatja, hogy a professzionális fagociták, például a neutrofilek várhatóan felveszik a baktériumokat. Érdekes módon az IC-k 22,2 százaléka vett fel zöld biorészecskéket, szemben a nem IC-k 5,6 százalékával (kiegészítő 2. ábra0), a tápközeg-kontroll az IC-k 0,7 százaléka és a nem IC-k 0 százaléka.
Vita
Az IC-ket nehéz tanulmányozni, különösen embereknél, mivel ezek mindössze 7 százalékát teszik kivesesejtek, egy sor altípusból állnak, és nem tartják meg fenotípusukat a tenyészetben33. Chen et al. 22 egysejtes elemzést számolt be egérenvesesejtek és Lake et al. egymagos RNS szekvenáló vezetékről számolt be emberenvesecellák 34,35 . Ezek a vizsgálatok az A-IC két altípusát azonosították. Itt módszertant dolgoztunk ki egysejtes szekvenálás végrehajtására életképes, dúsított humán IC-ken. Inkább életképes IC-kért dúsítottunk, nem pedig az összesetvesesejteket, hogy nagyobb fókuszt tegyen erre a sejttípusra. Elsődleges megállapításaink a következők voltak: (a) annak az azonosítása, hogy a hibrid PC-IC-k az UPEC-expozíció hatására az RNS-sebesség irányát a PC-ktől az A-IC-k felé változtathatják, (b) az A-IC-knek legalább három altípusa létezik, és ezek relatíve. a frekvenciák eltolódhatnak az UPEC-expozíció hatására, (c) a fagoszóma érése több A-IC altípus vezető biológiai útja, és relatív jelentősége nőhet az UPEC-expozícióval, és (d) az IC-k fagocitizálják és savanyítják az UPEC-et in vivo az élő képalkotás során egerek.
Az IC-k az acidózis hatására polaritásuk megfordításával differenciálódnak 36,37. A jelentések szerint az IC-k az AQP2--ot expresszáló sejtekből származnak38. 2017-ben Chen és munkatársai rágcsáló egysejt-profilozással azonosítottak olyan kettős pozitív sejteket, amelyek az Slc4a1 vagy Slc26a4 mellett Aqp2-t expresszáltak. Ezeket az eredményeket Park és munkatársai a következő évben igazolták 22,35 . 2019-ben fehérje és mRNS immunjelöléssel kimutattuk, hogy léteznek hibrid PC–IC-k 15 . Pontosabban, a V-ATPáz B1 fluoreszcens immunjelöléssel meghatározott rágcsáló IC-k 9%-a fluoreszcens in situ hibridizációval meghatározott Aqp2 mRNS-t is expresszált15. A jelen tanulmány meghatározta az emberi populációtvese- az AQP2-t, ATP6V1G3-at és SLC4A1-et expresszáló csatornasejtek összegyűjtése, összhangban a hibrid PC-IC-kkel. A tSNE és UMAP parcellákon ezek a hibrid sejtek csoportosultak a legközelebb a PC-khez, de az IC marker expressziója alapján különböztek a hagyományos PC-ktől. Az SLC8A1 expressziója különbözött ettől a sejttípustól. Érdekes módon az SLC8A1 nagymértékben részt vesz az epiteliális-mezenchimális átmenetben. Pontosabban, az SLC8A1 hiánya az E-cadherin 39 katenin által közvetített destabilizációján keresztül átalakítja az epiteliális sejt fenotípusait. Itt bemutatjuk, hogy az IC-k differenciálódnak az uropatogén expozíció hatására. A hibrid PC–IC sejtek az UPEC hatására megváltoztatják RNS sebességüket, az mRNS expresszió időbeli származékát, a PC-ktől eltérve az A-IC-k felé. Egerekben Ransick et al. 30 azonosította az Slc8a1 expresszióját elsősorban a disztális, csavarodott tubulusban, és a PC-kre emlékeztető sejteket az összekötő tubulusban. Konfokális mikrokópia képeinken kiértékeljükveseAz SLC8A1 expressziója során izolált sejteket találtunk, amelyek SLC8A1-et expresszáltak AQP2-pozitív tubulusokban (pl. gyűjtőcsatornákban vagy összekötő tubulusokban). Azonosítottunk továbbá AQP2-negatív tubulusokat, amelyekben a legtöbb sejt SLC8A1-et expresszált, ami potenciálisan összhangban van a fent említett disztális, csavarodott tubulus Slc8a1 expressziójával egerekben. Egyes A-IC altípusok eltérő vezető biológiai útvonalakkal rendelkeznek az UPEC expozíciót követően, és az A-IC A altípus relatív gyakorisága megnőtt az UPEC hatására. Ezek az eredmények azt mutatják, hogy az A-IC A altípus egy veleszületett immunvariáns lehet. Az SLC8A1 szerepe az IC-differenciálásban további vizsgálatokat igényel.

A CISTANCHE JAVÍTJA A vese-/veseelégtelenséget
1861 emberen scRNA-seq-et végeztünkvesesejt, amelyből 1066 volt IC. Ahhoz, hogy az egérkísérleti modelleket a humán patofiziológiával összefüggésbe hozzuk, fontos lesz az emberi és az egér IC-k összehasonlítása. Chen és munkatársai rágcsáló IC-ket dúsítottak c-KIT-tel, és scRNS-seq 22-t végeztek. 74 sejtet PC-nek, 87 sejtet A-IC-nek és 23 sejtet B-IC-nek 22 minősítettek. Ransick et al. 30 végzett scRNA-seq-et 688 IC-n. Nem dúsítottak az IC-kért, hanem inkább felosztották azvesea kéregbe, a belső velővel és a külső velővel a zonális különbségek értékelésére 30 . Kimutattuk, hogy az egér-gyűjtő duktusejt-típusú markerexpresszió nagyrészt konzerváltnak tűnik az emberi gyűjtőcsatorna sejtekben. Az, hogy az egerek A-IC altípusai hasonlóak-e az emberekhez, valószínűleg nagyobb számú egér IC-k célzott egysejtű értékelését teszi szükségessé.
Azonosítottuk a veleszületett immunfehérjék, például az immun- és gyulladásos mediátor galektin 3 (LGALS3) és az ADM scRNS-seq IC expresszióját, amelyekről korábban már beszámoltunk a rágcsálók 15,40–42 IC-jeiben. Azonban néhány kulcsfontosságú veleszületett immunfehérje, amelyet korábban az IC-kben jelentettek, mint például a Lipocalin 2 (LCN2/NGAL), az RNASE7 és a toll-like receptor 4 (TLR4) minimális expressziót mutattak, vagy nem voltak láthatók humán IC-kben egysejtszinten. elemzésünk 6,9 . Az LCN2/NGAL és a TLR4 expressziójának csekélysége az IC-kben összhangban van azzal, amit kutatócsoportunk, Ransick és mtsai. 30vesecellexplorer/] 15 . Chen et al. 22 jelentett némi TLR4 és NGAL mRNS expressziót IC-ben, de többszörösen kevesebbet, mint a PC-kben. Kiértékeltük az egyesített humán IC-ket az RNASE7 expressziójára, és 4-ből 1-ből azonosítottuk az IC-kben.vese(Kiegészítő 18. ábra), jelezve, hogy expressziója szakaszos lehet a régiótól, időponttól és fiziológiai körülményektől függően. Kimutatták, hogy a CISH-expresszió, amely nem A nonB IC-kben indukálódik az UPEC-re adott válaszként, szabályozza a Mycobacterium tuberculosis elleni veleszületett immunválaszt a tüdőben és a lépben43. Az IC-k néhány perc alatt fagocitáltak a baktériumokat, és az scRNS-seq sejtjeinket viszonylag rövid, 1 órás időtartamra UPEC-nek tesszük ki. Jövőbeli vizsgálatokra van szükség annak meghatározására, hogy az UPEC expozíciót követő későbbi időpontokban feltűnőbbé válnak-e más IC-útvonalak, mint például az AMP-expresszió vagy a sejthalál szabályozása.
Phagocytosis involves the cellular uptake of particulates >0.5 μm a plazmamembrán burkával 44 . A "professzionális fagociták", mieloid eredetű immunsejtek, beleértve a makrofágokat, neutrofileket és oszteoklasztokat, megkülönböztetik a behatoló mikrobákat a mikrobiotától és az egészséges sejtektől, bekebelezik a célpontot egy fagoszómába, reaktív oxigénfajtákat (ROS) hoznak létre, AMP-ket választanak ki és antigéneket mutatnak be egyéb sejtek 45–49 . Fontos, hogy a fagolizoszómák V-ATPáz általi erőteljes savanyítása, amely a legtöbb mikroba elpusztításához elegendő savas mikrokörnyezetet hoz létre, a professzionális fagociták jellemzője 48,50 . Például a V-ATPáz bafilomicin A1-gyel való gátlása elnyomja a makrofágok baktericid aktivitását51. Egyes hámsejtek fagocitizálják a mikrobákat, de kevésbé hatékonyak a baktériumok elpusztításában, mint a professzionális fagociták, és nem professzionális fagocitákként írják le őket 52 . Az IC-k olyan epiteliális vonalat képviselnek, amely fagocitózissal és antigén-prezentációs képességgel rendelkezik (6–9. ábra), valamint erőteljes AMP-expresszióval és nagyvonalú mitokondriumokkal, amelyek ROS-t generálnak; így úgy tűnik, hogy az IC-k a makrofágokkal összehasonlíthatóbb baktériumölő képességgel rendelkeznek, mint a fent említett nem professzionális fagociták 8,53–55. Korábban kimutatták, hogy az A-IC-k képesek a dextrán magas apikális endocitózisára a citoplazmatikus vezikulákba 56 . Úgy gondoljuk, hogy az UPEC IC fagocitózisa a makrofágokkal közös jellemzők kiterjesztése, beleértve a V-ATPáz expressziót, a redoxpotenciált, az AMP szekréciót és az endocitózis képességeit8,16,49,57,58. Azt még meg kell határozni, hogy az IC-k képesek-e a professzionális fagocitákhoz hasonló módon fagocitálni a sejttörmeléket és az UPEC-től eltérő baktériumokat.
Egyetlen konfokális képalkotásveseA baktériumokkal in vivo perfundált tubulus kiterjed a korábbi in vitro technikákra, mint például a sejttenyésztésre és a kimetszett tubulusok perfúziójára. Itt olyan módszert dolgoztunk ki, amellyel élő egereken közvetlenül teszteltük, hogy a fagocitózis IC-funkció-e. Az intravitális mikroszkópia lehetővé teszi a dinamikus sejtfolyamatok bonyolult tanulmányozását működő egérbenvese59 . Az intravitális mikroszkópia használatára vonatkozó korábbi stratégiák során intravitális festékek vagy markerek szisztémás injekciót adtak egerekbe a proximális tubulus endocitózisának tanulmányozására.vesea véráramlás dinamikája és a vaszkuláris vagy glomeruláris permeabilitás 60 . Ha az intravitális mikroszkópiát kifinomult sebészeti technikákkal kombinálják, a fertőzéses folyamatok nehezen értékelhető korai időpontjai tanulmányozhatók61. Korábban a baktériumokat mikroperfundálták patkányok proximális tubulusaiban, hogy értékeljék a véráramlást, a neutrofilek felszaporodását és a vizelet elzáródását62,63. A húgyúti fertőzések túlnyomó többsége a felszálló kórokozóknak köszönhető, és kezdetben a gyűjtőcsatornával találkozna64,65. Ezért azt javasoljuk, hogy a gyűjtőcsatorna egy kritikus tubuláris régió a gazda-patogén kölcsönhatások értékeléséhez. Intravitális modellrendszerünk hatékonyan teremt újra egy klasszikust

A CISTANCHE JAVÍTJA A VESE-/VESEBETEGSÉGET
egyetlen gyűjtő tubulus perfúziós vizsgálat, de élő egérben, ép egérrelvese,vér-, nyirok- és idegrendszeri ellátás, valamint az immunsejtekkel való kölcsönhatás megtartása. A pyelonephritis patofiziológiájában férfi és női különbségek vannak. Embereknél például a nőstényeknél ötször nagyobb valószínűséggel alakul ki akut pyelonephritis, de a hím egereknél a pyelonephritis androgén által közvetített fokozott súlyossága66,67. Ransick és munkatársai eltérő férfi és női különbségeket mutattak ki a proximális tubulussejtekben, különösen a szerves aniontranszporterekben30. A férfi IC-ket mind az egysejtes szekvenálási, mind az intravitális vizsgálataink során értékeltük. Az IC-k szerepe miatt a bakteriális védekezésben aveseés az elektrolit-egyensúly, az IC-funkciók, például a fagocitózis és az egysejtű génexpresszió, a nemekkel kapcsolatos sokféleség kulcsfontosságú területei lesznek a jövőbeli tanulmányoknak. Ennek a tanulmánynak vannak korlátai. Az UPEC expozíciója a humán IC-knek az scRNS-szekvenciánkban in vitro egyetlenveseés különbségek lehetnek az in vivo UPEC expozícióhoz képest. Ezen túlmenően eredményeink az ember anatómiai régióját képviseltékveseA különböző helyszíneken végzett mintavételes és jövőbeni tanulmányok regionális diverzitást mutathatnak, amint azt Ransick et al. 30 . Az IC-k a sejtek 57 százalékát tették ki az scRNS-szekvenciánkban, a kb. 7 százalékos IC-összetételből dúsítva.vesealapvonalon 33 . Mintánk tartalmazott néhány más epiteliális és endoteliális sejttípust is, de negatív volt a CD45 plusz immunsejtekre, amelyeket az IC-k feldúsítása előtt kiválogattunk (1. ábra, 1. kiegészítő ábra). Az scRNA-seq segítségével a cél IC-ket külön lehetett azonosítani és értékelni. A hematopoietikus őssejtek expresszálják a c-KIT-et, de valószínűleg nem képviselik aveserezidens mieloid sejtpopulációk 68 . Nem azonosítottunk más, egészséges emberben jelen lévő c-KIT-et expresszáló sejteketvese, mint például a stromasejtek/telociták 69 . Korábban már beszámoltak a Henle izolált hurokról és a proximális tubulus c-KIT pozitivitásárólveseimmunhisztokémia összhangban van scRNS-seq eredményeinkkel 70
