A minták szétválasztása és a forrásmemória különálló hippocampális és neokortikális régiókat von be a visszakeresés során
Mar 14, 2022
Kapcsolatfelvétel: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mail:audrey.hu@wecistanche.com
Bevezetés
A múltbeli események részletes ábrázolása az elemek és azok kontextuális jellemzői (pl. forrás) közötti asszociációs képességen alapulmemória), valamint annak képessége, hogy egy új eseményt egyértelműen ábrázoljon a tárolt hasonlótólmemória(azaz minta elválasztás). Ismeretes, hogy ezek a folyamatok befolyásolják a hippocampust, bár továbbra sem tisztázott, hogy hasonló mechanizmusokkal rendelkeznek-e. Az sem ismert, hogy az ezekkel a folyamatokkal kapcsolatos tevékenységek átfedik-e és/vagy kölcsönhatásba lépnek-e, és melyik régió(k)ban. Itt nagy felbontású fMRI-t használtunk, hogy megvizsgáljuk a hippocampális részmezők és a neokortikális területek hozzájárulását a minták elválasztásához és a forráshoz.memóriakísérleti paradigmával, amely egyszerre tesztelte mindkettőt. A kódolás során férfi és női alanyok véletlenül a képernyő négy kvadránsának egyikében tanulmányozták az elemeket. A teszt során megtekintették az ismétlődő elemeket (célpontokat), hasonló tárgyakat (csalik) és új elemeket (fóliákat), és megkérték őket, hogy jelezzék, hogy minden egyes elem régi, hasonló vagy új. Az egyes tételek megítélését követően az alanyokat arra kérték, hogy jelöljék meg azt a kvadránst, amelyben az eredeti inger mutatkozott. Így minden csalipróbának volt egy csali megkülönböztető komponense (adózási minta szétválasztása) és egy helymeghatározás (forrásmemória).Két fő válaszprofilt találtunk: (1) mintázat-elválasztással kapcsolatos jelek a DG/CA3-ban és a perirhinális kéregben és (2) a forrásmemóriajelek a hátsó CA1-ben, a parahippocampalis kéregben és az angular gyrusban. A teljes agy voxelwise elemzése feltárta, hogy a tevékenység a megkülönböztetés és a forrás csábításával kapcsolatosmemórianagyrészt átfedésmentes volt. Ezek az eredmények azt sugallják, hogy a mintázattól elválasztott elemreprezentációk előhívása és a forrásinformációk felidézése eltérő folyamatok hátterében állnak.
Kulcsszavak: kontextus; fMRI; hippocampus;memória; minta elválasztás;forrásmemória
a citanche gyógynövény előnyei: javítja a memóriát
A részletes epizodikus emlékek az elemek és a kontextusok (azaz a forrásmemória) közötti asszociációk kialakításának képességétől függenek, valamint attól, hogy képesek-e megkülönböztetni a hasonló elemeket vagy eseményeket a memóriában (azaz minták szétválasztása). Rengeteg bizonyíték utal arra, hogy a forrásmemória a hippokampuszra támaszkodik, amelyről azt gondolják, hogy az elemek és a kontextus közötti kapcsolatot reprezentálja (Diana et al., 2007). Rágcsálókon végzett vizsgálatok kimutatták, hogy a hippocampalis CA1 "helysejtek" kódolhatnak tárgyak és helyek közötti asszociációkat (Komorowski et al., 2009), míg az embereken végzett, nagy felbontású fMRI-t alkalmazó vizsgálatok azt mutatták, hogy az asszociatív memória során megnövekedett aktivitás a CA1-ben és a subiculumban kódolás és visszakeresés (Eldridge et al., 2005; Viskontas et al., 2009; Suthana és mtsai, 2015). A forrásmemória tanulmányozása általában összehasonlítja az elemfelismeréssel kapcsolatos tevékenységet (S ) és anélkül (S μ ) egy adott kontextuális részlettel (pl. térbeli elhelyezkedés), és az egyedüli elemfelismerést (S μ ) a kevésbé részletes, alacsonyabb pontosságú memóriával teszik egyenlővé. (Frithsen és Miller, 2014; Hutchinson és mtsai, 2014). Ezek a tanulmányok gyakran nem mutatják ki a hippocampális elkötelezettséget a tárgyfelismerésben a kapcsolódó kontextus (S μ ) visszakeresése nélkül. Maga az elemmemória azonban nagyon részletes lehet. Az elemek megkülönböztetett, nagy pontosságú reprezentációit kell kialakítani (mintaelválasztással), hogy megkülönböztessük őket a memória hasonló elemeitől. A forrásmemóriához hasonlóan a mintázatok szétválasztása is a hippokampuszra támaszkodik, rágcsálókban (Leutgeb et al., 2007; Neunuebel és Knierim, 2014), valamint az emberi mnemonikus diszkriminációs paradigmákban (Bakker et al., 2008; Berron et al. al., 2016), ami arra utal, hogy a gyrus fogazat (DG) kritikus szerepet játszik az átfedő bemenetek ortogonalizálásában.

Kattintson a Cistanche-ra a memóriaért
A hippokampuszon kívül a hátsó mediális kérgi területek széles hálózata támogatja a kontextust és a forrásmemóriát (Ranganath és Ritchey, 2012; Reagh és Ranganath, 2018). A parahippocampal cortex (PHC) térbeli/kontextuális információkat kódol a hippocampus mellett, míg az oldalsó hátsó parietális kéregben, különösen a gyrus szögletében zajló aktivitás az epizodikus részletek visszakereséséhez kapcsolódik (Johnson et al., 2013; Hutchinson et al., 2014). A közelmúltban végzett vizsgálatok azt találták, hogy a hippokampuszon kívüli kérgi régiók is hozzájárulhatnak a mintázatok szétválásához (Reagh és Yassa, 2014; Leal és Yassa, 2018). Például csoportunk legutóbbi munkája kimutatta, hogy a perirhinális kéreg (PRC), a hippokampuszba kinyúló ventrális „mi” folyam része, részt vesz a hasonló objektumok mnemonikus megkülönböztetése során (Reagh és Yassa, 2014).
Egy jól validált elem-megkülönböztetési feladatot használva, amelyet úgy módosítottak, hogy tartalmazzon egy forrásmemória-komponenst, a laboratóriumunkban végzett korábbi munkák azt mutatták, hogy a minták szétválasztása (azaz téves riasztások) hiányában is előfordulhat helyes forrásmemória-ítélet, jelezve, hogy ezek a folyamatok, amelyek feltehetően részletes hippocampális reprezentációkra támaszkodnak, legalábbis viselkedésileg disszociálhatók (Kim és Yassa, 2013). Nem ismert azonban, hogy ezek a folyamatok milyen mértékben hoznak létre különálló vagy átfedő jeleket a hippocampális alrégiókban és a kérgi területeken. A jelen tanulmány nagy felbontású fMRI-t (1,8 mm-es, majdnem teljes agyi lefedettséggel) használt a hippocampalis részmező és a kérgi aktivitás egyidejű felmérésére a hasonló csalielemek megkülönböztetése és a forrásmemória megítélése során. Korábbi fMRI vizsgálatok azt figyelték meg, hogy a hasonló csalik helyes kilökődése során a DG/CA3 régióban az aktivitás megegyezik az új fóliák aktivitásával (Bakker et al., 2008). Ez az aktivitási mintázat összhangban van a mintaelválasztási jellel, mivel a hasonló elemeket új elemként kezelik, és nem váltják ki az ismétlődés visszaszorítását (azaz az fMRI-adaptációt), amelyet azonos ismétlések esetén észleltek. Azt jósoltuk, hogy ezt a mintaelválasztó jelet látjuk majd a DG/CA3-ban a hasonló csalielemek helyes elutasítása során, míg a hippocampus más alrégiói (CA1 és subiculum) érzékenyek lesznek a forrásmemóriára (magasabb aktivitási szint a helyes forráshoz, szemben a helytelennel forrásítéletek). Mivel közel teljes agyi fMRI-lefedettséget szereztünk, azt is meg tudtuk vizsgálni, hogy a hippokampuszon kívül mely régiókban jelennek meg disszociált vagy átfedő mintázat-elválasztási és forrásmemóriai jelek.

A Cistanche javíthatja a memóriát
Anyagok és metódusok
Tantárgyak
Harmincegy egészséges alanyt kezdetben az irvine-i Kaliforniai Egyetemről és a nagyobb Orange megyei közösségből vontak be a vizsgálatba. Ebből a kezdeti mintából egyet kizártak a szkenner berendezésének meghibásodása miatt, egyet a kísérletből való idő előtti visszavonulás miatt, kettőt kizártak legalább egy feladatkörülményben való véletlenszerű teljesítmény miatt, kettőt pedig túlzott mértékű miatt. mozgás a szkennelés során. Ez a végső mintát eredményezte, amely 25 vizsgálati alanyból állt (17 nő, életkor 18-29 év, átlag 20,6 év, SD 2,47 év). A felvételkor minden alanyt szűrtek neurológiai állapotok (pl. stroke vagy mentális betegség anamnézisében), alváshiány és a depresszió főbb tünetei (a Beck Depression Inventory segítségével). Az alanyok írásos beleegyezésüket adták a Kaliforniai Egyetem Irvine Institutional Review Boardja után, és részvételükért kártérítést kaptak.
Feladat
A feladatot korábbi munkánkból (Kim és Yassa, 2013) adaptáltuk, és MRI-szkennerben való használatra optimalizáltuk (1A. ábra). A résztvevők először egy véletlenszerű vizsgálati fázist fejeztek be, amelyben 226 közös tárgy jelent meg a képernyő négy pozíciójának egyikében 3 másodpercig (1 s interstimulus intervallum), és azt a feladatot kapták, hogy jelezzék, hogy az egyes objektumok gyakrabban találhatók-e bent vagy kint. A képernyőt négy egyenlő kvadránsra osztották, és a tárgyak a négy pozíció egyikében jelentek meg (az egyes alanyokhoz beállított ingerek szerint véletlenszerűen). A vizsgálati szakaszt követően egy 300 kísérletből álló meglepetéstesztet végeztek. A 300 objektumból 74 teljesen újszerű volt (fóliák), 74 azonos volt a vizsgált tárgyakkal (célpontokkal), 150 pedig hasonló, de nem azonos a vizsgált objektumokkal (csalik). A vizsgálati fázishoz hasonlóan a tárgyak 3 másodpercig jelentek meg a képernyőn, és az alanyok feladata volt annak megítélése, hogy minden tárgy "régi", "hasonló" vagy "új"-e (ez a célpontoknak, csaliknak és fóliáknak felel meg). Ezen túlmenően, a tételértékelést követően a résztvevők elvégezték a forrásmemória értékelését. Ha a résztvevők a "régi" vagy a "hasonló" lehetőséget választották egy késleltetést követően, egy képernyő kérte őket, amely számozott kvadránsokat mutatott, és 3 másodpercet kaptak, hogy kiválasszák azt a kvadránst, ahol az eredeti objektumot látták. A csalik esetében egyértelművé tették az alanyok számára, hogy a forrás megítélése arra a vizsgált elemre vonatkozik, amelyhez a csali hasonló (olyan állapotot eredményez, amelyben feltehetően mintázatszétválás, valamint kontextuális emlékezés történt). Ha a résztvevők az "új" kifejezést választották a kvadráns ítélet helyett, akkor jelezniük kellett, hogy "biztosak" vagy "bizonytalanok" az ítéletüket illetően (analízisünkben nem tettünk különbséget ezek között a konkrét ítéletek között, és csak a következőt vettük figyelembe: fel a fóliákra, hogy megfeleljen a cél- és csalipróbák forrásítéletei által igénybe vett időnek). A válaszok gombnyomással történtek, és az egyes gombokhoz tartozó képernyőn megjelenő ikonok pirosan világítottak, amikor megnyomták, hogy segítsenek a résztvevőknek a kívánt válaszokhoz való hozzárendelésében.
MRI
beszerzés A neuroimaging adatokat egy 3.{1}} Tesla Philips Achieva szkenneren gyűjtöttük, egy 32-csatornaérzékenység kódoló tekercs segítségével a Kaliforniai Egyetem Irvine-i Neuroscience Imaging Centerében. Minden munkamenet elején nagy felbontású 3D MP-RAGE szerkezeti letapogatást végeztünk (0,75 mm-es izotróp voxelek): TR 11 ms, TE 4,43 ms, 200 szeletek, 0,75 mm izotróp, FOV 231 240 150. Az fMRI-vizsgálatok egy T2*-súlyozott EPI-szekvenciából álltak, BOLD kontrasztot használva: TR 3000 ms, TE 26 ms, 70 fokos átbillentési szög, 43 szelet, 1,8 x 1,8 mm-es síkbeli felbontás, 1,8 mm-es szeletszárvastagság 0,2 mm-es hézaggal, FOV 180 77,4 180. A szeleteket részleges axiális térfogatként vettük fel, eltolás vagy szögelés nélkül, így majdnem az egész agyat lefedték. A T1 jel stabilizálása érdekében négy kezdeti "álpásztázást" végeztünk. Összesen 6 funkcionális futtatást szereztek be minden résztvevő számára: 2 vizsgálati fázist és 4 tesztfázist. Minden vizsgálati futam 387 másodpercig tartott (123 dinamika), és minden tesztfutás 468 másodpercig tartott (150 dinamika).
MRI előfeldolgozás és ROI szegmentálás
Az összes neuroimaging adatot az Analysis of Functional NeuroImages (AFNI, 17.2.00) (Cox, 1996) segítségével GNU/Linux és Mac OSX platformokon előre feldolgoztuk és elemeztük. Az elemzések nagyrészt a szabványos afni_proc.py folyamatot követve zajlottak. Az EPI-ket a mozgás (3dvolreg) és a szeletidőzítés (3dTshift) szerint korrigáltuk, az agyon kívüli voxelek kizárása érdekében maszkoltuk (3dautomaszk), majd simítottuk (3dmerge) 2.{{10}} mm-es Gaussian FWHM kernellel. . A mozgáskorrekciós paramétereket szöveges fájlokba mentettük, hogy később lineáris regresszióban felhasználhassák (lásd MRI adatelemzés). Minden egyes futtatást megvetettek, hogy tovább csökkentsék a mozgás befolyását az adatokra (3dDespike). A funkcionális szkenneléseket az egyes alanyok koponyától lecsupaszított MP-RAGE-jához igazították (align_epi_anat.py). Az Advanced Normalization Tools segítségével az egyes résztvevők szerkezeti szkennelését egyedi, házon belüli, nagy felbontású 0,75 mm-es izotróp sablonunkba csomagoltuk SyN nemlineáris regisztrációval (Avants et al., 2011). Az ezekből a vetemítésekből származó paramétereket arra is használták, hogy a funkcionális szkenneléseket a sablontérbe vetítsék a csoportos ROI elemzésekhez. A maszkokat újra mintavételeztük, hogy megfeleljenek a simított fMRI adatok felbontásának (2,0 mm-es izotróp), és további maszkolást végeztünk, hogy kizárjuk a részben mintavételezett voxeleket a futtatásokon belül és azok között (3dcalc). Végül az adatokat a globális futáson belüli átlagra (3dcalc) normalizáltuk úgy, hogy az ezt követő együtthatók az alapvonalhoz viszonyított százalékos változást tükrözzék.
A hippocampális ROI-kat megállapított protokolljaink alapján határoztuk meg (pl. Yassa et al., 2010; Reagh és Yassa, 2014) (2. ábra). Röviden, a hippocampális almezők szegmentálását Yushkevich és munkatársai által közölt SY protokoll szerint végezték. (2015) egyéni, nagy felbontású csoportsablonunk használatával, bár a CA1-subiculum határát frissítettük, hogy tükrözze a hippocampális szegmentációs protokollok harmonizálására irányuló közelmúltbeli erőfeszítéseket (Wisse et al., 2017). A korábbi tanulmányokhoz hasonlóan (Reagh és mtsai, 2017), a hippocampális almezők elülső és hátsó részeit szegmentáltuk, mivel hipotéziseket fogalmaztunk meg a hátsó mediális temporális lebeny (MTL) specifikus részvételéről a kontextuális memóriában (Ranganath és Ritchey, 2012). Ezt a felosztást az uncalcsúcs után közvetlenül a szeletre helyezték el, így az "elülső" hippocampális részlegünk kifejezetten a hippokampusz fejére vonatkozik, míg a "hátsó" felosztás a testre és a farokra. Az angular gyrus ROI-t úgy határoztuk meg, mint egy inkluzív ROI-t, amelynek középpontja a szögletes gyrus, de magában foglalja a hátsó parietális kéreg szomszédos régióit.
Kísérleti tervezés és statisztikai elemzés
Viselkedési elemzések. A statisztikai elemzéseket GraphPad Prism 8.1.2 programmal végeztük. A kísérleteket az item (régi, hasonló, új) és a forrásmegítélés (forráshelyes és helytelen forrás) szerint osztályoztuk, és kiszámítottuk a válaszok arányát az egyes vizsgálattípusokra. A viselkedési hatások tesztelésére ismételt mérésű ANOVA-t futtattunk mind a célpontokra, mind a csalikra, tárgyi válasz (régi és hasonló) és forrásmemória (helyes és helytelen forrás) mellett, mint tárgyon belüli tényezők. Post hoc t-teszteket végeztünk a Holm–Sidak-féle többszörös összehasonlító teszttel a szignifikáns kölcsönhatások vizsgálatára.
MRI módszerek. Az elemzésekbe csak a visszakeresési adatok kerültek be. Létrehoztunk egy GLM-et regresszorokkal a céltalálatokhoz, a csali helyes elutasításokhoz (LCR) és a csalogató téves riasztásokhoz (LFA), mind a megfelelő, mind a helytelen forrásmeghatározással, valamint a megfelelő elutasításokkal (a megbízhatósági ítéletek összeomlásával). A téves riasztások, a célkihagyások, a csali kihagyások és a válaszadás nélküli kísérletek ritkaságuk és az értelmezési nehézségeik miatt érdektelenség regresszorává zuhantak. Ezenkívül tartalmaztunk regresszorokat hat mozgásvektorhoz, amelyek a mozgáskorrekciós előfeldolgozási lépésből származnak (x, y, z, pitch, roll, yaw). A GLM-et AFNI-ben futtattuk 3dDeconvolve segítségével. A hemodinamikai válasz dekonvolúcióját sátorfüggvényekkel végeztük, amelyek lefedik az inger fellépését a kezdet után 15 másodpercig, és 6 becslési függvényt osztottunk el ebben az időablakban. A mozgási paraméterek explicit regresszorként kerültek be a modellbe, hogy csökkentsék a fej mozgásának a feladattal kapcsolatos paraméterbecslésekre gyakorolt hatását, és a válaszadás nélküli kísérleteket annak érdekében, hogy kizárják ezeket a kétértelmű kísérleteket, hogy befolyásolják a modell maradványait. Ezenkívül az időbeli eltolódást modellező vektorokat regresszorként adtuk meg, amelyek lefedik az első, másod- és harmadrendű polinomokat. Az érdeklődésre számot tartó körülményeinkre vonatkozó válaszbecsléseink elkészítésekor kifejezetten kivontuk az új fólia-elutasításokat alapfeltételként. Röviden, ez azt az értelmezést adja, hogy az alapvonaltól való eltérések valószínűleg memóriavezérelt. Minden funkcionális futtatásnál a 0,5 mm-es keretelmozdulást meghaladó mozgású TR-eket (de a 3 mm-es kizárási küszöb alatti) cenzúráztuk az elemzésekből, valamint a közvetlenül megelőző és követő TR-eket. Végül az ANATICOR segítségével a kamrákból és a fehérállományból származó globális jelet kizártuk a szürkeállomány voxelekből (Jo et al., 2010). Ezeket az „adatsúroló” eljárásokat arra használták, hogy a lehető legnagyobb mértékben kizárják a fej mozgásának az aktiválási profilokra gyakorolt hatását (Power et al., 2012).
A második szintű elemzésekbe bevitt végső súlyok az első három becslési függvény átlagából álltak (a BOLD válasz csúcsának rögzítésére célozva). ROI elemzések. ROI-elemzéseinkhez a súlyokat az alapvonalhoz képest százalékos változásra konvertáltuk, majd kivontuk az a priori ROI-kból (3dmaskave). A statisztikai elemzéseket GraphPad Prism 8.1.2 és SPSS 26.0 (IBM) segítségével végeztük. A hippocampalis és a neocorticalis ROI-k hatásainak vizsgálatához ismételt mérésű kétirányú ANOVA-kat alkalmaztunk csali megkülönböztetéssel (LCR és LFA) és forrásmemóriával (helyes és helytelen), mint alanyon belüli tényezőkkel. Azon régiókban, ahol az aktivitás különbözött a féltekénként, a jobb és a bal agyféltekét külön vettük figyelembe. Azokban a régiókban, ahol az aktivitás nagyon konzisztens volt (pl. hátsó DG/CA3 és a szögletes gyrus), az adatokat a féltekéken összevontuk. A megfigyelt hippocampális mintázat-elkülönülés és a forrásmemória-hatások közvetlen összehasonlítása érdekében a parciális μ 2 négyzetgyökét mind a csali megkülönböztetés, mind a forrásmemória effektusok esetében Fisher z értékére konvertáltuk. Ezután Z-pontoztuk ezeknek az értékeknek a különbségét az alrégiók között (pl. Fisher z (csali) Z pontszáma a DG/CA3-ban μ Fisher z (csali) a CA1-ben). Holm–Sidak korrekciót alkalmaztunk a hippocampális almezőkön (n 12) annak vizsgálatára, hogy mely hippocampális hatások élték túl a többszörös összehasonlítás korrekcióját. Azon régiókban, ahol a csali megkülönböztetésének fő hatását figyeltük meg, egymintás t-teszteket futtattunk, amelyek az LCR-ek aktivitását hasonlították össze a kiindulási értékkel (fólia helyes elutasítások). Azokban a régiókban, ahol az aktivitás nem volt összhangban az előre jelzett mintaelválasztási forrásmemóriajelekkel, a céltalálatokat bevontuk az elemzésbe. Ezekben a régiókban ismételt mérésű, kétirányú ANOVA-kat végeztek, tárgymemóriával (LCR, LFA és céltalálatok) és forrásmemóriával (helyes és helytelen) mint tárgyon belüli tényezővel. A Holm–Sidak többszörös összehasonlító tesztjét használó post hoc t-teszteket használtunk az elemmemória főbb hatásainak tesztelésére.
Voxelwise elemzések. A hipotézisvezérelt ROI-alapú megközelítésünkön kívül megvizsgáltuk a csali megkülönböztetésének és a forráshoz kapcsolódó főbb hatásoknak, valamint az átfedési területeknek az egész agyra kiterjedő feltáró funkcionális térképeit az AFNI 17.2-es verziójával.00. Ennek érdekében az egyes alanyok együtthatóit bevittük egy ismételt mérésű ANOVA-ba (3dANOVA3), ahol a csali megkülönböztetés (LCR és LFA) és a forrásmemória (helyes és helytelen) alanyon belüli fix faktorként, az alanyok pedig véletlenszerű tényezőként szerepeltek. A szignifikáns aktiválási térképeket többszörös összehasonlításra korrigáltuk családi hibaarány-korrekcióval, legalább 46 összefüggő voxel terjedelmével, p 0.05 küszöbérték mellett (3dClustSim, nemrég frissítve a nem szándékos infláció kezelésére). Vizualizáláshoz binarizáltunk jelentős F-statisztikai térképeket a csali megkülönböztetés és a forrásmemória egyedi hatásaira, majd egyetlen térképpé egyesítettük őket egy egyszerű lépésfüggvény segítségével (azaz a csali megkülönböztető effektus voxelek 1 értéket kaptak, a forráshatás voxelek értéke 2, és az átfedő effektusokat tartalmazó voxelek együttes értéke 3).

Eredmények
Viselkedési megállapítások
Először megvizsgáltuk a régi, hasonló és új válaszok átlagos arányát az egyes ingertípusokra (célpont, csali vagy fólia) (1B. ábra). Összességében az alanyok helyesen tudták azonosítani a célpontokat régiként (65 százalék), a fóliákat pedig újként (69 százalék), míg a csalit tárgyakat gyakran hibásan azonosították régiként (36 százalék) a hasonlók helyett (49 százalék). Ez a viselkedési minta az LCR-ek és az LFA-k eloszlását jelzi, és megismétli a korábbi eredményeket ugyanazzal a feladattal (Kim és Yassa, 2013). Ezt követően a teljesítményt vizsgáltuk a forrásmemória megítélésének második szakaszában. Ismételt mérésű ANOVA-t futtattunk a tételre adott válaszon (régi és hasonló) és a forrásmemórián (helyes forrás és helytelen forrás) mind a célpontok, mind a csalik esetében. A célok esetében megtaláltuk az itemválasz és a forrásmemória fő hatását, valamint egy interakciót (elemválasz: F(1,24) 53,4, p 1,5 10 μ 7, forrás: F(1,24) ) 5.7, p 0.3, interakció: F(1,24) 16.6, 0.0004), több céltalálással (a helyesen régiként azonosított célpontok), mint voltak olyan célpontok, amelyeket tévesen hasonlónak és helytelenebbnek ítéltek meg, mint a helytelen forrásmegítélést. A post hoc t-tesztek azt mutatták, hogy az alanyok gyakrabban döntöttek helyesen a forrásmemóriából a célponttalálatok esetén (F(1,24) 5,7, p 0,02; forráshelyes vs forrás helytelen: átlagos különbség 0,14, p 0,05), ami azt jelzi, hogy amikor az alanyok a céltárgy pontosabb ábrázolása, általában jobb forrásmemóriával rendelkeztek az adott elemhez. Azt találtuk, hogy a csalik esetében nagyobb arányban fordult elő a helyes elutasítás (a megfelelően azonosított csalik, LCR), mint a téves riasztások (a csalik tévesen azonosították réginek, LFA) (F(1,24) 4,8, p 0,04) (1C. ábra) , de nincs szignifikáns különbség a helyes és helytelen forrásítéletek számában (F(1,24) 3,14, p 0,09). Kritikus módon ezek az adatok megismétlik a korábbi eredményeket, amelyek a forrásmemória és a minták szétválasztása közötti viselkedésbeli disszociációra utalnak, és azt mutatják, hogy helyes forrásmemóriai ítéletek születhetnek mintaszétválasztás (azaz téves riasztások) hiányában, és hogy elemszintű mintaszétválás történhet helytelen forrás esetén. emlékítéletek.

Neuroimaging leletek
Nagy felbontású (1,8 mm-es izotróp) fMRI-t alkalmaztunk, amely lehetővé teszi a közel egész agy felvételét, hogy megvizsgáljuk az elem- és forrásmemória megítélése során végzett regionális aktivitást. Minden ROI esetében ismételt mérésű ANOVA-t futtattunk a csalielemeken, rögzített tényezőkként a csali megkülönböztetést (LCR és LFA) és a forrásmemóriát (helyes forrás és helytelen forrás). Azon régiókban, ahol a csali megkülönböztetésének fő hatását figyeltük meg, t-teszteket futtattunk, amelyek az LCR-ek aktivitását hasonlították össze a kiindulási értékkel (fólia helyes kilökődés). A 3. és 4. ábra a jel százalékos változását mutatja be az egyes alrégiók esetében, minden érdeklődésre számot tartó körülmény között (LCR-ek, LFA-k, céltalálatok, külön-külön figyelembe véve az S és Sμ feltételeket).
Megkülönböztetett hippocampális mintázat elválasztás és forrásmemória jelek
A bal elülső DG/CA3 és a bilaterális hátsó DG/CA3 aktivitása nagyobb volt a helyes elutasításoknál, mint a hamis riasztásoknál, a helyes elutasítások aktivitása pedig megegyezett a fólia helyes elutasításával (azaz alapvonallal) (3C, E, F ábra); bal elülső DG/CA3: F(1,24) 6,9, p 0.016, t-teszt LCR vs alapvonal: t(24) 0.46, p {{ 21}},65; bal hátsó DG/CA3: F(1,24) 5,426, p 0.029, t-teszt LCR vs alapvonal: t(24) 1,3, p {{ 38}}.22; jobb hátsó DG/CA3: F(1,24) 1{{4{{50}}}},6, p 0.0{ {80}}3, t-teszt LCR vs alapvonal: t(24) 0.35, p {{1{{107}}1}}.73 ). Ez az aktivitási mintázat összhangban van a mintaelválasztó jellel (3A. ábra), mivel a helyesen elutasított csalikat úgy kezelik, mintha új elemek lennének (azaz a fólia helyes elutasítása), míg a tévesen régi csalikként azonosított csalik ismétlődés-elnyomást mutatnak. A jobb hátsó CA1 aktivitása erőteljesebben kapcsolódott be a helyes forrásmeghatározáshoz, mint a helytelen forrásmeghatározáshoz (3J. ábra; jobb hátsó CA1: F(1,24) 12,6, p 0,002), összhangban a forrásmemória jelével (3B. ábra). ). Szintén marginális volt a forrás hatása a jobb hátsó subiculumban (F(1,24) 2,7, p 0,11; 3N ábra). Ezeket a forráshatásokat akkor is megfigyelték, amikor a céltalálatokat bevontuk az elemzésbe (jobb hátsó CA1: F(1,24) 18,8, p 0,0002; jobb hátsó subiculum: F(1,24) 8,9, p 0,006). A mintaelkülönülés és a forráshatások közvetlenebb összehasonlítása érdekében az alrégiók között a részleges μ 2 -t Fisher z -re konvertáltuk, majd Z-pontoztuk ezeknek az értékeknek a különbségét az alrégiók között. Azt találtuk, hogy a mintázatszétválasztó hatás kismértékben nagyobb a jobb hátsó DG/CA3-ban (jobb hátsó DG/CA3 csali μ jobb hátsó CA1 csali Z különbsége 1,8, p 0,07), és a forráshatás kissé nagyobb a jobb hátsó CA1-ben. (jobb hátsó DG/CA3 forrás μ jobb hátsó CA1 forrás Z különbség μ 1,9, p 0,05). Hasonló mintát találtunk a bal elülső és hátsó DG/CA3 és CA1 hatásainak összehasonlításakor (bal elülső DG/CA3 csali μ jobb hátsó CA1 csali Z különbség 1,4, p 0,16; bal elülső DG/CA3 forrás μ jobb hátsó CA1 forrás Z különbség μ 2,05, p 0,04; bal hátsó DG/CA3 csali μ jobb hátsó CA1 csali Z különbség 1,2, p 0,2; bal hátsó DG/CA3 forrás μ jobb hátsó CA1 forrás Z különbség μ 1,85, p 0,06). A jobb hátsó DG/CA3 mintázatszétválasztó hatás, valamint a jobb hátsó CA1 forráshatás túlélte a Holm–Sidak korrekciót a hippocampális almezők többszöri összehasonlításához (n 12).

A bal hátsó CA1-ben és a bal hátsó PHC-ben az ismertségi és újdonságjelek A bal hátsó CA1-ben és a bal PHC-ben az aktivitás olyan válaszprofilokat mutatott, amelyek nem voltak összhangban a megjósolt mintázat-elválasztással vagy a forrásmemória jeleivel vagy a kettő közötti kölcsönhatással. A bal hátsó CA1-ben a forrás fő hatása volt; azonban a helytelen forrásmeghatározás aktivitása nagyobb volt, mint a helyes forrásmeghatározásé (S μ = S ) (F(1,24) 5.9, p 0.02). A bal oldali PHC-ben a csali megkülönböztetés volt a fő hatása, ahol a csali helyes elutasítása nagyobb volt, mint a csali téves riasztásai (F(1,24) 6.3, p 0.02). A csali helyes kilökődésének aktivitása azonban megnövekedett az alapvonalhoz képest (LCR = alapvonal) (t(24) 2,5, p 0.02). Mint ilyen, a céltalálatok bekerültek az ANOVA-ba, hogy jobban megvizsgálják e régiók bekapcsolódását a felismerési memória során, ami egy 2 2 ismételt mérésű ANOVA-t eredményezett elemmemóriával (LCR-ek, LFA-k és céltalálatok) és forrásmemóriával (forráshelyes és hibás forrás) rögzített tényezőkként. Amikor a céltalálatokat belefoglaltuk, az elemmemória (3I. ábra; F(2,48) 5.4, p 0.008) és a forrás (F() hatását figyeltük meg 2,48) 6.2, p 0.02) a bal hátsó CA1-ben, a post hoc tesztek nagyobb aktivitást mutattak a céltalálatok esetében, mint az LCR-ek és az LFA-k esetében (LCR vs Találatok: átlagos különbség μ { {60}}.07, p 0,01; LFA vs találatok: átlagos különbség μ 0,06, p 0,03). Ez az aktivitási mintázat a hippokampuszban gyakran megfigyelhető „ismeretségi jelet” tükrözheti, amely a korábban látott tárgyaknál nagyobb aktivitást mutat, mint az újdonságoknál (Reagh et al., 2014; Rutishauser és mtsai, 2015). A bal oldali PHC mind az elem (4E. ábra; F(2,48) 6,7, p 0,003), mind a forrás (F(1,24) 7,9, p 0,01) hatását mutatta, nagyobb aktivitással a helyes elutasításokhoz (LCR vs LFA : átlagkülönbség 0,08, p 0,01; LCR vs. Találatok: átlagkülönbség 0,1, p 0,004) és helytelen forrásmegítélések esetén. Bár ez a régió nagyobb aktivitást mutatott az LCR-eknél, mint az LFA-knál, ez nem követi a sok fMRI-vizsgálatban tapasztalt szabványos mintázatszétválasztó jelet, mivel a csali helyes kilökődésének aktivitása nem volt egyenlő a fóliás helyes kilökődéssel (LCR= FCR). Inkább a helyes elutasítások csábításának megnövekedett aktivitása tükrözheti a cikkek újdonságának különösen erőteljes jelzését. A tételinformáció forrásával kapcsolatos bizonytalanság hozzájárulhat mind a bal hátsó CA1-ben, mind a bal PHC-ben megfigyelt, helytelen forrásokkal kapcsolatos vizsgálatok megnövekedett aktivitásához.
Voxelwise elemzés
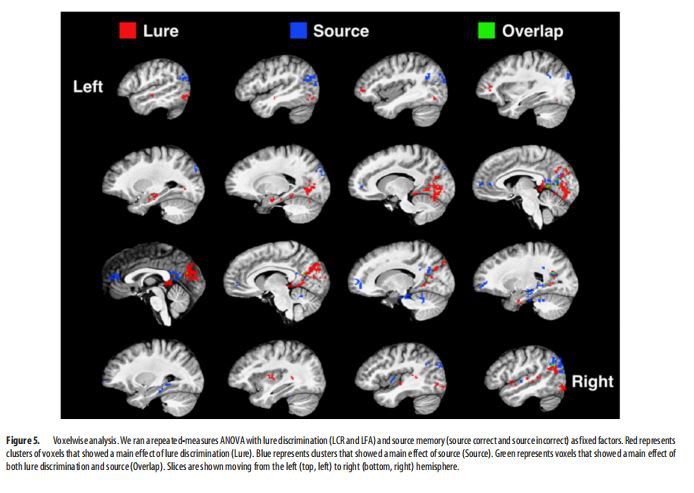
Annak érdekében, hogy azonosítsuk azokat a régiókat, ahol mind a csali megkülönböztetés, mind a forrásmemória átfedő hatásai lehetnek, amelyek kívül esnek a priori ROI-kon, feltáró voxel-analízist végeztünk. Futtattunk egy ismételt mérésű ANOVA-t a csali megkülönböztetés (LCR vs LFA) és a forrásmemória (forráshelyes vs. helytelen forrás) fix tényezőként. Az 5. ábra voxelcsoportokat mutat be, amelyek a csali megkülönböztetés (piros) vagy forrás (kék) fő hatását mutatták, valamint azokat a voxeleket, amelyek mind a csali megkülönböztetés, mind a forrás (zöld) fő hatását mutatták. Ez az elemzés három fő témát tárt fel. Először is, a diszkrimináció csábításával kapcsolatos tevékenység erőteljes aktivitást eredményezett a ventrális látófolyamban és az elülső MTL-ben, különösen az elülső hippocampusban és a PRC-ben. Ezzel szemben a forrásmemóriával kapcsolatos tevékenység olyan régiókban ösztönözte az aktivitást, mint az mPFC, a retrosplenialis cortex és a szögletes gyrus, amelyek gyakran szerepet játszanak a forrásmemóriában (Ranganath és Ritchey, 2012; Johnson és mtsai, 2013; Hutchinson et al., 2014). ). Ezenkívül a forrásmemória hatások nagyrészt jelen voltak a hátsó MTL-ben, beleértve a hippocampust és a PHC-t. Másodszor, bár ez kevésbé volt nyilvánvaló a ROI-alapú elemzéseinkben, a csali megkülönböztetés és a forráshatások meglepő mértékű oldalirányúságot mutattak az MTL-ben. Az anterior-posterior disszociációk mellett a csalikkal kapcsolatos aktivitás az MTL-ben inkább baloldali, míg a forrásmemóriával kapcsolatos aktivitás inkább jobb oldali volt. Harmadszor, annak ellenére, hogy a retrosplenialis kéregben, a precuneusban és a jobb szögletű gyrusban előfordult néhány közös voxel, a csali megkülönböztetés és a forrásmemória aktivitástérképei meglepően nem fedték egymást. Ez különösen feltűnő a sok csali- vagy forrásvezérelt voxel miatt, amelyek szomszédosak, de nincsenek megosztva.

Cistanche kiegészítés:javítja a memóriát
Vita
Leírunk egy nagy felbontású fMRI-vizsgálatot, amelynek célja a forrásmemória és a mintázatok szétválásának egyidejű tesztelése, valamint a hippocampalis almező és a neokortikális hozzájárulások ezekhez a folyamatokhoz való felmérése. Korábbi viselkedési munkánkat megismételve azt találtuk, hogy a helyes forrásmemóriai ítéletek előfordulhatnak minták szétválásának hiányában (és fordítva), ami azt jelzi, hogy ezek a folyamatok viselkedésileg disszociálhatók. Az ezekkel a folyamatokkal kapcsolatos jelprofilokban is disszociációt találtunk, a hippocampális részmezők és a kérgi ROI-k nagyrészt átfedő hatásokat mutatnak. Egyik vizsgált régióban sem figyeltek meg kölcsönhatást a forrásmemória és a csali megkülönböztetés között. Ezek az eredmények arra utalnak, hogy bár a forrásmemória és a mintázatok szétválása egyaránt hozzájárul a részletes epizodikus emlékezethez, és mindkettő a hippokampusztól függ, ezeket a folyamatokat különálló idegi mechanizmusok támogatják.
Amint azt előre jeleztük, a DG/CA3-ban egy jelet figyeltünk meg, amely összhangban van a mintázatok elválasztásával, az LCR-ek aktivitása nagyobb, mint az LFA-ké, és egyenértékű az új fóliák aktivitásával. Ez összhangban van ennek a régiónak az átfedő bemenetek ortogonalizálásában javasolt szerepével. Megfigyeltünk egy forrásmemória jelet a jobb hátsó CA1-ben és a jobb hátsó subiculumban, összhangban azokkal a korábbi tanulmányokkal, amelyek megnövekedett aktivitást mutattak visszakereséskor az asszociatív memória helyes megítélése érdekében ezekben a régiókban (Eldridge et al., 2005; Viskontas et al., 2009; Stevenson et al., 2018). Egyetlen hippocampális részmező sem mutatott átfedő hatást a csali megkülönböztetés és a forrásmemória között, vagy jelentős kölcsönhatást.
Megjegyezzük, hogy a mnemonikus diszkrimináció tesztelésére szolgáló módszerünk és a BOLD válaszadaptáció ezzel járó hiánya a hasonló elemekre adott válaszként a mintázatok szétválasztásának közvetett mértéke. Ezenkívül a hippocampális almezők jelprofiljaiban megfigyelt disszociáció ellenére ezeket az adatokat nem szabad arra utalni, hogy ezek a régiók nem vesznek részt sem a forrásmemória, sem a mintaelválasztási folyamatokban. Sok bizonyíték támasztja alá, hogy a DG/CA3 régió támogatja a forrásmemóriát, ha átfedés van az elemek és a hozzájuk tartozó kontextus között (pl. minden nap ugyanabban a helyen parkol az autó). Ezenkívül a CA3 alrégióról régóta úgy gondolták, hogy részt vesz a minta befejezésében vagy a kapcsolódó információk visszakeresésében, ha részleges jelzéssel mutatják be (O'Reilly és Norman, 2002; Kumaran et al., 2016). Úgy gondolják, hogy ez a folyamat kritikus a forrásmemória szempontjából (pl. egy elem megtekintése kiválthatja az adott elem helyének visszakeresését). Úgy gondolják, hogy a CA1 támogatja a minták szétválasztását azáltal, hogy a CA3 mintázattól elválasztott reprezentációit visszakapcsolja az entorhinalis kéreg bemeneti mintáihoz (Norman, 2010). A CA1 hozzájárulhat az emlékező diszkriminációhoz azáltal, hogy „match-mismatch” detektorként működik, jelezve a visszakeresett eredeti elem és a csali közötti eltéréseket (Duncan et al., 2012). Mivel a subiculum a hippocampus fő kimenete, ez a régió valószínűleg számos hippokampuszfüggő folyamatban vesz részt, beleértve a forrásmemóriát és a mintázatok szétválását. Ennek megfelelően fenntartjuk, hogy mind a forrásmemória, mind a mintázatok szétválasztása összetett hippocampális áramkörökre támaszkodik, nem pedig különálló régiókra. Valójában Libby et al. (2018) azt találta, hogy a hippocampális aktivitás mintái megkülönböztetést tettek a hasonló elemek és hasonló kontextusok között, de a kontextusban hasonló elemekre általánosítottak, ami összetett interakciókra utal. A jelen tanulmányban a forrásmemória és a mintázatok szétválasztása által kiváltott disszociált jelek azonban azt mutatják, hogy ezek a folyamatok különálló idegi mechanizmusokra támaszkodhatnak, amelyek azonosíthatók, ha a két folyamatot egymással szembeállítják egy kísérleti tervben.
Ezt a disszociációt a hippocampuson kívül is megfigyelték, a PHC és az angular gyrus fokozott aktivitást mutatott a helyes forrásmeghatározáshoz (nincs mintaelválasztó jel), a PRC pedig mintaelválasztó jelet mutat (nincs forrásmemória jel). Ez az aktivitási mintázat összhangban van a PHC jól bevált szerepével a térbeli/kontextuális feldolgozásban, valamint az angular gyrus szerepével az epizodikus részletek visszakeresésében. A ventrális „mi” folyam részeként a KNK régóta köztudott, hogy részt vesz a cikkfelismerésben. Csoportunk közelmúltbeli, hasonló feladattal végzett munkája azt mutatta, hogy ez a régió részt vesz a hasonló objektumok mnemonikus megkülönböztetése során (Reagh és Yassa, 2014). A jelenlegi eredmények megismétlik ezt a hatást, és egyre bővülő irodalmat egészítenek ki, amely a kérgi területeken a mintázat-elkülönüléshez hasonló hatásokat vizsgálja (Reagh és Yassa, 2014; Kent és mtsai, 2016; Pidgeon és Morcom, 2016). Úgy gondolják, hogy a Kínai Népköztársaság összetett észlelési diszkriminációban vesz részt, ami hozzájárulhat a későbbi mnemonikus diszkriminációhoz (Barense et al., 2011). Ezek az eredmények összhangban vannak a reprezentációs-hierarchikus modellel is, amely szerint a KNK olyan összetett elemjellemzőket képvisel, amelyek kevésbé valószínű, hogy a hasonló elemek között megoszthatók, és mint ilyenek, képesek feloldani az interferenciát ezen elemek között (Kent et al., 2016). . Bár ez nem feltétlenül tükrözi a minták szétválását a számítási modellek hagyományos értelmében, ez egyfajta megkülönböztetést jelent az átfedő bemenetek között. A forrásmemória és a mintázatszétválasztó jelek közötti disszociációt tovább erősítette egy voxel-alapú elemzés, amely feltárta, hogy néhány megosztott voxel kivételével a hátsó kérgi területeken, a diszkrimináció csábításával és a forrásmemóriával kapcsolatos tevékenység nagyrészt nem volt átfedésben.
Míg az eredményeket hipotéziseink keretein belül próbáltuk értelmezni, nem zárhatjuk ki annak lehetőségét, hogy más tényezők is hozzájárulhattak a megfigyelt eredménymintázathoz. Mivel kísérleti paradigmánk hasonló objektumokat használt a minták szétválasztására és a térbeli elhelyezkedést a forrásmemória tesztelésére, az egyik alternatív értelmezés az, hogy a megfigyelt mintaelválasztási és forrásmemóriai hatások tükrözhetik az objektumot, illetve a térbeli feldolgozást. Ez az értelmezés azonban nem magyarázza meg, hogy a megfigyelt hatások miért illeszkednek a specifikus válaszprofilhoz, amelyet az előre jelzett mintaelválasztási jelünk határoz meg, ahol a helyes elutasítások aktivitása nagyobb, mint a téves riasztások esetében, és egyenértékű a fólia helyes elutasításaival. Ezen túlmenően, ha ezt a hatást kizárólag az objektumfeldolgozás, nem pedig a minták szétválasztása vezérli, akkor nem feltétlenül várnánk, hogy ezt a hatást a DG/CA3-ban látjuk, mivel az objektumfelismerés gyakran nem érinti a hippokampuszt. Ezzel szemben az interferenciával szembeni objektumfelismerés, a feltételezett mintázatszétválasztás nem befolyásolja a DG/CA3-at, ami arra utal, hogy ez az, ami a megfigyelt hatásokat ebben a régióban vezeti. A PRC-ben és a PHC-ben megfigyelt disszociáció összhangban van az objektum versus térbeli értelmezéssel, mivel ismert, hogy ezek a régiók részt vesznek az objektum-, illetve a térbeli feldolgozásban. Mivel azonban a DG/CA3-ról kimutatták, hogy mind az objektum-, mind a térbeli feldolgozásra reagál, a tartományspecifikusság nem magyarázza egyértelműen a megfigyelt eredmények mintázatát. A jövőbeni tanulmányok különböző típusú minták szétválasztását vagy forrásmeghatározását használhatják annak meghatározására, hogy a megfigyelt jelenségek az objektum/térbeli feldolgozásra jellemzőek-e, vagy általánosíthatók-e a modalitásokon keresztül.
A másik lehetőség az, hogy a minták szétválasztását és a forrásmemória hatását a kódolás, illetve a visszakeresés vezérelhette, mivel a hasonló csalik helyes elutasítása viszonylag több kódolással kapcsolatos folyamatot is magában foglalhat. A kódolás és a visszakeresés azonban rendkívül dinamikus folyamatok, és a kódolási és visszakeresési folyamatok kombinációja egyaránt hozzájárul a tételek megkülönböztetéséhez és a forrásmemóriához. Például a hasonló csalik helyes elutasítása valószínűleg magában foglal egy „visszahívás az elutasításhoz” stratégiát. A harmadik lehetőség az, hogy a minták elválasztását és a forrásmemória hatását a minta elválasztása és a minta-kiegészítés vezérelhette, mivel a forrásmemória döntései egy részleges jelzés (az elem) alapján egy térbeli hely lekérését foglalják magukban. A minták szétválasztása és befejezése azonban nem zárja ki egymást, és a kódolással és a visszakereséssel kapcsolatos folyamatokhoz hasonlóan valószínűleg az összes különböző próbatípusunkban részt vesz. Például érvelhetnénk azzal, hogy a tételek megkülönböztetése magában foglalja a minta kiteljesedését is, mivel ezek a kísérletek valószínűleg egy „visszahívás az elutasításhoz” stratégiát foglalják magukban, amint azt fentebb megjegyeztük. Mint ilyen, sem a kódolás versus visszakeresés, sem a minta elválasztása a minta befejezése közötti disszociáció nem magyarázza egyértelműen a megfigyelt eredmények mintázatát.
A forrásmemória effektusok nagyrészt jelen voltak a hátsó MTL-ben, beleértve a hátsó hippocampust és a PHC-t, összhangban a legújabb elméletekkel, amelyek szerint ez a régió egy erősen összekapcsolt hátsó hálózat része, amelyről úgy gondolják, hogy részt vesz a kontextuális és térbeli feldolgozásban, beleértve a szögletes gyrust és a retrosplenialis kéreget. (Ranganath és Ritchey, 2012). Érdekes módon a mintaelválasztó hatások mind az elülső, mind a hátsó DG/CA3-ban jelen voltak. Míg egyes elméletek összekapcsolják az elülső hippocampust több pályával, lényegi alapú memóriával, amint azt Poppenk et al. (2013) szerint ez a DG/CA3 almező egyenetlen eloszlását tükrözheti a hippocampus hosszú tengelye mentén, mivel a hátsó hippocampusban magasabb a DG/CA3 aránya, mint más almezőkben. Eredményeink arra utalnak, hogy legalább a DG/CA3-on belül mind az elülső, mind a hátsó hippocampus támogatja a részletes epizodikus memóriát.
Ezek az eredmények rávilágítanak az epizodikus memória több aspektusának egyetlen kísérleti paradigmában történő tesztelésének értékére. Bár a forrásmemória és a mintázatok szétválasztása egyaránt befolyásolja a hippokampuszt, mindkét folyamat egyidejű tesztelésével meg tudtuk figyelni, hogy az ezekkel a folyamatokkal kapcsolatos tevékenységek átfedik-e és/vagy kölcsönhatásba lépnek-e, és hol. Itt azt találtuk, hogy a forrásmemória és a minták szétválasztása különböző mechanizmusokat használ. Ez a disszociáció magyarázatot adhat arra, hogy az emberek miért nagyon jól emlékeznek a kontextusra, de tévesen azonosítanak bizonyos személyeket vagy elemeket. A jövőbeni tanulmányok megvizsgálhatják azokat a körülményeket, amelyek között a forrásmemória és a mintázatok szétválasztása kölcsönhatásba léphet.

javítja a memóriátcistanche

