A vesebetegségek kezelésére tervezett vértisztító anyagok terápiás alkalmazásának legújabb trendjei
Jul 10, 2023
Absztrakt
A vértisztítás egy általánosan használt módszer a felesleges anyagcsere-hulladék eltávolítására a vérben a vesepótló kezelés során. Ezeknek a toxinoknak a vérből történő megfelelő eltávolítása csökkentheti a szövődményeket és javíthatja a túlélési időt a dializált betegeknél. A jelenlegi biológiai vértisztító anyagok azonban nem ideálisak a klinikai gyakorlatban, ahol kielégítetlen igény mutatkozik olyan új anyagok előállítására, amelyek jobb biokompatibilitásúak, csökkentik a toxicitást, és különösen hatékonyabbak a toxinok eltávolítási sebessége és alacsonyabb előállítási költsége. Tekintettel erre, ez az áttekintés gondosan összefoglalta az újonnan kifejlesztett különböző szerkezeti biomedicinális anyagokat a vér tisztítására a vértisztító anyagok típusai és szerkezeti jellemzői, a gyártási folyamat, valamint a határfelületi kémiai adszorpciós tulajdonságok vagy mechanizmusok tekintetében. Ez a tanulmány értékes referenciaként szolgálhat egy olyan felhasználóbarát tisztítóeszköz elkészítéséhez, amely alkalmasabb a dialízises betegek klinikai vértisztítására.
Kulcsszavak
Vértisztítás, Vesepótló terápia, Műszaki bioanyagok, Adszorbens, Polimer kompozit membrán.

Kattintson ide, hogy megtudja, mi az a Cistanche
Bevezetés
Az urémiás toxinok gyakran felhalmozódnak a károsodott vesefunkciójú betegekben, beleértve azokat is, akiknek végstádiumú vesebetegsége (ESKD) van. Ez súlyos betegségekhez vezet, és a vesepótló kezelés az egyetlen megoldás a túlélésre. Számos tanulmány csökkent mortalitást és jobb életminőségről számolt be a vesebetegek körében; a kereslet azonban meghaladja a rendelkezésre állást, ahol az ESKD-betegek mindössze 25 százaléka kap vesét [1]. Világszerte a becslések szerint körülbelül 280 beteg egymillióan részesül rendszeres hemodialízisben vagy peritoneális dialízis kezelésben, miközben ezeknek az embereknek az ötéves túlélési ideje 13-60 százalékkal alacsonyabb, mint a hasonló korú lakosságé [1–3] . A népesség elöregedése, valamint a cukorbetegség és a magas vérnyomás megnövekedett prevalenciája miatt az ESKD előfordulása várhatóan emelkedni fog a következő évtizedekben [4]. Mi több, az urémiás retenciós oldott anyagok magas koncentrációban történő felhalmozódása a dializált betegeknél kedvezőtlen kimenetelekkel jár, beleértve a magas mortalitást és az általános egészséggel összefüggő alacsony életminőséget [5–8].
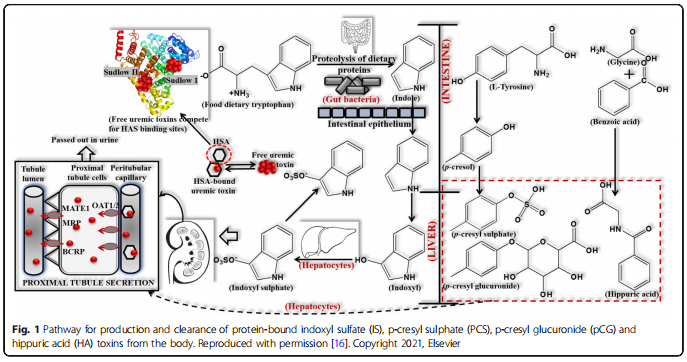
A kreatinin egy fő urémiás toxin, és a vérben való felhalmozódása egy sor toxikus tünetet okoz, amelyek csökkenthetik a veseműködést, és ennek következtében felgyorsíthatják a veseműködést [9]. A proteinhez kötött urémiás toxinok (PBUT) kis molekulák, amelyek elsősorban a transzportfehérjéhez, a vérben lévő humán szérumalbuminhoz kötődnek [10], és részt vesznek a reaktív oxigénfajták (ROS) létrehozásában [11]. Míg a PBUT-k különösen köztudottan káros/toxikus hatásokkal járnak, beleértve a szív- és érrendszeri betegségeket [12–14], a veseelégtelenség progresszióját [15] és a mortalitást [5], a vese-clearance mechanizmusuk és az urémiás patofiziológiában betöltött szerepük továbbra sem tisztázott [16]. ]. Gyakran p-krezil-szulfát (PCS), indoxil-szulfát (IS), 3- karboxi-4-metil-5-propil-2-furánpropionsav (CMPF) és indol{14 Az ecetsav (IAA) az urémia legmeghatározóbb biomarkerei, és a fehérjéhez kötött urémiás toxinok prototípusának tekinthetők, amelyek a plazmafehérjék több mint 90 százalékát képesek megkötni. Mind a négy PBUT-nak van aromás gyűrűje és ionos funkciós csoportja, és nem kovalens kötéseket, például Van der Waals-erőket és hidrogénkötéseket, valamint elektrosztatikus és hidrofób kölcsönhatásokat alakíthatnak ki [16]. A PBUT-k esetében egyensúly van mind a fehérjéhez kötött, mind a nem kötött formák között szekréciójukban és keringésükben, és a kötetlen toxinok inherens kiürülése nagymértékben függ a vese tubuláris szekréciójától a specifikus bazolaterális szerves anion transzportereken (OAT) keresztül. A fehérje PBUT-ok termelésének és kiürülésének útvonalát az 1. ábra mutatja [16]. Az urémiás toxicitás az endoteliális diszfunkcióhoz és az immunrendszer diszfunkciójához kapcsolódik, amely gyulladást okoz, és a veleszületett immuneffektorok aktiválódását okozza a Toll-szerű receptorok és gyulladásos citokinek bevonásával járó gyulladást elősegítő állapot kiváltása révén [14]. Így ezeknek a toxinoknak a vérből történő megfelelő eltávolítása növeli a dialízis hatékonyságát, ami viszont növeli az ESKD-s betegek túlélési arányát. A hemodialízis alapmechanizmusa a 2. ábrán látható. Azonban a felesleges metabolitok eliminációja hagyományos extracorporalis vesepótló terápiákkal szemipermeábilis porózus polimer membránokon keresztül jelenleg nem volt hatékony a klinikai alkalmazásban. Különösen a PBUT-okat nehéz eltávolítani hemodialízissel, mivel ezeknek a molekuláknak mindegyike rendelkezik aromás csoporttal és ionos funkciós csoporttal, amely lehetővé teszi a humán szérumalbumin számos adszorpciós helyéhez való kötődését [17–20]. Beszámoltak arról, hogy a nagy átfolyású hemodialízis során a PCS és az IS kevesebb mint 35 százalékos csökkenési aránya eliminálódik [11].
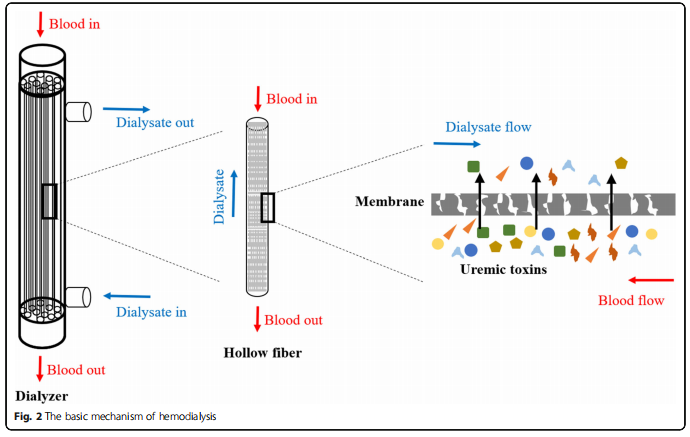
Tekintettel arra, hogy a hemodialízis a veseelégtelenség életfenntartó extracorporalis kezelése, ahol nagyszámú ESKD-beteg igényel hosszú távú dialízist, egyszerű és olcsó gyártási módszerekkel kell anyagokat készíteni. Bár a dialízis membránok hatékonysága és szelektivitása javult az elmúlt évtizedekben, a hagyományos dialíziskezelés továbbra is kényelmetlen, időigényes és költséges eljárás [21–23]. A közelmúltban számos orvosbiológiai vértisztító anyagot fejlesztettek ki a toxin eltávolítási sebességének növelésére, amelyek közül néhány olyan jellemzőkkel is rendelkezik, mint a kisebb toxicitás és az alacsony előállítási költség. Ebben a cikkben ezeket az eredményeket kategóriánként foglaljuk össze, hogy információkat nyújtsunk a továbbfejlesztett tulajdonságokkal rendelkező dialízis anyagokkal kapcsolatos további kutatásokhoz.

Cistanche tubulosa
Orvosbiológiai anyagok a toxinok eltávolításáraAdszorbensek
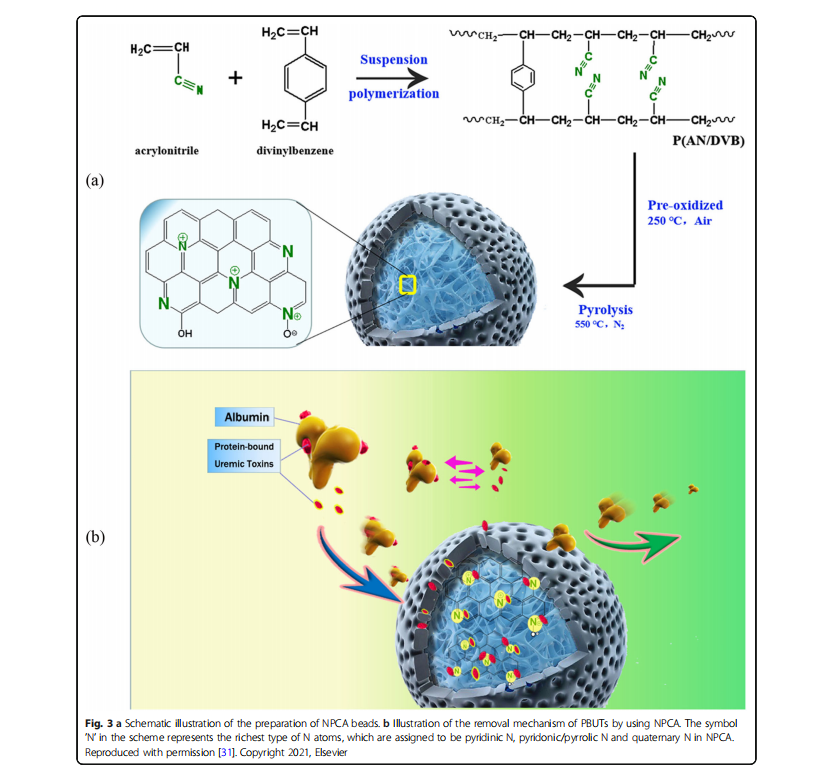
Az aktívszén (AC) és a zeolit két gyakori adszorbens, amelyet tisztítás során alkalmaznak az ultraszűrési tulajdonságok növelésére. Az AC hosszú múltra tekint vissza a méregtelenítő rendszerekben, mint adszorptív részecske, mivel sokféle oldott anyagot képes adszorbeálni [24–26]. Hatalmas pórusmérettel rendelkezik, de nem méretszelektív. Az AC nagy adszorpciós kapacitást mutat az urémiás toxinokhoz, de ezzel egyidejűleg más hasznos molekulákat is eltávolít. A részecskék átmérőjének csökkentése megvalósítható módja a külső felület növelésének, és ezáltal a hozzáférhető aktív helyek növelésének és a gyors kötődésnek. A por alakú aktívszén szuszpenziók felviteléhez azonban membránszűrőre van szükség, amely a szorbenseket szuszpendált állapotban tartja, és megakadályozza a részecskék vérrel való érintkezését, ami általában korlátozza a szorbens térfogatát, és elkerülhetetlenül a szorbensek alacsonyabb koncentrációját eredményezi [27]. Az AC-hez képest a szén nanocsövek (CNT) nagyobb felülettel, nagyobb méretaránnyal és jobb adszorpciós teljesítménnyel rendelkeznek az urémiás toxinokhoz, ezért alkalmasabb anyagnak tekinthetők egy nagyon hatékony vértisztító membrán kialakításához [28–30] . Liu et al. nitrogéntartalmú porózus szén adszorbens (NPCA) gyöngyök, amelyek további előnyökkel jártak a PBUT-k biztonságos és hatékony kiürülése szempontjából, és kielégítő in vitro hemokompatibilitást mutattak. Az NPCA-t térhálósított, porózus akrilnitril/divinilbenzol kopolimer gyöngyök pirolízisével állították elő (3a. ábra) [31]. Az NPCA gyöngyök a PBUT-ok (IS, PCS és IAA; 45 százalék, 44 százalék és 95 százalék) magasabb adszorpciós arányt mutattak, és ezzel egyenértékű adszorpciós teljesítményt mutattak a közepes molekulatömegű toxinokkal (PTH és IL) szemben{15}}. a humán plazmában a HA- 130/MG-150-hoz (a klinikán használt kereskedelmi adszorbenshez) képest. Az NPCA PBUT-eltávolító mechanizmusa az NPCA-n lévő nitrogén funkciós csoportok és a fehérjék közötti versengésnek tulajdonítható az elektrosztatikus kölcsönhatások révén létrejövő PBUT-kért, és nincs szoros kapcsolata a pórusszerkezettel (3b. ábra) [31].
Az amorf váltakozó áramtól eltérően a kristályos adszorbensek közvetlen szerkezeti jellemzést tesznek lehetővé, ami segíthet megérteni az adszorbens és a toxin közötti kölcsönhatásokat, ami kritikus fontosságú a kiváló adszorbens anyagok tervezésében. A zeolit az egyik legjobb timsó-szilikát, amelyet számos molekulaszitára alkalmaznak, és nagy ellenálló képességgel rendelkezik a kémiai és termikus folyamatokban [32]. A zeolitok nem mérgezőek, vizes oldatban stabilak és fiziológiás körülmények között nem bomlanak le. Ezen túlmenően a különböző típusú mikroporózus zeolitok különböző méretű csatornarendszerekkel rendelkeznek, amelyek szelektíven adszorbeálnak bizonyos urémiás toxinokat [33–36], és ezek megtalálhatók természetesen vagy szintetikusan előállíthatók. Ezek a tulajdonságok a zeolitokat potenciális anyaggá teszik a mesterséges vese alkalmazásokhoz. A zeolit részecskék mérete és alakja fontos a kreatinin-felvevő képesség szempontjából, amikor beépülnek a membránba [37, 38]. Például a mikrorészecskék jobban teljesítenek a kreatinin adszorpciójában, mint a nanorészecskék. Eközben a pálca nanorészecskékkel összehasonlítva a gömb alakú nanorészecskék jobb választás az elektrofonó polimer szálakba való beépítésre a kreatinin kiürülési sebességének javítása érdekében [37].

Cistanche kiegészítő
Wernet et al. az urémiás toxinok eliminációját vizsgálták különböző szerkezeti típusú zeolitok felhasználásával [33]. Arra a következtetésre jutottak, hogy a zeolitok adszorpciós tulajdonságai nemcsak a csatornák méretétől függenek, hanem az adszorbátumok és a zeolitrácsok közötti kölcsönhatásoktól is. Pontosabban, a zeolit szilikalit (MFI) a p-krezol erős adszorpcióját mutatja (körülbelül 60% p-krezol oldatban, amelynek koncentrációja közel van az urémiás betegekben tapasztaltakhoz), ami a csatornanyílás/méret hatásnak és a hidrogénkötési kölcsönhatásoknak tulajdonítható. Az adszorpció mechanizmusait a 4. ábra mutatja (pl. p-krezol adszorpciója szilikalit zeolitra) [39]. Az MFI-nek kevesebb az egyensúlyi ideje és magasabb a p-krezol adszorpciója, mint a cellulóz alapú membránok és a szintetikus membránok [39]. Emellett lehetőség van az oldatban lévő kreatinin 75 százalékának szelektív eltávolítására savas mordenittel (MOR), ami alapvetően az Ofunkcionális csoport és a MOR pórusokban jelenlévő Brønstedt helyek közötti elektrosztatikus kölcsönhatások következménye [33]. A húgysav magas adszorpciója az ioncserélt stilbiteken (STI), például a Ca-STI-n, a K-STI-n és a Na-STI-n, a kation és a poláris molekuláris kötés negatív atomja közötti elektrosztatikus kölcsönhatásnak tulajdonítható. Van azonban egy lehetséges mód az STI-k adszorpciós tulajdonságainak növelésére erős kovalens kölcsönhatások kialakításával, olyan kationok felhasználásával, amelyek affinitással rendelkeznek az urémiás toxinokhoz [33]. Bergé-Lefranc et al. továbbá bebizonyította, hogy a tiszta szilícium-dioxid MFI jobb p-krezol eltávolítási kapacitással rendelkezik, mint az aluminoszilikát MFI-k (Si/Al=30, a töltéseket H plusz, Na plusz, K plusz és Mg2 plusz kompenzálja) [34]. Azt találták, hogy az oldathoz képest a p-krezol affinitása a zeolitokhoz általában csökken a humán szérumban (amelyet dializált betegektől nyernek), mivel a fehérjék elzárták a pórusrendszert. Így a zeolitok csak az ultraszűrletben alkalmazhatók anélkül, hogy közvetlenül érintkeznének a szérumalbuminnal [35].

A fém-organikus váz (MOF) egyfajta új hibrid anyag, amely nagy termikus és kémiai stabilitással rendelkezik, és ultranagy porozitása és aktív helyei miatt hatékonyabbnak bizonyult, mint az AC vagy mezopórusos szilícium-dioxid anyagok [40–42] . A BET felületet és a belső MOF ketrecátmérőt pedig korábban a MOF-ok adszorpciós kapacitásának kulcsparamétereiként feltételezték [43]. A MOF fémionokból és szerves linkerekből áll, amelyek koordinátahatárokon keresztül 1D, 2D vagy 3D struktúrát alkotnak [40, 44]. A MOF-ok gyorsan elterjedtek a bioaktív vegyületek elválasztásában [45], a víztisztításban [46, 47], a gyógyszerszállításban [48] és a gázleválasztásban [49], de nem kizárólagosan. Mindazonáltal a MOF-ok mesterséges vese alkalmazásokban történő alkalmazása még mindig a korai szakaszban van. Ezenkívül a MOF-ok kivételes tartóssággal rendelkeznek, és a kristályos anyagok más osztályaitól eltérően szisztematikusan tanulmányozhatók és számos funkcióba beépíthetők [50].

Cistacnhe kivonat
Abdelhameed et al. beszámolt a Zr-alapú MOF egy típusáról, amelyet pamutszövet kompozitban termesztettek, és amely metanollal ultrahangos kezeléssel regenerálható, míg a kreatinin eltávolításának hatékonysága csak 16 százalékkal (98 százalékkal vs. 82 százalékkal) csökken három generációs ciklus után [ 51]. Ezt az in situ kompozitot közvetlenül formázták UiO-66-(COOH)2 előállítása nélkül, helyette 1,2,4,5- benzol-tetrakarbonsav-dianhidridet, cirkónium-tetrakloridot és pamutszövetet használtak [51]. Az UiO-66- (COOH)2@pamutszövet kompozit a MOF kötőhelyei és a kreatinin funkciócsoportjai közötti gyenge kölcsönhatások révén adszorbeálja a kreatinint. A reakciómechanizmust az 5. ábra szemlélteti. Emellett arról számoltak be, hogy az UiO-66 izovalens szubsztituensekkel, például -NH2, -OH és SO2H funkcionalizálása jelentősen javította az adszorpciós kapacitást a MOF elektronikus tulajdonságainak megváltoztatásával [52 , 53]. Klaudia et al. A H2BDC/H2BDC-NH2 arány megváltoztatásával és a modulált szintézis során sósav (HCl) hozzáadásával az aminocsoportok végső tartalmával változó UiO-66 anyagok sorozatát szintetizálta [52]. Megerősítették, hogy az UiO-66-NH2(75%) (75 mol% -aminocsoporttal) és az UiO-66-NH2(75% )12,5% HCl jobb adszorpciós kapacitást mutat a hippursav és a {{39} }indolecetsav, amely analóg adszorpciós kapacitást mutatott az NU-1000-hoz, eközben az elkészített UiO-66-NH2 továbbra sem mutatott citotoxikus hatást.

Kato et al. megfigyelték a krezil-szulfát adszorpciós viselkedését egy sor Zr6-alapú MOF-ban, változó topológiával, kapcsolódási lehetőséggel és linkerszerkezettel, beleértve az UiO-66, UiO-67, UiO-NDC, PCN{ {4}}OH, NU-901, NU-1000, NU-1010, NU-1200 és MOF-808 [50]. Ezek a cirkónium alapú MOF-ek hasonló felülettel és pórusmérettel rendelkeznek. Közülük az NU-1000 mutatja a legmagasabb toxineltávolítási hatékonyságot, ahol több mint 70 százaléka p-krezil-szulfát, 98 százaléka indoxil-szulfát és hippursav oldatban, valamint körülbelül 93 százaléka p-krezil-szulfát. , eltávolítható a humán szérum albuminból. Ez az erősen hidrofób adszorpciós helyeknek tudható be, amelyek két pirén linkerrel vannak szendvicsben, valamint a Zr6 csomópontokon lévő hidroxilcsoportok és az adszorbátumok ionos funkciós csoportjai közötti hidrogénkötésnek [50]. A p-krezil-szulfát két helye a NU-1000-on látható a 6. ábrán. Ez a két hely megközelítőleg azonos helyet foglal el, ahol elektrosztatikus kölcsönhatások lépnek fel a Zr6 csomópontokon lévő hidroxilcsoportokkal és π-π kölcsönhatások pirén alapú linkerekkel fontos tényezők az adszorpciós képességben. Cuchiaro et al. rámutatott, hogy az NU-1000 alkalmazása korlátozott, mivel kereskedelmi forgalomban nem kapható, és a vas kívánatos alternatívája a cirkóniumnak [43]. Cuchiaro et al. szintetizált MIL-100(Fe) és MOF-808, mindkettőnek ugyanaz a szerves linkereje a MOF-808-nak, de a MIL-100 (Fe) vasa miatt kevésbé mérgező -alapú fém csomópontok [43]. Azt találták, hogy a MIL-100(Fe) p-krezil-szulfát felvétele háromszor nagyobb, mint a MOF-808 esetében, ami kevésbé korrelált a BET felületével, a pórusablak méretével, a ketrec átmérőjével és a aromás szén a szerves linkerben, ami azt jelzi, hogy a fém-vas kölcsönhatások kedvezőbbek lehetnek a MIL-100(Fe)-ben, mint a MOF-808-ban.

A vese öntisztító képessége által inspirálva Chen et al. új adszorbenst javasoltak, az úgynevezett molekuláris imprinted polimer inverz opál részecskéket (MIPIOP) [54]. Itt a fluid környezetet arra használják, hogy megoldják az adszorbens anyagok és a célmolekulák közötti elégtelen érintkezés dilemmáját. A MIPIOP-ok egy halszálkás keverővel ellátott mikrofluidikus chipbe vannak beágyazva, és a skála könnyen erősíthető, hogy nagyszámú MIPIOP-t befogadjon a tisztításhoz. Ezen túlmenően a halszálkás csatornák kaotikus advekciót generálhatnak a folyadékban, és ezáltal javítják a keverési és adszorpciós hatékonyságot a cél biomolekulák és a MIPIOP-ok között. A MIPIOP-okat kombinált imprinting eljárással állítják elő (7. ábra). Először a szilícium-dioxid kolloid kristálygyöngyöket (SCCB) állították elő, majd az SCCB-k felületén lévő szilícium-dioxid nanorészecskék elektrosztatikus kölcsönhatás révén adszorbeálták a lizozimot. A következő lépés kitöltötte a lizozim-funkcionalizált SCCB-k szilícium-dioxid nanorészecskéi közötti űrt metakrilát zselatin (GelMA), polietilénglikol-diakrilát (PEGDA), karbamid és kreatinin előkeverékével. Ezután az SCCB-ket és a lenyomatmolekulákat, beleértve a lizozimet, a karbamidot és a kreatinint, eltávolítottuk a gél előtti polimerből. A kapott MIPIOP-ok felszínén több molekuláris kötőhellyel rendelkeznek a lizozim számára, míg a karbamid és a kreatinin belül találhatók. A MIPIOP-ok egyedi tulajdonságokkal rendelkeznek, és jó vérkompatibilitást mutatnak, és bebizonyosodott, hogy adszorpciós kapacitásuk stabilan megmarad ötszöri újrafelhasználás után [54]. Ezenkívül a rendkívül rendezett 3D porózus struktúráknak köszönhetően fotonikus sávrés tulajdonságokkal rendelkeznek, amelyek lehetővé teszik az adszorpciós állapot monitorozását és önjelentését.

A ciklodextrinek (CD-k) toroid alakú ciklikus oligoszacharidok, amelyek 6-8 D-glükóz egységekből ( , , ), hidrofil külsővel és viszonylag hidrofób belső üreggel rendelkeznek, amelyek különböző kis molekulatömegű lipofil vendégeket vagy makromolekulákat foglalhatnak magukba [55 , 56]. A csésze alakú -CD 7 glükóz egységből áll, és leggyakrabban a különféle hidrofób molekulák érzékeny felismerése miatt alkalmazzák, CD-vendég komplexet képezve. Li és mtsai. először javasolta térhálósított poli- -ciklodextrinek (PCD) hozzáadását a külső dializátor dializátumához az indoxil-szulfát (IS) tömegátviteli hatékonyságának javítása érdekében (8a. ábra) [56]. A PCD-t -CD és epiklórhidrin (ECH) közötti keresztkötéssel szintetizálták. Először NaOH-oldatban oldott -CD-t, majd ECH-t adtunk az elegyhez, majd 2 órán át 30 fokon kevertük. Az eredeti tanulmány szerint a PCD maximális kötőképessége az IS-hez körülbelül 45 mg g{19}}, és a PCD bevezetésével végzett szimulált dialíziskísérletben 21 százalékkal nőtt az eltávolítási sebesség. Az IS PCD-hez való kötődésének mechanizmusa az lehet, hogy az IS indolgyűrűje hidrofób kölcsönhatáson és hidrogénkötésen keresztül beépül a -CD üregébe [56]. Ez az új stratégia nem fejt ki negatív hatást a dialízis membránra, és biztonságos a klinikai alkalmazásban, mivel a PCD bizonyítottan alacsony hemolízis sebességgel rendelkezik, és nem képes áthaladni a membránon, hogy érintkezzen a vérrel (a polimer hidrodinamikai átmérője 9 nm). Li és mtsai. továbbá összehasonlította a poli- -ciklodextrinek, poli- - ciklodextrinek és poli- -ciklodextrinek adszorpciós kapacitását, valamint a poli- - ciklodextrinek a legjobb teljesítményt a maximális krezol-szulfát (PCS) megkötő kapacitással (263 mg g{29}}) [57]. Azt találták, hogy a PCS kiürülése a plazmában az egyszeri módban (8b. ábra) hatékonyabb, mint az újrahasznosított mód (96 százalék vs. 43 százalék), ami a plazma és a dializátum közötti PCS-koncentráció különbségének tulajdonítható a PCS. A plazmában lévő PCS-t (96%), hippursavat (98%) és kinolinsavat (97%) eltávolították PCD-vel kiegészített dializátumrendszerben, ami tovább világította a PCD széles spektrumú PBUT-eltávolító tulajdonságait [57].

Az MXének az átmeneti fémek kétdimenziós karbidjainak és nitrideinek családja, amelyek általános szerkezete Mn plusz 1XnTx (M egy korai átmenetifém, például Ti, V, Nb stb.; n plusz 1=1-3; X jelentése C és/vagy N; Tx a felületi végződéseket jelenti, például O, OH, F és/vagy Cl) [58, 59]. Az MXének a tulajdonságok egyedülálló kombinációjával rendelkeznek, köztük a funkcionalizált felületeknek köszönhetően hidrofilek, és a magas negatív zéta-potenciál miatt stabil kolloid oldatok vízben, és az elmúlt években alaposan kutatták őket az orvosbiológiai területen [58]. A Ti3C2Tx az MXenes első bejelentett és legtöbbet tanulmányozott tagja, és ismert, hogy hatékonyan adszorbeálja a karbamidot. A Ti3C2Tx-ről pedig a korábbi in vivo vizsgálatok erősen bizonyították, hogy viszonylag magas biokompatibilitással és alacsony biotoxicitással rendelkezik [60]. Zhao és munkatársai munkája során adszorbensként Ti3C2Tx-et (Ti3C2- F, Ti3C2-O, Ti3C2-OH, Ti3AlC2 prekurzorból 10 tömegszázalékos fluorsav felhasználásával állítanak elő) használtak. vizes oldatban, és a hagyományos aktív szénhez képest gyors adszorpciós sebességet és nagyobb adszorpciós kapacitást mutatott kreatinin és húgysav felé [59]. A Ti3C2Tx és a kreatinin közötti nagy affinitás az adszorpciós folyamatban a Ti3C2Tx hidrofil felületi végződéseinek és a kreatinin intrapartikuláris diffúziójának tulajdonítható a Ti3C2Tx réteg között. A húgysav adszorpciós folyamatában azonban a nagy affinitás a hidrogénkötésből (TiOH … N) és a van der Waals kölcsönhatásokból származhat. Sőt, figyelembe véve, hogy a Ti3C2Tx hatékonyan adszorbeálja a karbamidot, a kreatint és a húgysavat, valamint az elektrolit kationokat (K plus, Ca2 plus, Mg2 plus stb.) is elfoglalhatják a Ti3C2Tx aktív helyeit, Zhao et al. azt javasolta, hogy a Ti3C2Tx potenciálisan hatékony szorbensként használható a dializátum regenerálására. Újabban Wang et al. Ti3C2Tx nanolapot készített a maratott Ti3C2Tx légtelenített vízben ultrahangos kezeléssel történő delaminációjával, és először fedezte fel, hogy a Ti3C2Tx ultramagas eltávolító képessége IL felé-6, amely 13,4-szeres a hagyományos aktív szénnél és sokkal gyorsabb eltávolítási sebességet mutat [ 61]. Az adszorpció fő mechanizmusa az MXene és az IL-6 (TI-X … HNC=O) közötti hidrogénkötés kialakulása, valamint az IL-6 immobilizálása a sejtek felületén. MXene nanolapok.
Cistanche kapszula
Következtetés
Összegezve összefoglaltuk az elmúlt években jelentett új vértisztítási bioanyagot. Ezeket a bioanyagokat nagyjából három kategóriába sorolták, beleértve az adszorbenseket, a polimer kompozit membránokat és a nanoanyagokat. Adszorbenseket, például zeolitokat, aktív szenet és CTN-ket általában beépítenek a polimer anyagokba az ultraszűrési kapacitás növelése érdekében. Ha az adszorpciós részecskéket szétszórják a polimer mátrixban, az urémiás toxinok eltávolítási hatékonysága jelentősen javítható az urémiás retenciós oldott anyagok adszorpciójának és diffúziójának kombinálásával, amelyet MMM és f-CNT/PES kompozit membránokkal kapcsolatos vizsgálatokban igazoltak. A nagy felület és a porozitás miatt a nanoanyagok és a MOF-ek egyaránt kedvező adszorpciós képességet mutatnak. Ezenkívül a polimer nanoszálak előállítása költséghatékony, és a Zr-alapú MOF-ek újrafelhasználhatósága jó.
A permeáció a hemodiafiltrációhoz használt membrán létfontosságú tulajdonsága, mivel a toxinok alacsony eltávolítási sebessége miatt a betegek hosszú ideig tartó dialízist szenvednek el, ami magasabb költséggel jár. Ha a szabad toxin koncentrációját a dializátum oldalán alacsony szinten tartják, folyamatos diffúziós hajtóerő van a hemodializátor teljes hosszában, különösen a PBUT-ok esetében [130, 131]. Amint ebben a cikkben említettük, a nagy felületű és porozitású anyagok ígéretes jelöltek hemodialízis membránok előállítására. Az adszorpciós részecskék polimer membránmátrixba való beágyazása szintén hatékony módszer az urémiás toxinok hatékonyabb kiürülési sebességének elérésére, ami a koncentrációkülönbség fenntartásának köszönhető. Vannak olyan adszorbensek is, amelyek adszorpciós képessége kevésbé korrelál a pórusszerkezettel, például az NPCA gyöngyök. Ezért kulcsfontosságú az adszorbens és urémiás toxinok molekulaszerkezetének, valamint a bennük lévő kölcsönhatások elemzése.
A dialízis egy hosszú távú és életben tartó kezelés az ESKD-s betegek számára, és közel 500 liter csapvíz szükséges ahhoz, hogy tiszta dialízisvizet kapjunk egyetlen hemodialízis alkalmával, ami költség és energiafogyasztás tekintetében is magas [132]. Ezért a dialízis anyag egyszerű és olcsó gyártási módja nagy jelentőséggel bír a klinikai alkalmazása szempontjából. Ezenkívül a víz pangása okozta mikrobiológiai biofilm akkor is képződik, ha a csőrendszer nem megfelelő vagy a gép nem megfelelő karbantartása [133, 134]. A víztisztító rendszerben a baktériumok szaporodása és lízise, így a pirogének bekerülhetnek a betegek vérébe, ami mikrogyulladásos állapotot okoz, ami kardiovaszkuláris mellékhatásokhoz vagy akut mellékhatásokhoz, például lázhoz és izomgörcsökhöz vezet [133–139] . Számos szorbens rendszerről számoltak be az endotoxinok (pl. lipopoliszacharidok) eltávolítására, mint például funkcionalizált nanorészecskék [140], aktív szén [26, 141], PS-poli (etilénglikol) kopolimer (PS-PEG) és fehérítő hozzáadása. sterilizálás [133]. Ezenkívül az MMM kiváló endotoxineltávolítást kínál, és biztonsági gátként működik, amely elkerüli a gyulladásos reakciókat anélkül, hogy csökkentené az urémiás toxinok eltávolítását [71]. Általánosságban elmondható, hogy a hosszú távú és magas ultraszűréssel, kedvező biokompatibilitással és költséghatékony gyártási módszerekkel rendelkező bioanyagok ideális jelöltek a vértisztításhoz. Még ha a jelen áttekintésben említett új bioanyagok javított adszorpciós kapacitással és biokompatibilitással is rendelkeznek, még mindig sok a tennivaló az anyagok olyan módosítására összpontosítva, hogy alkalmasak legyenek klinikai alkalmazásra.
Hivatkozások
1. Webster AC, Nagler EV, Morton RL, Masson P. Krónikus vesebetegség. Gerely. 2017;389(10075):1238–52.
2. Tonelli M, Wiebe N, Knoll G, Bello A, Browne S, Jadhav D és mások. Szisztematikus áttekintés: a veseátültetés összehasonlítása a dialízissel a klinikailag releváns eredményekben. Am J transzplantáció. 2011;11(10):2093–109.
3. Nordio M, Limido A, Maggiore U, Nichelatti M, Postorino M, Quintalani G. Hosszú távú dialízissel kezelt betegek túlélése az általános populációhoz képest. Am J Kidney Dis. 2012;59(6):819–28.
4. Liyanage T, Ninomiya T, Jha V, Neal B, Patrice HM, Okpechi I és mások. A végstádiumú vesebetegség kezeléséhez való hozzáférés világszerte: szisztematikus áttekintés. Gerely. 2015;385(9981):1975–82.
5. Bammens B, Evenepoel P, Keuleers H, Verbeke K, Vanrenterghem Y. A proteinhez kötött retenciós oldott p-krezol szabad szérumkoncentrációi előre jelzik a hemodializált betegek mortalitását. Kidney Int. 2006;69(6):1081–7.
6. Cheung AK, Rocco MV, Yan G, Leypoldt JK, Levin NW, Greene T és társai. A szérum béta{1}} mikroglobulinszintjei előre jelzik a dializált betegek mortalitását: az otthoni vizsgálat eredményei. J Am Soc Nephrol. 2006;17(2):546–55.
7. Ito S, Osaka M, Higuchi Y, Nishijima F, Ishii H, Yoshida M. Az indoxil-szulfát leukocita-endothel kölcsönhatásokat indukál a szelekció fokozása révén. J Biol Chem. 2010;285(50):38869–75.
8. Duranton F, Cohen G, De Smet R, Rodriguez M, Jankowski J, Vanholder R és mások. Az urémiás toxinok normál és kóros koncentrációja. J Am Soc Nephrol. 2012;23(7):1258–70.
9. Panasyuk-Delaney T, Mirsky VM, Wolfbeis OS. Kapacitív kreatinin-érzékelő, amely egy fényképezett molekuláris lenyomatú polimeren alapul. Elektroanalízis. 2002;14(3):221–4.
10. Vanholder R, De Smet R, Glorieux G, Argiles A, Baurmeister U, Brunet P és mások. Az urémiás toxinok áttekintése: osztályozás, koncentráció és egyének közötti változékonyság. Kidney Int. 2003;63(5):1934–43.
11. Itoh Y, Ezawa A, Kikuchi K, Tsuruta Y, Niwa T. Protein-bound urémiás toxinok hemodializált betegekben folyadékkromatográfiával/tandem tömegspektrometriával mérve és hatásuk az endothel ros termelésére. Anal Bioanal Chem. 2012;403(7):1841–50.
12. Lin CJ, Pan CF, Liu HL, Chuang CK, Jayakumar T, Wang TJ és mások. A fehérjéhez kötött urémiás toxinok szerepe a perifériás artériás betegségekben és a hemodializált betegek érelégtelenségében. Érelmeszesedés. 2012;225(1):173–9.
13. Wu PH, Lin YT, Chiu YW, Baldanzi G, Huang JC, Liang SS és mások. Az indoxil-szulfát és a p-krezil-szulfát kapcsolata a kardiovaszkuláris célfehérjékkel hemodializált betegekben. Sci Rep. 2021;11(1):3786.
14. Falconi CA, Junho CVDC, Fogaça-Ruiz F, Vernier ICS, Da Cunha RS, Stinghen AEM és mások. Urémiás toxinok: riasztó veszély a szív- és érrendszerre nézve. Front Physiol. 2021;12:686249.
15. Wu IW, Hsu KH, Lee CC, Sun CY, Hsu HJ, Tsai CJ és mások. A P-krezil-szulfát és az indoxil-szulfát előrejelzi a krónikus vesebetegség progresszióját. Nephrol Dial Transplant. 2011;26(3):938–47.
16. Daneshamouz S, Eduok U, Abdelrasoul A, Shoker A. Protein-bound urémiás toxinok (PBUTS) krónikus vesebetegségben (CKD) szenvedő betegeknél: termelési út, kihívások és a renális PBUTS clearance terén elért legújabb eredmények. NanoImpact. 2021;21:100299.
17. Ghuman J, Zunszain PA, Petitpas I, Bhattacharya AA, Otagiri M, Curry S. A humán szérumalbumin gyógyszerkötő-specifitásának strukturális alapjai. J Mol Biol. 2005;353(1):38–52.
18. Brettschneider F, Toelle M, von der Giet M, Passlick-Deetjen J, Steppan S, Peter M és munkatársai. Fehérjéhez kötött, hidrofób urémiás toxinok eltávolítása kombinált frakcionált plazma elválasztási és adszorpciós technikával. Artif orgonák. 2013;37(4):409–16.
19. Berge-Lefranc D, Chaspoul F, Cerini C, Brunet P, Gallice P. Az indoxil-szulfát kölcsönhatása humán szérumalbuminnal és kompetitív kötődés p-krezil-szulfáttal termodinamikai vizsgálata. J Therm Anal Calorim. 2014;115(3):2021–6.
20. Yu S, Schuchardt M, Toelle M, van der Giet M, Zidek W, Dzubiella J és munkatársai. Az emberi szérum albumin kölcsönhatása urémiás toxinokkal: termodinamikai vizsgálat. RSC Adv. 2017;7(45):27913–22.
21. Baboolal K, McEwan P, Sondhi S, Spiewanowski P, Wechowski J, Wilson K. A vesedialízis költsége az Egyesült Királyságban--egy többközpontú tanulmány. Nephrol Dial Transplant. 2008;23(6):1982–9.
22. Harris A, Cooper BA, Li JJ, Bulfone L, Branley P, Collins JF és mások. A dialízis korai megkezdésének költséghatékonysága: randomizált, kontrollált vizsgálat. Am J Kidney Dis. 2011;57(5):707–15.
23. Young BA, Chan C, Blagg C, Lockridge R, Golper T, Finkelstein F és mások. Hogyan lehet legyőzni az akadályokat és létrehozni egy sikeres otthoni HD programot. Clin J Am Soc Nephrol. 2012;7(12):2023–32.
24. Dinh DC, Recht NS, Hostetter TH, Meyer TW. A bevont szén hemoperfúzió a fehérjéhez kötött oldott anyagok korlátozott kiürülését biztosítja. Artif orgonák. 2008; 32(9):717–24.
25. Ash SR. Szorbensek az urémia kezelésében: rövid történelem és nagy jövő. Semin Dial. 2009;22(6):615–22.
26. Gun'Ko VM, Betz WR, Patel S, Murphy MC, Mikhalovsky SV. Lipopoliszacharid adszorpciója szénszitákon. Szén. 2006;44(7):1258–62.
27. Ash SR, Sullivan TA, Carr DJ. Szorbens szuszpenziók vs. Szorbens oszlopok extracorporalis méregtelenítéshez májelégtelenségben. Ott Apher Dial. 2006;10(2):145–53.
28. Ye C, Gong Q, Lu F, Liang J. Adsorption of uraemic toxins on carbon nanotubes. Szept Purif Technol. 2007;58(1):2–6.
29. Lu C, Su F. Természetes szerves anyagok adszorpciója szén nanocsövekkel. Szept Purif Technol. 2007;58(1):113–21.
30. Spitalsky Z, Tasis D, Papagelis K, Galiotis C. Szén nanocső-polimer kompozitok: kémia, feldolgozás, mechanikai és elektromos tulajdonságok. Prog Polym Sci. 2010;35(3):357–401.
31. Liu Y, Peng X, Hu Z, Yu M, Fu J, Huang Y. Fabrication of a novel nitrogen-containing porous carbon adsorbent for protein-bound urémiás toxinok eltávolítása. Mater Sci Eng C Mater Biol Appl. 2021;121:111879.
32. Soldatkin OO, Soy E, Errachid A, Jaffrezic-Renault N, Akata B, Soldatkin AP és társai. Zeolit/enzim nanobiokompozitok összetételének hatása az ionszelektív térhatású tranzisztorokon alapuló karbamid bioszenzor analitikai jellemzőire. Sens Lett. 2011;9(6SI):2320–6.
33. Wernert V, Schäf O, Ghobarkar H, Denoyel R. A zeolitok adszorpciós tulajdonságai mesterséges vese alkalmazásokhoz. Micropor Mesopor Mat. 2005;83(1): 101–13.
34. Bergé-Lefranc D, Pizzala H, Paillaud JL, Schäf O, Vagner C, Boulet P, et al. Kis urémiás toxin molekulák adszorpciója mfi típusú zeoliton vizes oldatból. Adszorpció. 2008;14(2):377–87.
35. Bergé-Lefranc D, Vagner C, Calaf R, Pizzala H, Denoyel R, Brunet P és társai. A fehérjéhez kötött urémiás toxin p-krezol in vitro eliminációja mfi típusú zeolitokkal. Micropor Mesopor Mat. 2012;153:288–93.
36. Namekawa K, Tokoro Schreiber M, Aoyagi T, Ebara M. Zeolit–polymer kompozit nanoszálak gyártása urémiás toxinok eltávolítására veseelégtelenségben szenvedő betegekből. Biomater Sci-Uk 2014;2(5):674–9.
37. Lu L, Chen C, Samarasekera C, Yeow JTW. A zeolit alakjának és részecskeméretének hatása az urémiás toxin porként és töltőanyagként való adszorbeálására való képességére a membránokban. J Biomed Mater Res B Appl Biomater. 2017;105(6):1594–601.
38. Tantekin-Ersolmaz SB, Atalay-Oral C, Tatlier M, Erdem-Senatalar A, Schoeman B, Sterte J. A zeolit részecskeméret hatása a polimer zeolit kevert mátrix membránok teljesítményére. J Membrane Sci. 2000;175(2):285–8.
39. Wernert V, Schäf O, Faure V, Brunet P, Dou L, Berland Y és társai. Az urémiás toxin p-krezol adszorpciója hemodialízis membránokra és mikroporózus adszorbens zeolit szilikalitra. J Biotechnol. 2006;123(2):164–73.
40. Furukawa H, Cordova KE, O'Keeffe M, Yaghi OM. Fém-szerves vázszerkezetek kémiája és alkalmazásai. Tudomány. 2013;341(6149):974.
41. Haque E, Jun JW, Jhung SH. Metilnarancs és metilénkék adszorpciós eltávolítása vizes oldatból fém-szerves vázanyaggal, vas-tereftaláttal (mof-235). J Hazard Mater. 2011;185(1):507–11.
42. Fletcher AJ, Thomas KM, Rosseinsky MJ. Fém-szerves vázanyagok rugalmassága: hatása a szorpciós tulajdonságokra. J Solid State Chem. 2005;178(8):2491–510.
43. Cuchiaro H, Thai J, Schaffner N, Tuttle RR, Reynolds M. Exploring the parameter space of p-cresyl sulfate adsorption in metal-organic frameworks. ACS Appl Mater interfészek. 2020;12(20):22572–80.
44. Tan J, Civalleri B. Fém-szerves keretek és hibrid anyagok: az alapoktól az alkalmazásokig. Crystengcomm. 2015;17(2):197–8.
45. Abdelhameed RM, Abdel-Gawad H, Taha M, Hegazi B. Bioaktív chamazulene szétválasztása kamilla kivonatból fém-szerves keret segítségével. J Pharmaceut Biomed. 2017;146:126–34.
46. Mon M, Bruno R, Ferrando-Soria J, Armentano D, Pardo E. Fémorganikus kerettechnológiák a víz helyreállításához: a fenntartható ökoszisztéma felé. J Mater Chem A. 2018;6(12):4912–47.
47. Abdelhameed RM, Abdel-Gawad H, Elshahat M, Emam HE. Cu–btc@cotton kompozit: etionos rovarölő szer tervezése és eltávolítása a vízből. RSC Adv. 2016;6(48):42324–33.
48. Huxford RC, Della Rocca J, Lin W. Metal-organic frameworks as potencial drug carriers. Curr Opin Chem. Biol. 2010;14(2):262–8.
49. Rodenas T, Luz I, Prieto G, Seoane B, Miro H, Corma A és mások. Fém-szerves váz nanolemezek polimer kompozit anyagokban gázleválasztáshoz. Nat Mater. 2015;14(1):48–55.
50. Kato S, Otake K, Chen H, Akpinar I, Buru CT, Islamoglu T és mások. Cirkónium alapú fém-szerves keretek a fehérjéhez kötött urémiás toxin eltávolítására a humán szérumalbuminból. J Am Chem Soc. 2019;141(6):2568–76.
51. Abdelhameed RM, Rehan M, Emam HE. A zr alapú mof@cotton szövet kompozit figurája a lehetséges vese alkalmazáshoz. Carbohyd Polym. 2018; 195:460–7.
52. Dymek K, Kurowski G, Kuterasinski L, Jedrzejczyk R, Szumera M, Sitarz M, et al. Hatékony auto-66 fém-szerves keretek keresése mesterséges vese alkalmazásához. ACS Appl Mater Inter. 2021;13(38):45149–60.
53. Zhu J, Wu L, Bu Z, Jie S, Li B. Polyethyleneimine-modified UiO-66-nh2 (zr) metal-organic frameworks: Preparation and enhanced co2 selective adsorption. ACS Omega. 2019;4(2):3188–97.
54. Chen H, Bian F, Sun L, Zhang D, Shang L, Zhao Y. Hierarchikusan molekuláris lenyomatú porózus részecskék biomimetikus vesetisztításhoz. Adv Mater. 2020; 32(52):2005394.
55. Mejia-Ariza R, Grana-Suarez L, Verboom W, Huskens J. Cyclodextrin-based supramolecular nanopartticles for biomedical applications. J Mater Chem B. 2017;5(1):36–52.
56. Li J, Han L, Liu S, He S, Cao Y, Xie J et al. Indoxil-szulfát eltávolítása vízoldható policiklodextrinekkel dialízis során. Colloid Surface B. 2018;164:406–13.
57. Li J, Han L, Xie J, Liu S, Jia L. Multi-sites poly cyclodextrin adsorbens for remove of protein-bound urémiás toxinok kombinálva hemodialízissel. Carbohyd Polym. 2020;247:116665.
58. Gogotsi Y, Anasori B. A mxének felemelkedése. ACS Nano. 2019;13(8):8491–4.
59. Zhao Q, Seredych M, Precetti E, Shuck CE, Harhay M, Pang R és munkatársai. Urémiás toxinok adszorpciója ti3c2tx men segítségével a dializátum regenerálására. ACS Nano. 2020;14(9):11787–98.
60. Dai C, Lin H, Xu G, Liu Z, Wu R, Chen Y. Biocompatibilis 2d titanium carbide (mxenes) kompozit nanosheets for ph-responsive mri-guided tumor hyperthermia. Chem. Mater. 2017; 29(20):8637–52.
61. Wang T, Sun X, Guo X, Zhang J, Yang J, Tao S és mások. Ultrahatékonyan csillapító citokinvihar ti (3) c (2) t (x) mxén használatával. Kis módszerek. 2021;5(5): e2001108.
62. Tian H, Tang Z, Zhuang X, Chen X, Jing X. Biológiailag lebomló szintetikus polimerek: előállítás, funkcionalizálás és orvosbiológiai alkalmazás. Prog Polym Sci. 2012;37(2):237–80.
63. Weber V, Linsberger I, Hauner M, Leistner A, Leistner A, Falkenhagen D. Neutral styrene-divinylbenzole copolymers for adsorption of toxins in májelégtelenség. Biomakromolekulák. 2008;9(4):1322–8.
64. Jiang X, Xiang T, Xie Y, Wang R, Zhao W, Sun S et al. Funkcionális poliéterszulfon részecskék a bilirubin eltávolítására. Journal of Materials Science: Materials in Medicine 2015;27(2):28.
65. Lu L, Samarasekera C, Yeow JTW. Elektrofonású poliakrilnitril (PAN)-zeolit nanoszálas membránok kreatinin adszorpciós képessége potenciális mesterséges vese alkalmazásokhoz. J Appl Polym Sci 2015;132(34): 42418- 26.
66. Lu L, Yeow JTW. Indoxil-szulfát adszorpciós vizsgálata zeolitok és poliéterszulfon-zeolit kompozit membránok segítségével. Mater Design. 2017;120: 328–35.
67. Tijink MS, Wester M, Sun J, Saris A, Bolhuis-Versteeg LA, Saiful S et al. Egy új megközelítés a vértisztításhoz: vegyes mátrixú membránok, amelyek egy lépésben kombinálják a diffúziót és az adszorpciót. Acta Biomater. 2012;8(6):2279–87.
68. Tijink MSL, Wester M, Glorieux G, Gerritsen KGF, Sun J, Swart PC és mások. Vegyes mátrixú üreges rostos membránok fehérjéhez kötött toxinok eltávolítására az emberi plazmából. Bioanyagok. 2013;34(32):7819–28.
69. Pavlenko D, van Geffen E, van Steenbergen MJ, Glorieux G, Vanholder R, Gerritsen KGF et al. Az új alacsony fluxusú kevert mátrix membránok kiválóan eltávolítják a fehérjéhez kötött toxinokat az emberi plazmából. Sci Rep 2016;6:34429.
70. Geremia I, Pavlenko D, Maksymow K, Rueth M, Lemke HD, Stamatialis D. Ex vivo értékelése a kevert mátrix hemodialízis membránok vérkompatibilitásának. Acta Biomater. 2020;111:118–28.
71. Geremia I, Bansal R, Stamatialis D. Vegyes mátrixú hemodialízis membrán in vitro vizsgálata endotoxin-mentes dializátum eléréséhez, kombinálva az urémiás toxinok magas eltávolításával az emberi plazmából. Acta Biomater. 2019;90:100–11.
72. Nie C, Ma L, Xia Y, He C, Deng J, Wang L és mások. Új, heparint utánzó polimer ecsettel oltott szén nanocső/pes kompozit membránok a biztonságos és hatékony vértisztítás érdekében. J Membrane Sci. 2015;475:455–68.
73. Zhang Y, Lim CT, Ramakrishna S, Huang Z. A polimer nanoszálak legújabb fejlesztése orvosbiológiai és biotechnológiai alkalmazásokhoz. J Mater Sci Mater Med. 2005;16(10):933–46.
74. Ramakrishna S, Fujihara K, Teo W, Yong T, Ma Z, Ramaseshan R. Electrospun nanofibers: solving global problems. Mater Today. 2006;9(3):40–50.
75. Huang Z, Zhang YZ, Kotaki M, Ramakrishna S. A polimer nanoszálak elektrofonással és nanokompozitokban való alkalmazásaik áttekintése. Compos Sci Technol. 2003;63(15):2223–53.
76. Fu GD, Xu LQ, Yao F, Zhang K, Wang XF, Zhu MF és társai. Intelligens nanoszálak kombinált élő gyökös polimerizációból, "kattintásos kémiából" és elektrofonásból. ACS Appl Mater Inter. 2009;1(2):239–43.
77. Kim Y, Ebara M, Aoyagi T. Intelligens nanoszálas háló, amely befogja és felszabadítja a sejteket. Angew Chem Int. Szerk. 2012;51(42):10537–41.
78. Wang XY, Drew C, Lee SH, Senecal KJ, Kumar J, Samuelson LA. Elektrospinning technológia: újszerű megközelítés az érzékelők alkalmazásához. J Macromol Sci Pure Appl Chem. 2002; A39(10):1251–8.
79. Barhoum A, Pal K, Rahier H, Uludag H, Kim IS, Bechelany M. Nanoszálak, mint új generációs anyagok: a fonástól és a nanoszálas gyártási technikáktól a feltörekvő alkalmazásokig. App Mater ma. 2019;17:1–35.
80. Peh P, Lim NSJ, Blocki A, Chee SML, Park HC, Liao S és mások. Különféle bioaktív vegyületek egyidejű szállítása kevert elektrofonású rostokból a bőrsebek gyógyulásához. Bioconjugate Chem. 2015;26(7):1348–58.
81. Qi R, Guo R, Shen M, Cao X, Zhang L, Xu J et al. Electrospun poli (tej-ko-glikolsav)/halloysite nanocső kompozit nanoszálak a gyógyszer kapszulázásához és nyújtott hatóanyag-leadáshoz. J Mater Chem. 2010;20(47):10622–9.
82. Salalha W, Kuhn J, Dror Y, Zussman E. Baktériumok és vírusok kapszulázása electrospun nanofibresben. Nanotechnológia. 2006;17(18):4675–81.
83. Luo Y, Nartker S, Miller H, Hochhalter D, Wiederoder M, Wiederoder S et al. Elektrofonású nanoszálak felületi funkcionalizálása pl. Coli o157:h7 és testsejtek közvetlen töltésű transzfer bioszenzorban. Biosens Bioelectron. 2010;26(4):1612–7.
84. Esmaeili A, Haseli M. Hőre lágyuló karboxi-metil-cellulóz/poli(etilén-oxid) nanoszálak elektrofonása gyógyszer-kibocsátó rendszerekben való felhasználáshoz. Mat Sci Eng C-Mater. 2017;77:1117–27.
85. Han D, Steckl AJ. Triaxiális elektrofonású nanoszálas membránok a funkcionális molekulák szabályozott kettős felszabadulásához. ACS Appl Mater Inter. 2013;5(16):8241–5.
86. Bahramimehr F, Esmaeili A. Hibrid nanoszál alapú /pan/fe3o4/zeolit/csalán növényi kivonat/ureáz és deformált koaxiális természetes polimer előállítása a toxicitás csökkentésére a dializált betegek vérében. J Biomed Mater Res A. 2019;107(8):1736–43.
87. Irfan M, Idris A, Yusof NM, Khairuddin NFM, Akhmal H. Nano-hibrid f-mwcnt/pvp90/pes hemodialízis membránok felületének módosítása és teljesítménynövelése. J Membrane Sci. 2014;467:73–84.
88. Niyogi S, Hamon MA, Hu H, Zhao B, Bhowmik P, Sen R et al. Egyfalú szén nanocsövek kémiája. Accounts Chem Res. 2002;35(12):1105–13.
89. Raravikar NR, Schadler LS, Vijayaraghavan A, Zhao Y, Wei B, Ajayan PM. Vastagságra igazított szén nanocső-polimer kompozit filmek szintézise és jellemzése. Chem. Mater. 2005;17(5):974–83.
90. Valcárcel M, Cárdenas S, Simonet BM, Moliner-Martínez Y, Lucena R. Carbon nanostructures as sorbent materials in analytical process. TrAC Trends Analyt Chem. 2008;27(1):34–43.
91. Tsuge M, Takahashi K, Kurimoto R, Fulati A, Uto K, Kikuchi A és mások. Vízelnyelő nanoszálas hálók gyártása a felesleges víz hatékony eltávolítása érdekében veseelégtelenségben szenvedő betegekből. Rostok. 2019;7(5):39.
92. Khan I, Saeed K, Khan I. Nanorészecskék: tulajdonságok, alkalmazások és toxicitások. Arab J Chem. 2019;12(7):908–31.
93. Wang L, Zhang Y, Li Y, Chen J, Lin W. Az akut vesesérülések terápiájában használt mesterséges nanoanyagok legújabb eredményei. Nano Res. 2021;14(4):920–33.
94. Stamopoulos D, Bouziotis P, Benaki D, Kotsovassilis C, Zirogiannis PN. A nanobiotechnológia hasznosítása a hemodialízisben: homocisztein ál-dialízis kísérletei. Nephrol Dial Transplant. 2008;23(10):3234–9.
95. Ma Y, Cai F, Li Y, Chen J, Han F, Lin W. A nanorészecskék alkalmazásának áttekintése a krónikus vesebetegség diagnosztizálásában és kezelésében. Bioact Mater. 2020;5(3):732–43.
96. Cheah W, Ishikawa K, Othman R, Yeoh F. Nanoporous biomaterials for urémiás toxin adszorpciója mesterséges veserendszerekben: áttekintés. J Biomed Mater Res B Appl Biomater. 2017;105(5):1232–40.
97. Abidin MNZ, Goh PS, Ismail AF, Said N, Othman MHD, Hasbullah H és mások. Erősen adszorpciós képességű oxidált keményítő nanorészecskék a karbamid hatékony eltávolításához. Carbohyd Polym. 2018;201:257–63.
98. Cabello-Alvarado C, Andrade-Guel M, Pérez-Alvarez M, Cadenas-Pliego G, Cortés-Hernández DA, Bartolo-Pérez P, et al. Változó frekvenciájú ultrahangos sugárzással aminocsoportokkal módosított grafén nanolemezkék az urémiás toxinok potenciális adszorpciójára. NanoanyagokBasel. 2019;9(9):1261.
99. Andrade-Guel M, Ávila-Orta CA, Cadenas-Pliego G, Cabello-Alvarado CJ, Pérez-Alvarez M, Reyes-Rodríguez P, et al. Nylon 6/módosított korom nanokompozitok szintézise húgysavadszorpcióban történő alkalmazásra. Anyagok. 2020;13(22):5173.
100. Korsvik C, Patil S, Seal S, Self WT. Szuperoxid-diszmutáz-utánzó tulajdonságok, amelyeket az üresedési céllal tervezett cérium-nanorészecskék mutatnak. Chem. Commun. 2007; 10:1056–8.
101. Pirmohamed T, Dowding JM, Singh S, Wasserman B, Heckert E, Karakoti AS és mások. A nanoceriumok redox állapottól függő kataláz mimetikus aktivitást mutatnak. Chem. Commun. 2010;46(16):2736–8.
102. Xue Y, Luan Q, Yang D, Yao X, Zhou K. Közvetlen bizonyíték a cérium-oxid nanorészecskék hidroxil gyökfogó aktivitására. J. Phys. Chem. C. 2011; 115(11):4433–8.
103. Ni D, Wei H, Chen W, Bao Q, Rosenkrans ZT, Barnhart TE és munkatársai. A cérium nanorészecskék találkoznak a máj ischaemia-reperfúziós sérülésével: a tökéletes tökéletlenség. Adv Mater. 2019;31(40):1902956.
104. Fleming RE, Ponka P. Iron overload in human disease. New Engl J Med. 2012;366(4):348–59.
105. Hamilton JL, Kizhakkedathu JN. Polimer nanohordozók szisztémás vastúlterhelés kezelésére. Mol Cell Ther. 2015; 3:3.
106. Kang H, Han M, Xue J, Baek Y, Chang J, Hu S et al. Vesenálisan kitisztítható nano kelátképzők vastúlterhelés kezelésére. Nat Commun 2019;10(1):5134.
107. Mobarra N, Shanaki M, Ehteram H, Nasiri H, Sahmani M, Saeidi M és mások. Áttekintés a vaskelátképzőkről a vastúlterhelési szindrómák kezelésében. Int J Hematol Oncol Stem Cell Res. 2016;10(4):239–47.
108. Shapiro SM. Bilirubin toxicitás a fejlődő idegrendszerben. Pediatr Neurol. 2003;29(5):410–21.
109. Peng Z, Yang Y, Luo J, Nie C, Ma L, Cheng C és mások. Nanoszálas polimer gyöngyök aramid szálakból a hatékony bilirubin eltávolításhoz. Biomater Sci-Uk. 2016;4(9):1392–401.
110. Yang M, Cao K, Sui L, Qi Y, Zhu J, Waas A és munkatársai. Az aramid nanoszálak diszperziói: új nanoméretű építőelem. ACS Nano. 2011;5(9):6945–54.
111. Zhao C, Xue J, Ran F, Sun S. Modification of polyethersulfone membránok - a módszerek áttekintése. Prog Mater Sci. 2013;58(1):76–150.
112. Goldberg AL. A fehérjék lebontása és védelem a rosszul hajtogatott vagy sérült fehérjék ellen. Természet. 2003;426(6968):895–9.
113. Furie B, Furie Kr. e. A betegség mechanizmusai: a trombusképződés mechanizmusai. New Engl J Med. 2008;359(9):938–49.
114. Arepally GM. Heparin által kiváltott thrombocytopenia. Vér. 2017;129(21):2864–72.
115. Ratner BD. Vérkompatibilitás – perspektíva. J Biomat Sci-Polym E. 2000; 11(11):1107–19.
116. Mao C, Qiu YZ, Sang HB, Mei H, Zhu AP, Shen J és mások. Különféle megközelítések a bioanyag felületek módosítására a hemokompatibilitás javítása érdekében. Adv kolloid interfész. 2004;110(1-2):5–17.
117. Werner C, Maitz MF, Sperling C. A hemokompatibilis bevonatok jelenlegi stratégiái. J Mater Chem. 2007;17(32):3376–84.
118. Huang J, Xue J, Xiang K, Zhang X, Cheng C, Sun S és mások. Poliéterszulfon membránok felületének módosítása metoxil poli(etilénglikol)-poliuretán-metoxil poli(etilénglikol) triblokk kopolimerek keverésével. Colloid Surface B. 2011;88(1):315–24.
119. Liu X, Xu Y, Wu Z, Chen H. Poly(n-vinylpyrrolidone)-modified surfaces for biomedical applications. Macromol Biosci. 2013;13(2):147–54.
120. Li X, Wang M, Wang L, Shi X, Xu Y, Song B és társai. Blokk-kopolimerrel módosított felületek biomakromolekulák konjugálásához a mennyiség és az aktivitás szabályozásával. Langmuir. 2013;29(4):1122–8.
121. Modi A, Verma SK, Bellare J. Hidrofil zif{1}} díszített go nanolapok javítják a poliéterszulfon üreges rostos membránok biokompatibilitását és elválasztási teljesítményét: potenciális membránanyag bioműves májalkalmazáshoz. Mater Sci Eng C. 2018;91:524–40.
122. Said N, Abidin MNZ, Hasbullah H, Ismail AF, Goh PS, Othman MHD és mások. A vas-oxid nanorészecskék javították a biokompatibilitást és eltávolították a poliszulfon üreges rostos membránok középmolekulájú urémiás toxinját. J Appl Polym Sci. 2019;136(48):48234.
123. Wang L, Gong T, Brown Z, Randle C, Guan Y, Ye W és mások. Ascidian-ihlette heparin-utánzó mágneses nanorészecskék, amelyek hemodialízisben újrahasznosítható antikoagulánsként alkalmazhatók. ACS Biomater Sci Eng. 2020;6(4): 1998–2006.
124. Cheng C, Sun S, Zhao C. Progress in heparin and heparin-like/mimicking polimer-functionalized membránok. J Mater Chem B. 2014; 2(44): 7649–72.
125. Nie S, Xue J, Lu Y, Liu Y, Wang D, Sun S és mások. A hidrofil és anionos felületű poliéterszulfon membrán jobb vérkompatibilitása. Colloid Surface B. 2012;100:116–25.
126. Li L, Cheng C, Xiang T, Tang M, Zhao W, Sun S és mások. Poliéterszulfon hemodialízis membrán módosítása citromsavval ojtott poliuretán és véralvadásgátló hatásának keverésével. J Membrane Sci. 2012;405:261–74.
127. Wang LR, Qin H, Nie SQ, Sun SD, Ran F, Zhao CS. Heparinszerű poli(éter-szulfon) polimer közvetlen szintézise és vérrel való kompatibilitása. Acta Biomater. 2013;9(11):8851–63.
128. Nie S, Tang M, Cheng CS, Yin Z, Wang L, Sun S és mások. Biológiailag inspirált membrán kialakítás heparinszerű interfésszel: elhúzódó véralvadás, gátolt komplementaktiváció és bio-mesterséges májsejtek proliferációja. Biomater Sci-Uk. 2014;2(1):98–109.
129. Ma L, Qin H, Cheng C, Xia Y, He C, Nie C és társai. Kagyló ihlette önbevonat a makro-interfészen, javított biokompatibilitással és bioaktivitással a dopaminnal átoltott heparinszerű polimerek és heparin révén. J Mater Chem B. 2014;2(4):363–75.
130. Meyer TW, Peattie JWT, Miller JD, Dinh DC, Recht NS, Walther JL és mások. A fehérjéhez kötött oldott anyagok kiürülésének növelése szorbens hozzáadásával a dializátumhoz. J Am Soc Nephrol. 2007;18(3):868–74.
131. Patzer J. A kötött oldott anyag dialízis elvei. Ott Apher Dial. 2006;10(2):118–24.
132. Agar JWM. Zöld dialízis: az előttünk álló környezeti kihívások. Semin dialízis. 2015;28(2):186–92.
133. Madsen B, Britt DW, Ho C, Henrie M, Ford C, Stroup E és mások. A hemodialízis membránfelületi kémiája a lipopoliszacharid transzfer gátjaként. J Appl Polym Sci. 2015;132(4155021).
134. Lonnemann GR. A dializátum minősége: integrált megközelítés. Kidney Int. 2000;5876:S112–9.
135. Susantitaphong P, Riella C, Jaber BL. Az ultratiszta dializátum hatása a gyulladás markereire, az oxidatív stresszre, a táplálkozásra és a vérszegénység paramétereire: metaanalízis. Nephrol Dial Transpl. 2013;28(2):438–46.
136. Gorbet MB, Sefton MV. Endotoxin: a hívatlan vendég. Bioanyagok. 2005; 26(34):6811–7.
137. Schepers E, Glorieux G, Eloot S, Hulko M, Boschetti-de-Fierro A, Beck W és mások. A növekvő membrán pórusméret és az endotoxin permeabilitás közötti összefüggés felmérése egy új, kísérleti dialízis szimulációs rendszer segítségével. BMC Nephrol. 2018;19(1):1–0.
138. Glorieux G, Hulko M, Speidel R, Brodbeck K, Krause B, Vanholder R. Az endotoxinon túl nézve: A pirogén visszatartás összehasonlító vizsgálata a steril dialízisfolyadék előállításához használt ultraszűrőkkel. Sci Rep 2014;4:6390.
139. van Tellingen A, Grooteman M, Schoorl M, Bartels P, Schoorl M, van der Ploeg T és társai. Az interkurrens klinikai események előrejelzik a plazma c-reaktív fehérje szintjét hemodializált betegekben. Kidney Int. 2002;62(2):632–8.
140. Darkow R, Groth T, Albrecht W, Lutzow K, Paul D. Funkcionalizált nanorészecskék endotoxin kötéshez vizes oldatokban. Bioanyagok. 1999;20(14):1277–83.
141. Murphy MC, Patel S, Phillips GJ, Davies JG, Lloyd AW, Gun'Ko VM és társai. Gyulladásos citokinek és endotoxin adszorpciója mezopórusos polimerek és aktív szén által. In: RodriguezReinoso F, McEnaney B, Rouquerol J, Unger K, szerkesztők. Felszíntudományi és katalízissel kapcsolatos tanulmányok; 2002. p. 515–20.
Cui Gao1, Qian Zhang1, Yi Yang1,2,3, Yangyang Li4,5 és Weiqiang Lin1,3
1 Vesebetegség Központ, The First Affiliated Hospital, Zhejiang University School of Medicine, Hangzhou 310003, Zhejiang, Kína.
2 Nephrology Department, The Fourth Affiliated Hospital, Zhejiang University School of Medicine, Yiwu 322000, Zhejiang, China.
3 International Institutes of Medicine, The Fourth Affiliated Hospital, Zhejiang University School of Medicine, Yiwu 322000, Zhejiang, China.
4 Női Reproduktív Egészségügyi Kutatólaboratórium Zhejiang tartományban, Női Kórház, Zhejiang Egyetem Orvostudományi Kara, Hangzhou 310006, Zhejiang, Kína.
5 Cancer Center, Zhejiang University, Hangzhou 310058, Zhejiang, Kína.






