A liponsav vesevédő szerepe vesebetegségben
Aug 31, 2023
Absztrakt:A vese kulcsfontosságú szerv, amely eltávolítja az anyagcsere-hulladékot és visszaszívja a tápláló elemeket. Részt vesz a vérnyomás szabályozásában, az elektrolit-egyensúly és a vér pH-háztartásának fenntartásában, valamint az eritropoézisben és a D-vitamin érésében. Az ilyen nagy terhelés miatt a vese energiaigényes szerv, és folyamatosan ki van téve endogén és exogén inzultusoknak, ami akárakut vese sérülés(AKI) illkrónikus vesebetegség(CKD). Ennek ellenére nincs terápiás kezelés az AKI vagy a CKD hatékony kezelésére. Ezért sürgősen szükség van új terápiás megközelítésekre a vesekárosodás leküzdésére. Ez az áttekintő cikk a -liponsav (ALA) szerepét tárgyalja a vesebetegségek megelőzésében és kezelésében. A vesekárosodás különféle állatmodelljére összpontosítunk, amelyekkel az ALA mögöttes renoprotektív mechanizmusait feltárták. Az érintett állatmodellek közé tartozik a diabéteszes nefropátia, a szepszis által kiváltott vesekárosodás, a vese ischaemiás sérülése, az egyoldali ureterelzáródás, valamint a folsav és fémek, például ciszplatin, kadmium és vas által kiváltott vesekárosodások. Kiemeljük az ALA vesevédő hatásának közös mechanizmusait, amelyek magukban foglalják az oxidatív károsodások csökkentését, az antioxidáns kapacitás növelését, a gyulladások ellensúlyozását, a vesefibrózis mérséklését és a nephron sejthalál mérséklését. Ezekkel a mechanizmusokkal éri el az ALA biológiai funkcióját a vesekárosodás enyhítésében és a veseműködés javításában. Mindazonáltal arra is rámutatunk, hogy átfogóbb, preklinikai és klinikai vizsgálatokra lesz szükség ahhoz, hogy az ALA-t jobb terápiás szerré tegyük a vesebetegségek megcélzására.
Kulcsszavak: liponsav;akut vese sérülés; krónikus vesebetegség; diabéteszes vesebetegség; diabéteszes nefropátia; nephroprotection

KATTINTSON IDE, HA SZEREZZEN CISTANCHE-T CKD-KEZELÉSEKRE
1. Bemutatkozás
A vese létfontosságú szerv, részt vesz az elektrolit-egyensúly fenntartásában, a vér pH-stabilitásában, az anyagcsere-hulladékok eltávolításában, valamint a tápanyagok és ásványi anyagok visszaszívásában [1,2]. A vese részt vesz az eritropoézisben, a D-vitamin érésében és a vérnyomás szabályozásában is [3]. Patofiziológiás körülmények között, például éhezés, hosszan tartó éhezés és inzulinrezisztencia esetén a vese glükoneogenezis útján is képes regenerálni a glükózt olyan prekurzor molekulák felhasználásával, mint a glicerin, alanin, piruvát és laktát [4]. Mint ilyen, a vese mindig nagy terhelést jelent, és így számos kockázati tényezőnek van kitéve, amelyek vesebetegséget vagy sérüléseket okozhatnak. Kétféle vesebetegség létezik: krónikus vesebetegség (CKD) [5] és akut vesekárosodás (AKI) [6]. CKD akkor fordul elő, ha a vesefunkció fokozatos, több mint 3 hónapig tartó hanyatlása következik be a glomeruláris filtráció károsodása és a tubuláris sérülések következtében [7]. Az előrejelzések szerint 2040-re a krónikus vesebetegség lesz az ötödik vezető halálok világszerte [8]. Másrészt az AKI akkor fordul elő, ha a vesefunkció gyors, 3 hónapnál rövidebb hanyatlása következik be, és ezt acidózis, folyadéktúlterhelés, valamint elektrolit- és hematológiai változások jelzik [7]. Az is ismert, hogy a CKD-ben szenvedő egyéneknél megnövekedett az AKI kockázata [8]. Jelenleg nincs gyógyszerkészítmény az AKI vagy a krónikus vesebetegség gyógyítására. Míg a vesedialízist gyakran alkalmazzák a vesék további károsodásának megelőzésére és működésük fenntartására, a vesecsere lehet az utolsó lehetőség a beteg túlélése szempontjából. Ezért ha nem kontrollálják, az AKI és a CKD veseelégtelenséghez vezethet, ami jelentősen növeli a morbiditást és a mortalitást [7,9]. Ezért kielégítetlen igény mutatkozik a vesebetegség elleni küzdelemben.
A vesebetegségek leküzdésére számos terápiás megközelítést vizsgáltak [10–13]. Ide tartoznak az exogén és endogén vegyületek, az étrendi manipulációk, az anyagcsere-utak modulálása, az őssejt-megközelítések és a sejtjelátviteli folyamatok [10,11,14–21]. Ebben az áttekintő cikkben a liponsav szerepére fogunk összpontosítani a vesesérülések megelőzésében és enyhítésében. Különösen azokra a vizsgálatokra összpontosítunk, amelyek állatmodelleket alkalmaznak a liponsav vesekárosodásokra gyakorolt védő hatásának feltárására. A vesekárosodás ezen állatmodelljei közé tartozik a diabéteszes vesebetegség vagy diabéteszes nephropathia, a vese ischaemia-reperfúziós sérülése, a szepszis által kiváltott vesekárosodás, az unilaterális ureterelzáródás (UUO) által kiváltott vesekárosodás, a ciszplatin-indukált vesekárosodás, kadmium okozta vesekárosodás, folsavsav által kiváltott vesekárosodás, ésvas okozta akut vesekárosodás(1.ábra).

1. ábra: A vesekárosodás állatmodelljeit tárgyaljuk ebben a cikkben. Ezek a modellek az akut vesekárosodást és a krónikus vesebetegséget egyaránt tartalmazzák.
2. Alfa-liponsav
Az ALA egy természetben előforduló ditiolvegyület [22]. A -ketoglutarát-dehidrogenáz, az elágazó láncú aminosav-dehidrogenáz és a piruvát-dehidrogenáz kofaktora [23–25] (2. ábra). Ezért az ALA energiamodulátor [26,27] (3. ábra). Ezen túlmenően, mivel képes tiolcsoportokat kicserélni más tioltartalmú molekulákkal, például glutationnal és fehérje cisztein-maradékaival, az ALA redox modulátorként is ismert [26–28] (3. ábra). Az ALA-t gyakran univerzális antioxidánsként emlegetik, mivel mind lipofil, mind hidrofil környezetben antioxidánsként hat, és csökkenti az oxidatív anyagcsere melléktermékeit, például a reaktív oxigénfajtákat (ROS) és a reaktív nitrogénfajokat (RNS) (4. ábra) [29] ]. Az ALA minimális mellékhatással képes fémeket, például cinket, vasat és réz kelátot képezni, valamint endogén antioxidánsokat – például glutationt – és exogén vitamin-antioxidánsokat – például C- és E-vitamint – regenerálni [30] (4. ábra). Ennél is fontosabb, hogy az ALA a gyulladást is gátolja az NF-KB megcélzásával és a gyulladásos citokinek felszabadulásának csökkentésével (4. ábra). Ezért kimutatták, hogy az oxigén szabad gyökök megkötésével az ALA fokozhatja a glomeruláris funkciót és csökkentheti a vesegyulladást [31]. A vizsgálatok azt is kimutatták, hogy az ALA-kezelés csökkentheti az akut vesekárosodást azáltal, hogy csökkenti a szérum vér karbamid-nitrogénjét,kreatininszint tumornekrózisfaktor alfa (TNF-), interleukin-6 (IL-6) és interleukin-1 béta (IL-1), ezáltalcsökkent endotelinszint-1érszűkület, neutrofil diffúzió és gyulladás a vesékben.

2. ábra. A liponsav a mitokondriális 2-ketosav-dehidrogenáz komplex kofaktora, beleértve a piruvát-dehidrogenáz komplexet, a -ketoglutarát-dehidrogenáz komplexet és az elágazó láncú aminosav-dehidrogenáz komplexet. Az E1 alegység a 2-ketosav-dekarboxiláz, kofaktorként TPP-t használva; az E2 alegység egy dihidrolipoamid-aciltranszferáz, liponsavat alkalmazva kofaktorként; az E3 alegység egy dihidrolipoamid-dehidrogenáz, amely NAD+-t használ elektronakceptorként az E2 alegységhez kapcsolódó lipoilcsoport oxidációjához. Az E3 katalizálja a liponsav oxidált formájának képződését, és közben NADH-t termel [32–34].

3. ábra. A liponsav részt vesz a tiol-diszulfid cserében, amely módosítja a sejt redox- és energiaállapotát.
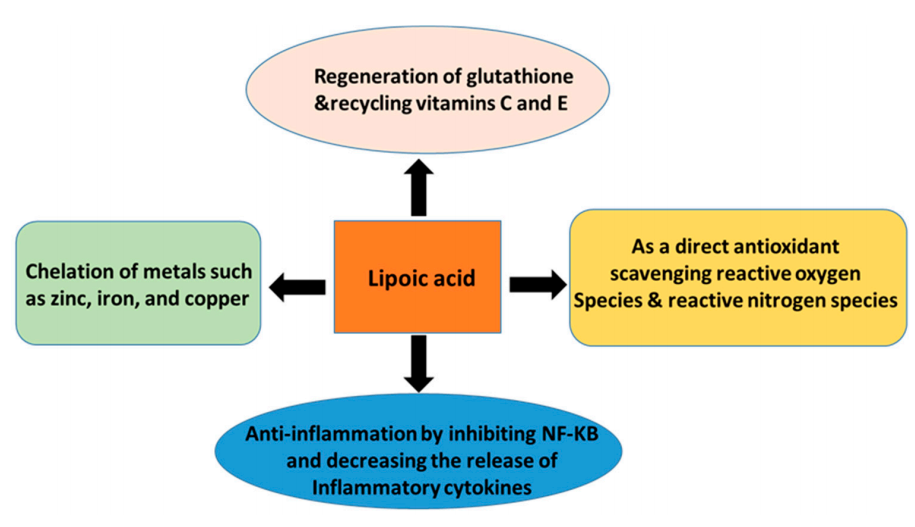
4. ábra: A liponsav biológiai hatásai és lehetséges mechanizmusai, amelyek magukban foglalják a glutation, a C- és E-vitamin regenerációját, a ROS megkötését, a kelátképző fémionokat és a gyulladáscsökkentő hatást

3. A liponsav (ALA) védő szerepe vesekárosodásban
A vesebetegséget számos sértés idézheti elő, például cukorbetegség, ischaemiás reperfúzió, gyógyszertoxicitás, kontrasztanyag és gyógyszerek [7]. Ha nem kontrollálják, az AKI veseelégtelenséghez vezethet, 20%-os halálozási aránnyal [25]. Az AKI-t a szérum kreatininszint emelkedése, az oliguria és a vesekárosodás markereinek jelenléte jellemzi, mint például az albuminuria, a tubuláris rendellenességek miatti elektrolit-rendellenességek vagy a képalkotó vagy szövettani strukturális károsodás [9]. Kimutatták, hogy az ALA profilaxis csökkenti a vesetubuláris sérülések pontszámait, a vizeletkárosodás markereit, a szérum kreatinin szerkezeti károsodását és növeli a glomeruláris filtrációt [35]. A következő szakaszokban az ALA nefroprotektív hatásait és a mögöttes védőmechanizmusokat tárgyaljuk a vesekárosodás különféle állatmodelljeiben, amint azt az 1. ábra mutatja.
3.1. Diabetikus nefropátia
A diabéteszes nephropathia (DN), más néven diabéteszes vesebetegség (DKD) [36–38], a CKD és a végstádiumú veseelégtelenség fő oka a cukorbetegeknél [39–41]. Jól bebizonyosodott, hogy a mitokondriális diszfunkció hozzájárul a DKD-hez, és a mitokondrium a DKD elleni küzdelem célpontja [42–44]. A DN az 1-es vagy 2-es típusú diabetes mellitus mikrovaszkuláris szövődményének tekinthető [7,41]. Ezt a diabéteszes vesebetegséget a glomeruláris filtráció csökkenése, proteinuria és vesefibrózis jellemzi [7]. A hiperglikémia fokozza az oxidatív stresszt, ami a reaktív oxigénfajták (ROS) korai túltermeléséhez [45] és a glutation metabolikus utak szabályozási zavarához [7] vezet. A malondialdehid (MDA) a lipid-peroxidáció végterméke, és gyakran használják a szabad gyökök és az oxidatív stressz jó markereként [46–49]. Tanulmányok kimutatták, hogy az ALA-val végzett előkezelés csökkentette az MDA-tartalmat és javult a vese oxidatív stressze [32,50]. A lipoamidról, az ALA származékáról kimutatták, hogy gátolja a vesefibrózist cukorbetegségben azáltal, hogy fokozza a mitokondriális funkciót és szabályozza a retina X receptor alfa transzkripciós faktor aktiválódását [51]. A nikotinamiddal és sztreptozotocinnal együtt kiváltott cukorbetegség patkánymodelljében, amely kevésbé időigényes módszer a cukorbetegség rágcsálómodelljeinek létrehozására [52], Dugbartey et al. azt is kimutatták, hogy az ALA vesevédő mechanizmusa magában foglalja a vese cisztationin-liáz/hidrogén-szulfid rendszerének aktiválását [53]. Azt is kimutatták, hogy az ALA szinergikus hatást fejt ki a gyulladásos citokinek szérumszintjének csökkentésére és a vesefunkció javítására cukorbeteg állatoknál, ha az angiotenzin II receptor inhibitor valzartánnal kombinálják [54]. Az 5. ábra meggyőző bizonyítékot mutat a szövettani festődésre vonatkozóan, miszerint az ALA erős védőhatást fejt ki a diabéteszes vesére egy 2-es típusú diabéteszes állatmodellben [55] Az ALA vesevédelmének mechanizmusa cukorbetegségben az a képessége, hogy aktiválja az Nrf2 jelátviteli útvonalat, ami a második fázisú citoprotektív fehérjék, mint például a hem oxigenáz-1 (HO-1) és a NAD(P)H kinon-dehidrogenáz 1 (NQO1) [56–58]. Hangsúlyozni kell, hogy bár az ALA nefroprotektív diabéteszes vesebetegségben, prooxidáns vagy toxikus hatásokat fejthet ki, és bizonyos patofiziológiás körülmények között nem szolgálhat Nrf2 induktorként [59–61]. Ezen túlmenően, míg azt gondolták, hogy az ALA aktiválja az inzulin jelátviteli utakat a cukorbetegség leküzdésére [28], és kimutatták, hogy megelőzi a magas fruktóz okozta kardiometabolikus rendellenességeket és a veseműködési zavarokat [62], arról is beszámoltak, hogy az ALA csak csillapítja a proteinuriát és az oxidatív hatást. stressz a diabéteszes veseelégtelenség progressziójának lassítása nélkül [63].
3.2. Szepszis okozta vesekárosodás
A szepszis potenciálisan életveszélyes patológiás állapot a bakteriális fertőzésre adott túlzott gyulladásos válasz következtében [64–66]. A súlyos szepszis többszervi elégtelenséget okozhat, a vese a leginkább érintett szerv [67,68]. Becslések szerint a szeptikus betegek közel 50%-ánál akut vesekárosodás alakul ki, és nincs hatékony kezelés a szeptikus AKI kezelésére [69]. Ebben a tekintetben számos kutató átfogóan értékelte az ALA védő és terápiás értékeit a lipopoliszacharidok injektálásával modellezett szepszis által kiváltott AKI-ban, bár alkalmanként alkalmaztak cacal punkciót és ligáció (CPL) által kiváltott szeptikus AKI-t [22,70]. Kimutatták, hogy az ALA képes megvédeni a szeptikus vesekárosodást az autofágia fokozásával [71]. Ezenkívül az ALA enyhítheti a szepszis által kiváltott AKI-t azáltal, hogy az NF-KB jelátviteli útvonal gátlásán keresztül ellensúlyozza a gyulladást [72], mérsékli a mitokondriális oxidatív stresszt, valamint megőrzi a 3-as típusú Na+/H+ hőcserélőt és az akvaporin 2 expresszióját a vesében [73]. . Az ALA gátolja a tumornekrózis faktor, az interleukin (IL)-6 és az IL-1 felszabadulását a szérumba, és elnyomja az indukálható nitrogén-monoxid-szintáz [22] expresszióját szeptikus AKI-ben. Ezért az ALA ígéretes természetes termék lehet a szeptikus AKI kezelésére.

3.3. Vese ischaemiás reperfúzió
Ischaemia akkor fordul elő, ha a vér perfúziója csökken, és a szervek véráramlása csökken [74]; ennek számos oka lehet, például trombusok, traumák és érelmeszesedés [75]. A szövetkárosodás és a nekrózis megelőzése érdekében az ischaemiát reperfúzióval oldják meg [75]. Bár az ischaemiás reperfúzió elengedhetetlen a szöveti nekrózis megelőzéséhez, gyulladást, valamint a reaktív oxigénfajták és reaktív nitrogénfajták számának növekedését is okozhatja [75–77]. Tanulmányok kimutatták, hogy az ALA előkezelése javíthatja a vesék, a retina, az idegrendszer, a máj, a belek és egyebek károsodását [75]. Az ALA mögött meghúzódó védőmechanizmusok a vese ischaemia-reperfúziós sérülésében többtényezősek lehetnek, beleértve az oxidatív károsodások ellensúlyozását [32,75] és a csatornák, enzimek és transzporterek, például az akvaporinok és a nátrium transzporterek, valamint a nátrium-kálium ATPáz és nitrogén-monoxid-szintáz izoformák [78]. Az ALA védheti a vese ischaemia-reperfúziós sérülését is azáltal, hogy mérsékli a neutrofil infiltrációt és gátolja a gyulladásos mediátorok felszabadulását [79]. A tanulmányok azt is kimutatták, hogy a végtag ischaemia-reperfúziós sérülése által kiváltott vesekéreg szerkezeti károsodást az ALA [80] és az ALA enyhítheti, és a xantin-oxidáz inhibitor febuxosztáttal kombinálva kiváló védőhatást mutat a vese ischaemia-reperfúziós sérülése esetén [81]. . Az ALA a veseműködési zavart és a vesekárosodást is megelőzheti azáltal, hogy gátolja az endotelin-1 túlzott expresszióját vese ischaemia-reperfúziós károsodás esetén [82].
3.4. Egyoldali ureterelzáródás (UUO) által kiváltott vesekárosodás
A vesekárosodás egyoldali ureterelzáródásos (UUO) állatmodelljét széles körben alkalmazták a vesekárosodás mechanizmusának és számos szer terápiás értékének vizsgálatára [83–87]. Ennek a modellnek megvannak az előnyei, mivel nem urémiás normotenzív rendellenességről van szó, a vese nyilvánvaló gyulladásos vagy toxikus károsodása nélkül [88]. Ezenkívül a vesekárosodás UUO modellje a vesefibrózis patofiziológiájának tanulmányozására is jó modell [89–93]. Ezért a vesekárosodás UUO modellje szorosan utánozhatja a humán obstruktív vesekárosodás mögöttes patofiziológiáját [94,95]. Az ALA-ról kimutatták, hogy renoprotektív az UUO által kiváltott vesekárosodással szemben [88]. Wongmekiat et al. azt találták, hogy amikor az ALA-t (60/mg/ttkg) ip injekcióban adták patkányoknak két nappal az UUO indukciója előtt, és az UUO után egy hétig folytatták, UUO által kiváltott veseműködési zavar, oxidatív stressz, valamint nitrogén-monoxid-termelés és transzformáció következett be. faktor-1 értékeit nagymértékben gyengítette az ALA-kezelés [88]. Ezenkívül az ALA-ról kimutatták, hogy az UUO vesekárosodás egérmodelljében javítja az epiteliális-mezenchimális átmenetet [96]. Ezek a vizsgálatok tehát azt mutatják, hogy az ALA nefroprotektív az UUO által kiváltott vesekárosodással szemben.
3.5. Ciszplatin által kiváltott nefrotoxicitás
A ciszplatin egy kemoterápiás gyógyszer, amely úgy kezeli a rákot, hogy behatol a daganatsejtekbe, kloridionokat szabadít fel, és hidratálódik, hogy keresztkötést kapjon a DNS-sel, és DNS-adduktumokat képezzen a tumorsejtek replikációjának gátlása érdekében [97,98]. A ciszplatin gyógyszeres kezelésnek azonban számos mellékhatása van, például ototoxicitás, neurotoxicitás, nefrotoxicitás, hányinger és hányás [35,97–99]. A nefrotoxicitás azért jelentkezik, mert a ciszplatint a proximális tubuláris sejtek felveszik, és a szérumban akár ötször nagyobb koncentrációra képes, mint a ciszplatin [35,97]. A ciszplatin nefrotoxicitása csökkent kreatinin-clearance-hez, megnövekedett szérum kreatininszinthez, emelkedett karbamidszinthez, fokozott vizeletkibocsátáshoz és csökkent glomeruláris filtrációs sebességhez vezet 100 1011. A ciszplatin emellett csökkenti a glutation S-transzferáz, glutation-peroxidáz és szuperoxid-diszmutáz antioxidánsokat is, ami a ROS és az oxidatív markerek, például a lipid-peroxidációból származó MDA szintjének emelkedését okozza [35,100,102]. A vesék proximális tubulusai nagy mennyiségű mitokondriumot tartalmaznak (35). A hidrolizált ciszplatin pozitív töltésű metabolitot hoz létre, amely a mitokondriumok negatív töltésű molekulái miatt felhalmozódik a mitokondriumokban, magas szintű oxidatív stresszt hozva létre (35) Ennek kezelésére a mitokondriumok használjon endogén antioxidánsokat, például liponsavat a ROS csökkentésére (351. Tanulmányok kimutatták, hogy az ALA megvédi a vesesejteket a ciszplatin toxicitásával szemben (98]), csökkenti a strukturális proximális tubuláris károsodást, és fokozza a glomeruláris filtrációt a vesékben (99,103). Az ALA-ról azt is kimutatták, hogy csökkenti a plazma kreatininszintjét és a vizeletkibocsátást, növeli a kreatinin clearance-ét és a vizelet ozmolalitását, és normalizálja a nátrium kiválasztását ciszplatin vesekárosodás esetén [101].

3.6. Folsav által kiváltott nefrotoxicitás
A magas folsavszint tubuláris károsodást okozhat a tubuláris sejtek leválása és kitágulása miatt [104], ami sejthalálhoz vezet [105]. A ferroptózis a vas- és lipidperoxidáció által okozott sejthalál egy fajtája, amely folsav által kiváltott AKI során lép fel [106]. Ha nagy mennyiségű vas van jelen a szervezetben, ROS keletkezik, ami lipidperoxidációt okoz, károsítja a lipidmembránokat és sejthalált [105]. Megállapítást nyert, hogy az ALA antioxidáns hatása a folsav által kiváltott vesekárosodással szembeni renoprotekciót eredményezett [105]. Li és munkatársai tanulmányában nem volt szignifikáns különbség az alacsony és a nagy dózisú ALA között, ami azt jelzi, hogy az ALA előnyei nem dózisfüggőek [105]. Ezenkívül az ALA úgy működhet, hogy gátolja a p53 ferroptózist, valamint a ferritin és a ferroportin vasexportőrök szabályozását, így megakadályozza a folsav által kiváltott AKI-t [105]. A 6. ábra a folsav által kiváltott vesekárosodás elleni ALA-védelem szövettani ábrázolását mutatja be [105].
3.7. Kadmium által kiváltott nefrotoxicitás
A kadmium egy természetben előforduló mérgező nehézfém, amely nefrotoxicitást okoz [104,107–109]. A kadmium által kiváltott nefrotoxicitás növeli az MDA-szintet, ami károsítja a vese mitokondriumait és a vesekéreget [110]. A kadmiumról kimutatták, hogy csökkenti a glutation-antioxidáns (GSH), a glutation-peroxidáz, a kataláz és a szuperoxid-diszmutáz (SOD) szintjét is [110].
Az ALA-val végzett kezelés antioxidánsként csökkentette az MDA-t és az apoptózist, a kadmium kelátot pedig a vesék kadmiumkárosodásának csökkentése érdekében [111]. Az ALA emellett csökkentette az oxidatív stresszt, elősegítette a glutationhoz kapcsolódó endogén enzimek működését, és megakadályozta a mitokondriális apoptózist kadmium által kiváltott vesekárosodás esetén [110–112].
3.8. Vas okozta akut vesekárosodás
Úgy gondolják, hogy a vas hozzájárul az AKI-hoz és a CKD-hez is [113–118]. Valójában megfigyelték, hogy a vesetubulusok megnövekedett vasszintnek vannak kitéve vesebetegségben szenvedő betegeknél, ami valószínűleg a vas és a vastartalmú fehérjék fokozott szűrésének köszönhető a glomeruláris apparátuson keresztül [114,117,119]. A vas az oxidatív stressz fokozásával súlyosbíthatja a diabéteszes vesebetegséget is [120,121]. Ezért a vas által kiváltott vesekárosodás állatmodellei értékes eszközt jelentettek a vas okozta vesekárosodás mechanizmusainak tanulmányozásában, valamint a természetes termékek vagy gyógyszerek terápiás hatásainak tesztelésében [122–125]. Ebben a tekintetben az ALA-ról kimutatták, hogy nefroprotektív ionok által kiváltott vesekárosodás esetén [126,127]. A vesekárosodás vas-túlterheléses patkánymodelljében az ALA antioxidáns hatást mutatott az oxidatív károsodás gyengítése révén [128]. Azt is megállapították, hogy az ALA gátolja a p38 MAPK jelátvitelt és a NADPH-oxidáz 4 expresszióját vas-indukált vesekárosodásban [127]. Meg kell jegyezni, hogy az ALA vas-indukálta vesekárosodás esetén mindezen védőhatásai részben vaskelátképző tulajdonságának tulajdoníthatók [128–131], amely csökkenti a szabad vas elérhetőségét.
Támogató szolgáltatás:
E-mail:wallence.suen@wecistanche.com
Whatsapp/Tel.:+86 15292862950
Üzlet:
https://www.xjcistanche.com/cistanche-shop






