A karvedilol, egy adrenerg blokkoló, gátolja a melaninszintézist azáltal, hogy gátolja a CAMP/CREB jelátviteli útvonalat az emberi melanocitákban és az ex vivo emberi bőrkultúrában
Mar 20, 2022
Kapcsolatba lépni:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Myoung Eun Choi 1,†, Hanju Yoo 1,2,†, Ha-Ri Lee 2,3, Ik Joon Moon 1, Woo Jin Lee 1, Youngsup Song 3,*,‡ és Sung Eun Chang 1
Absztrakt:A katekolaminok a G-fehérjéhez kapcsolt receptorokon keresztül működnek, és különböző sejtekben 30-as, 50-ciklusos adenozin-monofoszfát (cAMP) intracelluláris szintjének növekedését váltják ki. A katekolamin-bioszintézis és az -adrenerg receptor létezikmelanociták; így a katekolaminok kritikus szerepet játszhatnak a bőr pigmentációjában. Hatásukat és az embertelen bőr melanogenezisét közvetítő mechanizmusokat azonban még nem vizsgálták. Ezért megvizsgáltuk a carvedilol potenciális melanogenetikai hatását, amely egy nem szelektív -blokkoló, amely gyenge 1-blokkoló aktivitással rendelkezik. A karvedilol csökkentette a melanin tartalmat és a celluláris tirozináz aktivitást anélkül, hogy veszélyeztetné a sejtek életképességét normál emberbenmelanocitákvalamint a Mel-Ab-vel immortalizált egér melanocitákban. A carvedilol-szabályozott mikroftalmiával összefüggő transzkripciós faktor (MITF), tirozináz, tirozinázzal kapcsolatos fehérje (TRP)-1 és TRP{4}}. A carvedilol kezelés a foszfor-cAMP-response element-binding protein (CREB) csökkenéséhez vezetett. Ezenkívül a cAMP-szint növekedése forskolinnal végzett kezelés hatására megfordította a karvedilol melanogénellenes hatását. Ezenkívül a carvedilol jelentősen csökkentette a melanin indexet ultraibolya sugárzással besugárzott emberi bőrtenyészetekben. Összességében eredményeink azt mutatják, hogy a karvedilol hatékonyan gátolja a melanogenezist az emberbenmelanocitákés ex vivo humán bőrre a cAMP/protein kinase A/CREB jelátvitel gátlásával. A karvedilol anti-melanogén hatása potenciálisan jelentős hatással lehet a bőrrefehérítésügynökök.
Kulcsszavak:carvedilol; adrenerg blokkolók;melanin szintézis; cAMP/CREB jelzés

Cistancheképes gátolni a melanin szintézist
1. Bemutatkozás
A pigmentált bőrbetegségek széles köre jelentős pszichológiai és szociális hatással van a betegekre. Különféle kezelési módokat fejlesztettek ki, beleértve a szisztémás és helyi szereket, valamint a lézerterápiát [1–3]. Az eredmények azonban gyakran nem kielégítőek, és gyakoriak a kezelésből származó mellékhatások, mint például a gyulladásos hiperpigmentáció (PIH) és a hypopigmentáció. Ezenkívül a kezelés költséges és időigényes [4–6].
A katekolaminok, köztük a dopamin, az adrenalin és a noradrenalin, jelzőmolekulák, amelyek neurotranszmitterként és endokrin hormonként működnek. A bőrben a katekolaminok bioszintézise és lebomlása az emberi keratinocitákban megy végbe, de a melanocitákban a katekolamin szintézise némileg eltérő [7–9]. A katekolaminok a G-fehérjéhez kapcsolt receptorokon (GPCR) keresztül működnek. A katekolaminok kötődése a GPCR-ekhez az intracelluláris adenilátcikláz aktiválását váltja ki, amely 30, 50-ciklusos adenozin-monofoszfátot (cAMP) szintetizál az ATP-ből [10]. A másodlagos hírvivő cAMP úgy fejti ki aktivitását, hogy megköti a protein kináz A (PKA) R-alegységét, ami a cAMP válaszelem-kötő fehérje (CREB) foszforilációját eredményezi. A GPCR-eket aminok és peptidek aktiválják, beleértve a glukagont, a mellékpajzsmirigy hormont, a szekretint és a kalcitonint [10].
Az adrenerg receptor antagonisták közé tartoznak a -receptor és -receptor antagonisták. - A receptorantagonisták nem-szelektív, 1-szelektív és 2-szelektív ágensekre vannak osztva, míg a -receptorantagonisták nem szelektív, 1-szelektív és 2-szelektív ágensekre oszthatók. szelektív blokkoló tevékenységük alapján. Ellentétben az első generációs nem szelektív receptor antagonistákkal, mint a propranolol, timolol és nadolol, a karvedilol egy harmadik generációs nem szelektív blokkoló, amely értágító hatást fejt ki az 1-adrenoreceptorok (1-AR) blokkolásával. [11]. Ezért a karvedilol anonszelektív -blokkoló, gyenge 1-blokkoló hatással [12]. Főleg orális gyógyszerként használják a magas vérnyomás és a pangásos szívbetegségek kezelésére, hasonlóan más -blokkolókhoz [12]. A harmadik generációs blokkolók azonban angiogén, antioxidáns, antiproliferatív, antihipertrófiás és anti-apoptotikus aktivitást mutatnak, amelyek további tisztázást igényelnek [11]. A bőrgyógyászatban antioxidáns és gyulladáscsökkentő hatása miatt a karvedilolt gyakran használják szájon át szedhető készítményekben az erythematotelangiectaticus rosacea kezelésére [13,14]. Ezenkívül a carvedilol antioxidáns hatása megakadályozza az ultraibolya (UV) által kiváltott bőrkarcinogenezist, így vonzó szer az UV-sugárzás okozta bőrbetegségek kezelésében [15–18]. A carvedilolare kemopreventív hatásait azonban nem közvetlenül az AR-k közvetítik. [19] Bár a pontos mechanizmus viszonylag ismeretlen, a cAMP/PKA és a PKC-δ jelátviteli útvonal összefüggésbe hozható a carvedilol bőráttét elleni tulajdonságaival [20].
A pigmentáció vizsgálatának kezdeti szakaszában az emberimelanocitákkimutatták, hogy -1-AR jelátvitelt fejeznek ki noradrenalinnal történő extracelluláris indukció után. Azonban -AR-t nem találtak az adrenerg jelzéssel történő stimuláció utánmelanociták[8]. Ezzel szemben Cillbro et al. később kimutatták, hogy egy specifikus funkcionális 2-AR szignál létezik az emberi melanocitákban, és hogy az 2-ARstimuláció az 2-AR/cAMP útvonalon keresztül pigmentációhoz vezet [7]. Ezért javasolták a katekolaminok szerepét a pigmentáció szabályozásában, és a cAMP-t tekintik a melanogenezis katekolamin szabályozásának fő tengelyének.
A melanogenezis egy összetett folyamat, amely számos útvonalat foglal magában. A tirozináz, a tirozinázzal rokon protein 1 (TRP-1) és a TRP-2, más néven dopakróm tautomeráz (DCT), a három fő melanocita-specifikus enzim, amely részt veszmelanin szintézis[21]. A melanogenezist számos tényező indukálja vagy gátolja, köztük hormonok, citokinek, neurotranszmitterek, növekedési faktorok és mikromolekulák [21–23].
A legfontosabb pozitív szabályozó a melanocortin{0}} receptor és ligandumai, a melanokortin és az adrenokortikotrop hormon [23]. A melanogenezisben szerepet játszó különféle tényezők azonban az -endorfin, az ösztrogének, az androgének, a D3-vitamin és a katekolaminok [23]. A kumulált bizonyítékok azt sugallják, hogy az L-tirozin és az L-DOPA, amelyek a melanogenezis szubsztrátjai és intermedierei, más sejtfunkciók szabályozói mellett a melanogén útvonal induktorai és pozitív szabályozói is [24]. Ezenkívül Jeff Howe és mtsai. felvetették, hogy az L-tirozin melanogenezisének indukálását és szabályozását az adrenerg receptorok L-tirozin általi közvetlen aktiválása közvetíti, nem pedig metabolikus termékei, például a katekolaminok [25]. Vizsgálataik során a noradrenalin és az epinefrin stimulálta a tirozináz aktivitást, de induktív hatásukmelanin szintézisviszonylag alacsonyabb volt, mint az L-tirozin [25].
A katekolaminok fontos szerepet játszhatnak a bőr pigmentációs rendszerében; azonban a melanogenezisre gyakorolt hatásukat a harmadik generációs, nem szelektív blokkolók hatását illetően még nem vizsgálták. Ezért jelen tanulmányunkban arra törekedtünk, hogy megvizsgáljuk, hogy a karvedilol befolyásolja-e a melanogenezist, és feltártuk a hatásmechanizmusait emberi szervezetben.melanocitákés ex vivo emberi bőr és lehetséges felhasználása afehérítéstermék.

gátolják a melanin képződéstgyógynövényes tartályok
2. Eredmények
2.1. A karvedilol elnyomja a melanogenezist
A karvedilol citotoxicitása normál emberrel szembenmelanociták(NHMs) és Mel-ab sejteket WST sejtproliferációs vizsgálattal értékeltük. A 10 µM carvedilol-koncentráció citotoxicitást mutatott mind az NHM-ekkel, mind a Mel-ab sejtekkel szemben (1A, B ábra). Ezért a további vizsgálatok során 8 µM karvedilolt használtunk, amely nem citotoxikus az NHM-ekre.
A karvedilollal végzett kezelés dózisfüggő módon csökkentette a melanintartalmat anélkül, hogy az NHM-ek életképességét befolyásolta volna (1C. ábra). A melanintartalom 28,36 százalékkal csökkent 96 hof 8 µM carvedilol kezelés után (1C. ábra). 100 mg/ml arbutin hozzáadása kisebb mértékben csökkentette a melanintartalmat, mint a karvedilol (1C. ábra). 4 napos carvedilol-kezelés után a melanintartalom időfüggő módon csökkent (1D. ábra). A karvedilollal végzett előkezelés után 4 napig tartó forskolinnal (FSK) végzett kezelés azonban a melanintartalom növekedését idézte elő (1E. ábra). Az FSK NHM-ekben 2 óra múlva a legnagyobb mértékben növeli a MITF transzkripcióját, és feltételezhetően a cAMP-n keresztül működik. /PKA/CREB útvonal (1F. ábra).

2.2. A karvedilol gátolja az MITF és célgének expresszióját, és csökkenti a foszfo-CREB NHM-szintet
Mivel a karvedilol csökkentette a melanin felhalmozódását, a celluláris tirozináz aktivitást vizsgáltuk. A karvedilollal végzett kezelés dózisfüggő módon csökkentette a celluláris tirozináz aktivitást NHM-ekben (2A. ábra). A tirozináz aktivitás 28,48 százalékkal csökkent 96 órás 8 µM karvedilollal végzett kezelés után (2A ábra). Ezt követően meghatároztuk, hogy a carvedilol befolyásolja-e a MITF expresszióját, amely döntő szerepet játszik a tirozináz és a downstream melanogén gének szabályozásában. Az FSK-kezelés növelte az intracelluláris cAMP-szintet és megfordította a karvedilol anti-melanogén hatásait. A carvedilol szignifikánsan csökkentette a melanogenezis központi transzkripciós faktora, az MITF fehérjeszintjét 72 órával (2B. ábra). Ezenkívül a célgének, például a tirozináz és a TRP{10}} expressziója csökkent a carvedilol-kezelés után (2B. ábra). Ezek az eredmények azt mutatják, hogy a karvedilol gátolja a melanogenezist azáltal, hogy csökkenti a MITF jelátvitelt.
Ezt követően a melanogenezis intracelluláris jelátviteli útvonalait vizsgáltuk, amelyek szabályozzák a MITF-transzkripciót a foszfo-CREB és a foszfo-ERK expressziós szintjének mérésével. A foszfo-ERK szintek nem változtak az idő múlásával a carvedilol-kezelést követően; azonban a foszfo-CREB szintek csökkentek (2B. ábra). A korábbi megfigyelésekkel összhangban eredményeink azt mutatták, hogy a carvedilolin gátolja a melanogenezist a cAMP/PKA/CREB jelátviteli útvonal gátlásával. Ezenkívül az FSK-kezelés megfordította a carvedilol melanogénellenes hatását a cAMP-szintek növelésével.

2.3. Melanin index és immunhisztokémiai festés ex vivo humán bőrkultúrában
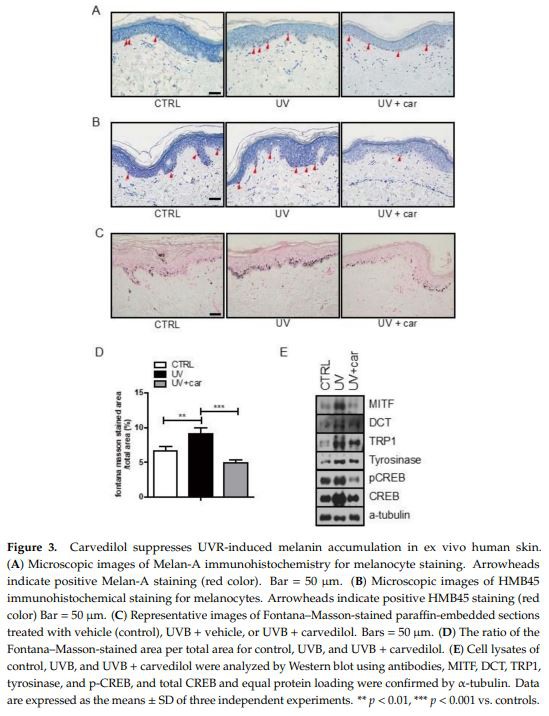
Az epidermális melanociták sűrűségét és a melanin indexet ex vivo humán bőrkultúra szövetmetszetekben Melan-A, illetve Fontana–Masson festéssel detektáltuk. A karvedilol nem befolyásolta a Melan-A (plusz) számátmelanocitáka carvedilollal plusz UV-sugárzással (UVR) kezelt mintában, összehasonlítva a csak UVR-rel kezelt mintában (3A. ábra). A HMB45(plus)melanociták azt jelezhetik, hogy a melanocita aktivitás nőtt az UVR-kezelés hatására, és a carvedilol-kezelést követően fordítottan lecsökkent (3B. ábra). A melanintartalom azonban szignifikánsan csökkent a carvedilollal plusz UVR-rel kezelt mintákban, összehasonlítva az egyedül UVR-val kezelt mintákban (3C. ábra). A melaninindex kiszámításához a Fontana–Masson festett területének hányadát az UVR-nek kitett minta és a karvedilol plusz UVR-sugárzásnak kitett minta közötti teljes területen kiszámoltuk és összehasonlítottuk (3D. ábra). Az egyes minták sejtlizátumait Western blotassay-vel elemeztük, amely kimutatta, hogy a tirozináz, a TRP1 és a DCT szintje az UVR hatására megnőtt, a karvedilol-kezelés pedig csökkentette a szabályozást (3E. ábra). Ennek eredményeként a carvedilol jelentősen csökkentette a melanin indexet és a melanogenezishez kapcsolódó fehérjéket, megmutatva anti-melanogén hatását az UVR-kezelt emberi bőrön.
3. Vita
A melanin a bőr és a haj színéért felelős pigment, amelyet a melanoszómák szintetizálnakmelanociták. Bár az epidermális melanin fontos védő szerepet játszik az UVR ellen, a melanin túltermelése és felhalmozódása a bőrben problémás bőrhiperpigmentáris rendellenességeket okoz, mint például a PIH, a fotoöregedés okozta diszpigmentáció, a melasma és a szoláris lentigines [18,26]. Ezért a melanogenezis gátlása állt a bőr szépségét és egészségét szolgáló gyógyászati és kozmetikai kezelések középpontjában. Jelentős erőfeszítéseket tettek új és hatékony pigmentáció elleni szerek azonosítására. A specifikus szerek melanogenezis-ellenes mechanizmusai azonban jelenleg bizonytalanok, és általában egérsejtekben értékelték őket, amelyek nem mindig konzisztensek az emberi bőrön végzett vizsgálatok eredményeivel [27, 28]. Ezen túlmenően, mivel a melanociták melanogenezisét a keratinociták és más szomszédos sejtek szigorúan szabályozzák, az együtttenyésztett emberi sejtek vagy az ex vivo emberi bőr megbízhatóbb kísérleti környezet a hatékony módszerek feltárására.fehérítésügynökök [29]. A legtöbb bőrfehérítő anyag, akár természetes, akár kémiai eredetű, bőrmérgezést vagy irritációt okozhat, ami bizonyos mértékig előre jelezhető melanocitákkal végzett in vitro sejtéletképességi vizsgálatokkal. Vizsgálatunkban a carvedilol mérsékelt dózisban alkalmazva nem mutatott citotoxicitást.

cistanche bienfaits
A hidrokinonos helyi krémek nemkívánatos hipopigmentációs rendellenességeket és bőrtoxicitást okozhatnak [30–32]. Továbbá néhányfehérítésA kozmetikumok katasztrofális következményekkel járnak azáltal, hogy a tirozináz fehérjék lebomlásával hipopigmentációt váltanak ki [33–35]. A fehérítő szerek a felhasználótól függően nagyobb dózisban is használhatók, hogy maximalizálják a hiperpigmentáris elváltozások fehéredését. Ezért folyamatosan vizsgálják a biztonságos és egészséges bőrfehérítő szerek felfedezésére irányuló erőfeszítéseket.
Ezért a jelen vizsgálatot úgy tervezték, hogy normál emberi sejtekben és ex vivo emberi bőrön végezzék el. Továbbá, a katekolaminok által kialakított G-jelátviteli mechanizmus alapján, amely növeli a celluláris cAMP-szintet, úgy gondoltuk, hogy egy adrenerg blokkoló csökkentheti a cAMP-szintet, és gátolja az UVR/cAMP/CREB jelátviteli útvonalat, amely az UV-indukált bőrhiperpigmentáció fő mechanizmusa. [36,37]. Ezért azt feltételeztük, hogy a cAMP-szintet csökkentő adrenerg blokkolók csökkentikmelanin szintézis.
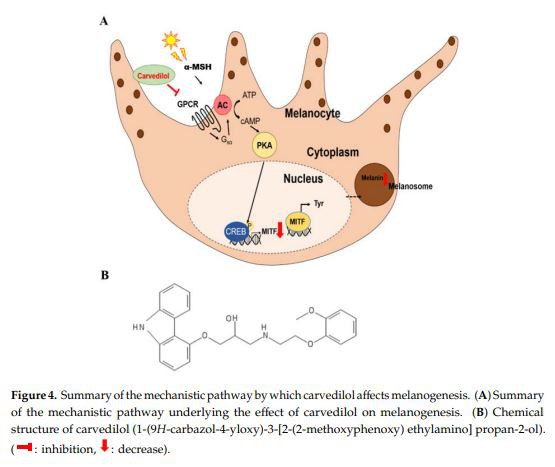
Ezen kívül, hogy dolgozzon biztonságosfehérítésAz antimelanogenezis megbízható és reprodukálható mechanizmusait párhuzamosan kell folytatni. Élettanilag legjelentősebb inger az UV, és az UVR jelátvitel között az epidermális felémelanociták, a CREB tengely a melanogenezis szabályozásának legmegbízhatóbb módja az emberi epidermiszben [29]. Az UV-expozíció egymás után aktiválja a cAMP termelést, a PKA-t és a CREB transzkripciós faktort, ami viszont indukálja a MITF és a downstream cél melanogén gének expresszióját [38,39]. A PKA által végzett CREB-foszforiláció mellett a közelmúltban végzett vizsgálatok kimutatták, hogy a cAMP-stimulált MITF-hez a CREB-szabályozott transzkripciós koaktivátor (CRTC) 3 CREB transzkripciós komplexbe történő felvétele is szükséges. A MITF a leglényegesebb szerepet tölti be a szabályozásbanmelanin szintézisés a melanogén enzimek ebből eredő transzkripciója [26,40,41]. Ezen intracelluláris jelátviteli folyamat során a melanogenezist egy kulcsenzim, a tirozináz és további enzimatikus fehérjék, például a TRP-1 és a DCT [1–4] szabályozzák. Jelen tanulmányban a karvedilol hatékonyan csökkentette a CREB foszforilációját, ami azt jelzi, hogy csökkentette a MITF és a tirozináz fehérjéket azáltal, hogy gátolta a MITF transzkripciót (4. ábra). Figyelembe véve, hogy a MITF mRNS génszabályozását bonyolultan szabályozzák és megmentik más intracelluláris jelátviteli molekulák és koaktivátorok, a MITF transzkripciós szintű szabályozása ígéretes stratégia az egészséges bőrfehérítő összetevők feltárására, mivel a MITF túlélési funkciója megmarad és megmenthető [1,38,40]. Valójában, amikor az FSK-indukált MITF transzkripciót vizsgáltuk, az MITF mRNS-nek saját csúcsválasz görbéje van a melanogenezis és a sejtes túlélés szempontjából a celluláris homeosztázis szempontjából. A biológiai funkcióimelanocitákúgy tűnt, hogy alapvetően más visszacsatolási jelek szabályozzák az emberi melanocitákban. Ezenkívül a carvedilolnak kisebb a kockázata a hipopigmentáció nemkívánatos eseményeinek, mivel idővel gyengíti a sejt tirozináz aktivitását, nem pedig hirtelen.
A katekolaminok közé tartozik a dopamin, az adrenalin és a noradrenalin, és enzimek hatására az étrendi tirozinból szintetizálódnak [42]. A katekolaminok bioszintézise és lebomlása a sejtek széles körében zajlik, beleértve a szimpatikus idegek és az agy neuronjait, az adrenomedulláris sejteket, az endothel sejteket, a neutrofileket és a mononukleáris sejteket [43–45]. Az emberi bőrben a katekolamin-szintézis a keratinocitákban megy végbe. Ezzel szemben a melanociták mRNS-t és enzimeket is expresszálnak a noradrenalin autokrin szintéziséhez, de az epinefrint nem [7,42]. Emberbenmelanociták, -1-AR fontos lehet a noradrenalinra adott reakcióban, demelanin szintézisa funkcionális 2-ARsignaling [7,8] is befolyásolja. Érdekes módon a vitiligóban szenvedő betegeknél megnőtt az 2-AR-sűrűség a keratinocitákban [46]. A nem szegmentális vitiligóban szenvedő betegek vizeletében és plazmájában megemelkedett a noradrenalin szint, ami arra utal, hogy a katekolamin-anyagcsere összefüggésbe hozható a vitiligo kialakulásával és progressziójával. [47]. Ezenkívül a klasszikus stressz neurotranszmitterek mellett a melanociták neuropeptideket és hormonokat termelnek, mint például a kortikotropin-felszabadító faktor és a proopiomelanokortin. Ezt a termelést az UVR és más, a bőr neuroendokrin rendszerében ható szerek stimulálják [48]. Ezért a katekolaminok hatása és a melanocita funkció szorosan összefügg számos összetett útvonalon. Ezenkívül a karvedilol megzavarhatja a melanogén útvonal kémiai reakcióit, és ezt a lehetőséget tovább kell vizsgálni. A carvedilol előnyökkel járhat, mivel egyidejűleg gyulladáscsökkentő hatása is van, mivel a legtöbb hiperpigmentáris rendellenesség klinikailag vagy szubklinikailag PHI a sötét bőrű betegeknél. Mivel a carvedilol bőrön keresztüli átjutását in vitro és ex vivo is tanulmányozták, a carvedilol helyi gyógyszerként is kifejleszthető.fehérítésügynök a jövőben [49–51].
A karvedilol szisztémás alkalmazása bradycardiát, szédülést, hipotenziót, fejfájást és szédülést okozhat. A carvedilol helyi alkalmazása általában nem okoz szisztémás tüneteket, azonban ezekre a tünetekre fokozottan ügyelnünk kell, ha bőrproblémákkal küzdő, például atópiás dermatitiszben szenvedő betegeknél alkalmazzuk. Ezenkívül ritka esetekben ekcémát, viszketést és lichenoid kitörést jelentettek a karvedilol szedése során. Ezeket a bőrgyógyászati mellékhatásokat, valamint a kontaktdermatitist is figyelembe kell venni a carvedilol helyi alkalmazásánál.fehérítésügynök.
Összefoglalva, kimutattuk, hogy a karvedilol hatékonyan csökkentette a melanogenezist humánbanmelanocitákés ex vivo emberi bőr a cAMP/CREB/MITF útvonal gátlásával, ami arra utal, hogy hatékony fehérítőszerként használható. A karvedilol humán melanocitákban az adrenerg-kreceptor funkcionális szerepének további vizsgálatát kell követni.
4. Anyagok és módszerek
4.1. Anyagok
A karvedilolt, a 3-4-dihidroxi-L-fenilalanint (L-DOPA), a koleratoxint (CT) és az 12-otetradekanoilforbol-13--acetátot (TPA) a Sigma-Aldrich Co.-tól vásárolták. (St. Louis, MO, USA). A Dulbecco's Modified Eagle's Medium (DMEM) és a Dulbecco's foszfáttal pufferolt sóoldat a WelGENE-től (Daegu, Korea) vásárolt. A magzati szarvasmarha szérumot (FBS), az antibiotikum-antimikotikumot és a tripszin-EDTA-t a Gibco-tól (Grand Island, NY, USA) vásároltuk. 254-es médium (CascadeBiologics, Portland, OR, USA) és FSK ([3R-(3,4a,5,6,6a,10,10a,10b)]-5-(acetiloxi)-3-etenildodekahidro{ {24}},10,10b-trihidroxi-3,4a,7,7,10a-pentametil-1H-nafto[2,1-b]pirán-1-on ) a Tocris Bioscience-től (Bristol, Egyesült Királyság) vásárolták.
4.2. Sejtvonalak és sejtkultúra
Az Invitrogentől (Carlsbad, CA, USA) beszerzett elsődleges NHM-eket 254-es táptalajban (Thermo Fisher, Waltham, MA, USA) tartottuk humán melanocita növekedési kiegészítéssel (Thermo Fisher) kiegészítve. A Mel-ab sejteket, egy egéreredetű spontán immortalizált melanocita sejtvonalat a Korean Cell Line Bank-tól (KCLB, Seoul, Korea) szereztük be, és DMEM-ben tartották, amelyet 10% FBS-sel, penicillin-sztreptomicinnel, 100 nM TPA-val és 1 nM-mal kiegészítettek. CT. Minden sejtet rutinszerűen 37 °C-on tartottunk párásított, 5 százalékos CO2-tartalmú környezetben.
4.3. Antitestek és Western blot
A sejteket egyszer mostuk hideg PBS-sel, és fehérje lízis pufferben (1% SDS 10 mMTris-ben és 5 mM EDTA, pH 7,4) lizáltuk, majd 98 ◦C-on 10 percig inkubáltuk. A fehérjemintákat 8 százalékos SDS-poliakrilamid gélelektroforézissel választottuk el, nitrocellulóz membránokra blottoltuk (GE Healthcare Life Sciences, Chicago, IL, USA), majd blokkoltuk 0,5 százalék Tween 20 és 5 százalék BSA-t tartalmazó Tris-pufferolt sóoldattal, és immunblot vizsgálatnak vetik alá. A tirozináz és TRP{14}} antitesteket a Santa Cruz Biotechnology-tól (Dallas, TX, USA), az MITF-et pedig az Abcamtól (Cambridge, Egyesült Királyság) vásárolták. -tubulint (Gentex, Holland, MI, USA) használtunk belső terhelési kontrollként.
4.4. Melanin tartalom
A karvedilol citotoxikus hatását az Ez-Cytox Cell Viability Assay Kit (Dogen-Bio Co., Ltd., Szöul, Korea) segítségével értékelték ki a gyártó utasításai szerint. A Mel-Ab sejteket és az NHM-eket hatlyukú lemezekre oltottuk. 6 × 105 és 3 × 105 sejt/lyuk sűrűséggel. A sejteket karvedilollal kezeltük, amint az az ábrákon látható, 3 vagy 5 napig (d). A melanintartalom mérése előtt a sejteket fáziskontraszt mikroszkóp alatt megfigyeltük és lefényképeztük (Olympus, Tokió, Japán). A sejteket 550 µl 1 N NaOH-ban oldottuk fel 100 °C-on 30 percig, és 13, 000 fordulatszámmal 5 percig centrifugáltuk. A felülúszók abszorbanciáját 405 nm-en mértük mikrolemez-leolvasóval. Az intracelluláris melanin tartalmat a sejtek kezeletlen kontrolljához viszonyított százalékban mutattuk be. Arbutint (100 mg/ml) használtunk pozitív kontrollként.
4.5. Celluláris tirozináz aktivitás
A tirozináz aktivitást az L-DOPA dopakróm képződési sebességének mérésével értékeltük. Carvedilollal való inkubálás után a sejteket jéghideg PBS-ben mostuk, és tirozináz lízispufferben (foszfát puffer, pH 6,8, 1% Triton X{-t tartalmazó) lizáltuk. {5}}) ismételt fagyasztási/olvadási ciklusokkal. A lizátumokat centrifugálással tisztítottuk 15, 000 fordulat/perc 4 ◦ C-on 10 percig. A lizátum fehérjeszintjének mennyiségi meghatározása és a fehérjekoncentráció lízispufferrel történő beállítása után 90 µl felülúszót 10 µl 10 mM L-DOPA-val keverve tirozináz lízispufferben inkubáltunk 37 °C-on. A celluláris aktivitást tirozináz mérésével mértük 475 nm mikroplatereaderrel 10 percenként legalább 1 órán keresztül. Arbutint (100 mg/ml) használtunk pozitív kontrollként.

gyógynövényes tartályok
4.6. Immunhisztokémiai elemzés
A paraffinba ágyazott emberi bőrszöveteket 6-µm vastag metszetekre vágtuk, és Melan-A-val (Novocastra, Newcastle, Egyesült Királyság), Fontana-Masson készletekkel (ID Labs, London, ON, Kanada) és HMB45-tel (Santa Clara) festették. , CA, USA), a gyártó utasításai szerint. A melanin indexet úgy határoztuk meg, hogy megmértük a festett terület százalékos arányát a teljes szövetterülethez viszonyítva ImageJ 1.52a szoftverrel (National Institutes of Health, Bethesda, MD, USA).
4.7. Statisztikai analízis
Az adatokat az átlag ± standard hiba (SEM) formájában mutatjuk be, és a statisztikai szignifikanciát nem párosított Student-féle t-teszttel határoztuk meg GraphPad Prism5 szoftverrel (San Diego, CA, USA). Ebben a vizsgálatban a p < 0.05,="" p="">< 0,01="" és="" p="">< 0,001="" értéket="" tekintettük="" statisztikailag="" szignifikánsnak,="" és="" *,="" **="" és="" ***="" jelöli,="">
Hivatkozások
1. Gillbro, JM; Olsson, MJ A bőrvilágosító szerek melanogenezise és mechanizmusai – meglévő és új megközelítések. Int. J. Cosmet. Sci. 2011, 33, 210–221. [CrossRef] [PubMed]
2. Lee, YJ; Shin, HJ; Nem, TK; Choi, KH; Chang, SE Melasma és gyulladás utáni hiperpigmentáció kezelése pikoszekundumos 755- nm-es alexandritlézerrel ázsiai betegeknél. Ann. Dermatol. 2017, 29 779–781. [CrossRef] [PubMed]
3. Lee, YJ; Park, JH; Lee, DY; Lee, JH kétoldali diszpigmentációt szerzett az arcon és a nyakon: Klinikailag megfelelő megközelítések. J. Korean Med. Sci. 2016, 31, 2042–2050. [CrossRef] [PubMed]
4. Kang, HJ; Na, JI; Lee, JH; Roh, MR; Ko, JY; Chang, SE Posztinflammatorikus hiperpigmentáció, amely a szoláris lentigines kezeléséhez kapcsolódik Q-Switched 532-nm Nd: YAG lézer: A multicenter felmérés.J. Bőrgyógyász. Csemege. 2017, 28, 447–451. [CrossRef] [PubMed]
5. Kato, H.; Araki, J.; Eto, H.; Doi, K.; Hirai, R.; Kuno, S.; Higashino, T.; Yoshimura, K. Egy prospektív, randomizált, kontrollált vizsgálat orális tranexámsavról a gyulladás utáni hiperpigmentáció megelőzésére Q-kapcsolt rubinlézer után. Dermatol. Surg. 2011, 37, 605–610. [CrossRef] [PubMed]
6. Taylor, CR; Anderson, RR A refrakter melasma és a gyulladás utáni hiperpigmentáció hatástalan kezelése Q-kapcsolt rubinlézerrel. J. Dermatol. Surg. Oncol. 1994, 20, 592–597. [CrossRef]
7. Gillbro, JM; Marles, LK; Hibberts, NA; Schallreuter, KU Az autokrin katekolamin bioszintézis és a béta-adrenoceptor jel elősegíti a pigmentációt az emberi epidermális melanocitákban. J. Investig. Dermatol.2004, 123, 346–353. [CrossRef]
8. Schallreuter, KU; Korner, C.; Pittelkow, MR; Swanson, NN; Gardner, ML Az alfa-1-adrenoreceptor jelátviteli rendszer indukciója emberi melanocitákon. Exp. Dermatol. 1996, 5, 20–23.[CrossRef]
9. Sivamani, RK; Shi, B.; Griffiths, E.; Vu, SM; Lev-Tov, HA; Dahle, S.; Chigbrow, M.; La, TD; Mashburn, C.; Peavy, TR; et al. Az akut sebzés megváltoztatja a béta{2}}adrenerg jelátvitelt és a katekolamin szintetikus útvonalakat a keratinocitákban. J. Investig. Dermatol. 2014, 134, 2258–2266. [CrossRef]
10. Emery, AC katekolamin receptorok: Prototípusok a GPCR-alapú gyógyszerkutatáshoz. Adv. Pharmacol. 2013, 68 335–356.
11. Do Vale, GT; Ceron, CS; Gonzaga, NA; Simplicio, JA; Padovan, JC A béta-blokkolók három generációja: előzmények, osztálybeli különbségek és klinikai alkalmazhatóság. Curr. Hipertónia. Rev. 2019, 15, 22–31. [PubMed]
12. McTavish, D.; Campoli-Richards, D.; Sorkin, EM Carvedilol: Farmakodinámiás és farmakokinetikai tulajdonságainak, valamint terápiás hatékonyságának áttekintése. Drugs 1993, 45, 232–258. [CrossRef] [PubMed]
13. Hsu, CC; Lee, JY Kifejezett arckipirulás és tartós rosacea erythema, amelyet hatékonyan kezelt a carvedilol, egy nem szelektív béta-adrenerg blokkoló. J. Am. Acad. Dermatol. 2012, 67, 491–493. [CrossRef][PubMed]
14. Pietschke, K.; Schaller, M. Különleges arckipirulás és tartós erythema ofrosacea hosszú távú kezelése carvedilol-kezeléssel. J. Dermatolog. Csemege. 2018, 29, 310–313. [CrossRef] [PubMed]
15. Chang, A.; Yeung, S.; Thakkar, A.; Huang, KM; Liu, MM; Kanassatega, RS; Parsa, C.; Orlando, R.; Jackson, EK; Andresen, BT; et al. A bőr karcinogenezisének megelőzése a béta-blokkoló karvedilollal. RákPrev. Res. 2015, 8, 27–36. [CrossRef] [PubMed]
16. Chen, M.; Liang, S.; Shahid, A.; Andresen, BT; Huang, Y. A karvedilol béta-blokkoló megakadályozta az egerek epidermális sejtjeinek és a 3D-s emberi rekonstruált bőrnek az ultraibolya sugárzás által közvetített károsodását. Int. J. Mol. Sci. 2020, 21, 798. [CrossRef] [PubMed]
17. Huang, KM; Liang, S.; Yeung, S.; Oiyemhonlan, E.; Cleveland, KH; Parsa, C.; Orlando, R.; Meyskens, FL, Jr.;Andresen, BT; Huang, Y. Helyileg alkalmazott karvedilol gyengíti a szoláris ultraibolya sugárzás által kiváltott bőrkarcinogenezist. Rák Előz. Res. 2017, 10, 598–606. [CrossRef]
18. Brenner, M.; Hallás, VJ A melanin védő szerepe az UV-károsodással szemben az emberi bőrben. Photochem.Photobiol. 2008, 84, 539–549.
19. Cleveland, KH; Liang, S.; Chang, A.; Huang, KM; Chen, S.; Guo, L.; Huang, Y.; Andresen, BT Carvedilolin gátolja az EGF által közvetített JB6 P plusz telepképződést az adrenoceptoroktól független mechanizmuson keresztül.PLoS ONE 2019, 14, e0217038. [CrossRef]
20. Dzong, G.; Zhongbing, M.; Qinye, F.; Zhigang, Y. A Carvedilol elnyomja a rosszindulatú emlősejtek migrációját és invázióját az Src inaktiválásával a cAMP/PKA és a PKCdelta jelátviteli útvonalon. J. Cancer Res. Ther.2014, 10, 998–1003.
21. Rzepka, Z.; Bussman, E.; Beberok, A.; Wrzesniok, D. A tirozintól a melaninig: Jelátviteli útvonalak és a melanogenezist szabályozó tényezők. Postepy Hig. Med. Dosw. Online 2016, 70, 695–708. [CrossRef]
22. Kim, Y.; Cho, JY; Ó, SW; Kang, M.; Lee, SE; Jung, E.; Park, YS; Lee, J. A globuláris adiponektin melanogén jelként hat az emberi epidermális melanocitákban. Br. J. Dermatol. 2018, 179, 689–701. [CrossRef][PubMed]
23. Slominski, A.; Tobin, DJ; Shibahara, S.; Wortsman, J. Melanin pigmentáció emlősök bőrében és hormonális szabályozása. Physiol. Rev. 2004, 84, 1155–1228. [PubMed]
24. Slominski, A.; Zmijewski, MA; Pawelek, J. L-tirozin és L-dihidroxi-fenilalanin, mint a melanociták működésének hormonszerű szabályozói. Pigment Cell Melanoma Res. 2012, 25, 14–27. [CrossRef] [PubMed]
25. Howe, J.; Costantino, R.; Slominski, A. Az L-tirozin melanogenezis indukciójának és szabályozásának feltételezett mechanizmusáról. Acta Derm Venereol. 1991, 71, 150–152.
26. D'Mello, SA; Finlay, GJ; Baguley, Kr. e. Askarian-Amiri, ME Signaling Pathways in Melanogenesis. Int. J. Mol. Sci. 2016, 17, 1144. [CrossRef]
27. Jung, JA; Kim, BJ; Kim, MS; Te, HJ; Yoon, ES; Dhong, ES; Park, SH; Kim, DW A botulinum toxin védő hatása az ultraibolya által kiváltott bőrpigmentáció ellen. Plast. Reconstr. Surg. 2019, 144, 347–356.[CrossRef]
28. Jeong, YM; Ó, WK; Tran, TL; Kim, WK; Sung, SH; Bae, K.; Lee, S.; Sung, JH Az Rh4 aglikonja gátolja a melanin szintézist B16 melanoma sejtekben: A protein kinase A útvonal lehetséges érintettsége.Biosci. Biotechnol. Biochem. 2013, 77, 119–125. [CrossRef]
29. Kim, YH; Kim, D.; Hong, AR; Kim, JH; Yoo, H.; Kim, J.; Kim, I.; Kang, SW; Chang, SE; Song, Y. Therapeutic Potential of Rottlerin for Skin Hyperpigmentary Disorders by Inhibiting the TranscriptionalActivity of CREB-Regulated Transcription Coactivators. J. Investig. Dermatol. 2019, 139, 2359–2367.e2.[CrossRef]
30. Das, A.; Ghosh, A.; Kumar, P. Kémiai leukoderma hidrokinon miatt: szokatlan jelenség. indiai J. Dermatol. Venereol. Leprol. 2019, 85, 567. [CrossRef]
31. Jow, T.; Hantash, BM Hidrokinon által kiváltott depigmentáció: Esettanulmány és szakirodalmi áttekintés. Dermatitis 2014, 25, e1–e5. [CrossRef]
32. Kersey, P.; Stevenson, CJ Vitiligo és a hidrokinon munkahelyi expozíciója az önfényképezőgépek szervizeléséből. Forduljon a Dermathoz. 1981, 7, 285–287. [CrossRef] [PubMed]
33. Sasaki, M.; Kondo, M.; Sato, K.; Umeda, M.; Kawabata, K.; Takahashi, Y.; Suzuki, T.; Matsunaga, K.; Inoue, S. A Rhododendron egy depigmentációt indukáló fenolos vegyület, melanocita citotoxicitást fejt ki tirozináz-függő mechanizmuson keresztül. Pigment Cell Melanoma Res. 2014, 27, 754–763. [CrossRef] [PubMed]
34. Yoshikawa, M.; Sumikava, Y.; Hida, T.; Kamiya, T.; Kase, K.; Ishii-Osai, Y.; Kato, J.; Kan, Y.; Kamiya, S.; Sato, Y.; et al. Klinikai és epidemiológiai elemzés 149 rododendron okozta leukoderma esetében.J. Dermatol. 2017, 44, 582–587. [CrossRef] [PubMed]
35. Harris, JE. Vegyi anyagokkal indukált vitiligo. Dermatol. Clin. 2017, 35, 151–161. [CrossRef] [PubMed]
36. Li-Sha, G.; Yi-He, C.; Na-Dan, Z.; Teng, Z.; Yue-Chun, L. A carvedilol-kezelés hatásai a szív cAMP-válasz elemkötő fehérje expressziójára és foszforilációjára akut coxsackievírus B3-indukált szívizomgyulladásban. BMC Cardiovasc. Zavar. 2013, 13, 100. [CrossRef] [PubMed]
37. Zhang, F.; A béta(1)-adrenerg receptor Steinberg, SF S49G és R389G polimorfizmusa befolyásolja a jelátvitelt a cAMP-PKA és ERK útvonalakon keresztül. Physiol. Genom. 2013, 45, 1186–1192. [CrossRef]
38. Lee, AY; Noh, M. Az epidermális melanogenezis szabályozása cAMP és/vagy PKC jelátviteli útvonalakon keresztül: Insights for the development of hypopigmented agents. Boltív. Pharm. Res. 2013, 36, 792–801. [CrossRef]
39. Garcia-Borron, JC; Abdel-Malek, Z.; Jimenez-Cervantes, C. MC1R, a cAMP útvonal és a nap UV-sugárzására adott válasz: A horizont kiterjesztése a pigmentáción túl. Pigment Cell Melanoma Res. 2014, 27, 699–720.[CrossRef]
40. Lin, CB; Babiarz, L.; Liebel, F.; Roydon Price, E.; Kizoulis, M.; Gendimenico, GJ; Fisher, DE; Seiberg, M. A microphthalmia-asszociált transzkripciós faktor génexpressziójának modulációja megváltoztatja a bőr pigmentációját.J. Investig. Dermatol. 2002, 119, 1330–1340. [CrossRef]
41. Kim, JH; Hong, AR; Kim, YH; Yoo, H.; Kang, SW; Chang, SE; Song, Y. A JNK elnyomja a melanogenezist azáltal, hogy megzavarja a CREB által szabályozott transzkripciós koaktivátor 3-függő MITF expresszióját. Theranostics2020, 10, 4017–4029. [CrossRef] [PubMed]
42. Rios, M.; Habecker, B.; Sasaoka, T.; Eisenhofer, G.; Tian, H.; Landis, S.; Chikaraishi, D.; Roffler-Tarlov, S. A katekolamin szintézist tirozináz közvetíti tirozin-hidroxiláz hiányában. J. Neurosci. 1999,19, 3519–3526. [CrossRef] [PubMed]
43. Cosentino, M.; Marino, F.; Bombelli, R.; Ferrari, M.; Lecchini, S.; Frigo, G. Endogén katekolaminszintézis, metabolizmus, tárolás és felvétel humán neutrofilekben. Life Sci. 1999, 64, 975–981. [CrossRef]
44. Marino, F.; Cosentino, M.; Bombelli, R.; Ferrari, M.; Lecchini, S.; Frigo, G. Endogén katekolamin-szintézis, metabolizmus tárolása és felvétele emberi perifériás vér mononukleáris sejtjeiben. Exp. Hematol.1999, 27, 489–495. [CrossRef]
45. Sorrento, D.; Santulli, G.; Del Giudice, C.; Anastasio, A.; Trimarco, B.; Iaccarino, G. Az endotélsejtek in vitro és in vivo is képesek katekolaminok szintetizálására és felszabadítására. Hypertension 2012, 60, 129–136.[CrossRef] [PubMed]
46. Cucchi, ML; Frattini, P.; Santagostino, G.; Preda, S.; Orecchia, G. A katekolaminok megnövekednek a nem szegmentális vitiligo vizeletében, különösen annak aktív fázisában. Pigment Cell Res. 2003, 16, 111–116. [CrossRef][PubMed]
47. Salzer, BA; Schallreuter, KU Vitiligóban szenvedő betegek személyiségszerkezetének vizsgálata és lehetséges összefüggés a károsodott katekolamin-anyagcserével. Bőrgyógyászat 1995, 190, 109–115. [CrossRef][PubMed]
48. Slominski, A. A melanociták neuroendokrin aktivitása. Exp. Dermatol. 2009, 18, 760–763. [CrossRef]
49. Gannu, R.; Visnu, YV; Kishan, V.; Rao, YM Carvedilol in vitro permeációja sertésbőrön keresztül: A hordozók és a penetrációt fokozó szerek hatása. PDA J. Pharm. Sci. Technol. 2008, 62, 256–263.
50. Kshirsagar, SJ; Bhalekar, MR; Mohapatra, SK Carvedilollal töltött transzdermális gyógyszeradagoló rendszer fejlesztése és értékelése: In vitro és in vivo jellemzési vizsgálat. Drug Dev. Ind. Pharm. 2012,38, 1530–1537. [CrossRef]
51. Tanwar, YS; Chauhan, CS; Sharma, A. Carvedilol transzdermális tapaszok fejlesztése és értékelése.Acta Pharm. 2007, 57, 151–159. [CrossRef] [PubMed]
