A Cistanche Deserticola-ból izolált oligoszacharidok összetételének elemzése és immunológiai aktivitása
Mar 08, 2022
Kapcsolatfelvétel: emily.li@wecistanche.com
Absztrakt.Egy oligoszacharidot (CDOS) szereztünk beCistanche deserticolalúgos (pH{0}}) extrakcióval, etanolos kicsapással és Sephadex G-100 által két tisztított frakcióra (azaz CDOS-1 és CDOS-2) frakcionálva. és Sephadex G{4}} oszlopszűrős kromatográfia. A CDOS monoszacharid összetételét nagy teljesítményű folyadékkromatográfiával (HPLC) vizsgáltuk. Azt találták, hogy a CDOS-1 csak szacharózból, a CDOS-2 pedig főleg szacharózból, ramnózból és mannitból állt, 1:0,73:3,61 mólarány mellett. Az immunológiai tesztek azt mutatták, hogy a CDOS szignifikáns hatást gyakorolt az egér lép indexére, növelve a makrofágok fagocitózis aktivitását és serkentve az antitest-termelő sejtproliferációt. Remélhetőleg a CDOS-t funkcionális élelmiszerré vagy gyógyszerré fejlesztik.
Kulcsszavak:Cistanchedeserticola, oligoszacharid, tisztítás, összetétel, immunológiai aktivitások.

A Cistanche deserticolának számos hatása van, kattintson ide, ha többet szeretne megtudni
1. Bemutatkozás
Cistanchedeserticola YCMa. (Orobanchaceae család) egy rövid élősködő növény, amely Kína északnyugati részén őshonos. Az egész szárított növényt (virágok nélkül) tonikként ismerik, és "Rou Congrong"-nak hívják. A keleti gyógyászatban édes és sós ízű, meleg természetű, és a vese- és vastagbélcsatornáknak tulajdonítják. funkciójaélénkítőazveseés az esszencia kiegészítése, a bél hidratálása és a belek ellazítása [1]-[3]. A modern farmakológiai tanulmányok kimutatták, hogy elősegítheti a DNS-szintézist és késleltetheti a szenilitás folyamatát, növelheti az antioxidáns hatást [4], megelőzheti és kezelheti a szív- és érrendszeri betegségeket [3]. Emellett fájdalomcsillapítót ésanti-gyulladásoshatások [5], fokozzák a tanulást és a memóriát az idegnövekedési faktorok indukálásával [6]. Egyes tanulmányok kimutatták, hogy a C. deserticola kivonatok aktiválhatják az intraabdominális makrofágok fagocita funkcióját egerekben [7]-[9] ésfokozza atest's immunitás[10]. A korábbi tanulmányok szerint ez a növény számos aktív összetevőt tartalmaz, köztük fenil-etanoid glikozidokat, iridoidokat, lignánokat, szacharidokat, alkaloidokat stb. [11] Ahogy a C.deserticolafeniletanoidglikozidokés a poliszacharidokat a fő aktív komponensekként ismerik el, szerkezetükre és bioaktivitásukra számos tanulmány összpontosított az elmúlt évtizedekben [12]-[17]. Ami az értékes oligoszacharidokat illetiC. deserticola, a jelentések meglehetősen korlátozottak. Az oligoszacharidok, egy rövid szénláncú homo- vagy heterocukrokat tartalmazó szacharidok, jól ismertek az emberi életre gyakorolt jótékony hatásukról, és régóta széles körben alkalmazzák [18]. A funkcionális oligoszacharidok, amelyek fiziológiás funkcióval rendelkeznek, mint például az alacsony kariogenitás és a bifidobaktériumok növekedési faktora [19], javítják az emberek és az állatok egészségét. Élelmiszer-összetevőként használták őket. A közelmúltban az oligoszacharidok új funkcióiról számoltak be, amelyek képesek modulálni az emberek, állatok és halak immunrendszerét [20]. Ebben a cikkben a kutatási program eredményeinek első részét, a frakcionálást ismertetjük. A C. deserticola lúgos kivonatából ultraszűréssel és gélpermeációs kromatográfiával kombinált összes oligoszacharidból, valamint ezek összetételének elemzése nagy teljesítményű folyadékkromatográfiával (HPLC). Emellett bemutatjuk a C. deserticola oligoszacharidok immunológiai aktivitását is. Tudomásunk szerint kevés közlemény jelent meg az immunstimuláló aktivitás vizsgálatárólC. deserticolaoligoszacharidok.

2. Kísérleti
2.1. Anyagok
A C. deserticolát az Alxa League-ből (Belső-Mongólia, Kína) termesztették és gyűjtötték be. Kunming egereket (GradeII, hat hetesek) a Belső-Mongólia Egyetem Pharmacology Experimental Centerétől vásároltunk. Sephadex G-100,Sephadex G-25, trifluor-ecetsav (TFA), 1-fenil-3-metil-5- pirazolon (PMP), D-glükóz, D- galaktózt, D-fruktózt, D-xilózt, D-mannózt, D-galakturonsavat, D-glükuronsavat, szacharózt, ramnózt, mannitot, fukózt, ramnózt a Sigmától (St. Louis, MO, USA) vásároltuk. A közepes RPMI-t{12}} a Gibco Invitrogen Co.-tól (San Diego, CA, USA) vásároltuk. Az összes többi vegyszer analitikai minőségű volt.
2.2. Oligoszacharidok kivonása
A C. deserticola szárított testét kisebb darabokra vágtuk, majd malomban porrá őröltük, majd 3x5000 ml vízmentes etanollal extraháltuk 70 fokon légköri nyomáson 3 órán át. A lipidek eltávolítására visszafolyató hűtőt rögzítettünk. A maradékot ezután lúggal (pH=10) extraháltuk 60 fokon háromszor (minden alkalommal 2 órán keresztül). Centrifugálás (2000 g, 15 perc, 20 °C) után a felülúszót a térfogat egytizedére bepároljuk rotációs bepárlóban csökkentett nyomáson 50 °C-on, és szűrjük. Ezután a szűrletet Sevag reagenssel [21] fehérjementesítettük, és aktív szénnel színtelenítettük.
2.3. Oligoszacharidok izolálása és tisztítása
A fagyasztva szárított nyers oligoszacharidokat desztillált vízben oldottuk, centrifugáltuk, majd a felülúszót Sephadex G-100 oszlopon (1×50 cm) tisztítottuk, amelyet ultratiszta vízzel ekvilibráltunk. A mintával való feltöltést követően az oszlopot ultratiszta vízzel eluáltuk 5 ml/perc áramlási sebességgel. A különböző frakciókat kémcsövek segítségével gyűjtöttük össze. Az egyes csövek teljes szénhidráttartalmát 490 nm-en mértük fenol-H2SO4 módszerrel [22]. A vízzel eluált oldatot két CDOS-1 és CDO-2 frakcióra osztottuk. Két frakciót Sephadex G-25 oszlopon (2,7 × 85 cm) tisztítottunk tovább ultratiszta vízzel (1 ml/perc áramlási sebességgel). A tisztított frakció összegyűjtése után liofilizáljuk.
2.4. A monoszacharid összetétel elemzése
A CDO-k monoszacharid összetételét HPLC analízissel határoztuk meg. A CDO-kat (2 mg) először 2 M HCl-t tartalmazó vízmentes metanollal hidrolizáltuk 80 fokon 16 órán át nitrogénatmoszférában, majd 2 M TFA-val 120 fokon 1 órán át. Miután a TFA-t bepárlással eltávolítottuk, a hidrolizátumokat ezután PMP-vel derivatizáltuk a leírt módszer szerint [23], és HPLC-vel analizáltuk. A HPLC elválasztást az EF-2002 HPLC rendszeren (KNAUER cég, Németország) végeztük. A PMP származékokat Sugar-PAK térfogat (6,5×300 mm, glasses of water company, America) alkalmazásával kromatografáltuk, és az abszorbanciát 245 nm-en mértük. Az injektált térfogat 20 µl volt, és a PBS-ből (A oldószer) és acetonitrilből (B oldószer) álló mozgó fázist használtuk izokratikus elúcióhoz 82% (A) és 18% (B) térfogatarányban. A teljes HPLC futási idő 40 perc, az áramlási sebesség 0,5 ml/perc.

2.5. Immunbiológiai tevékenységek
2.5.1. A monocita-makrofág fagocita funkciója
Hatvan Kunming egeret (GradeII, hat hetes) a Belső-Mongólia Egyetem Farmakológiai Kísérleti Központjától vásároltunk, és használat előtt 1 hétig akklimatizáltuk. Az összes egeret véletlenszerűen négy csoportra osztották, amelyek a sóoldat-kontroll csoportból, a magas CDO-dózisú csoportból, a közepes dózisú csoportból és az alacsony CDO-dózisú csoportból álltak. Az egereket intraperitoneálisan 0,5 ml oligoszacharid oldattal injekcióztuk naponta egyszer 5 napon keresztül. A magas, közepes vagy alacsony CDO dózisú csoport 10{{10}}, 50 vagy 25 mg/kg/ttkg CDO-t kapott; és 0,5 ml sóoldatot injektáltunk a kontrollcsoportba. A hetedik napon szénrészecske-tisztulási kísérletet végeztünk Hou [24] szerint, és megmértük a lépindexet és a csecsemőmirigy indexet. Röviden, 0,05 ml/10 g/bw India tintát fecskendeztünk minden egérbe a vena caudalison keresztül, majd 20 µl vért vettünk a vena orbitalis posteriorból 3 és 7 perccel az injekció beadása után. A vérmintákat 2 ml 0,1 százalékos Na2CO3-at tartalmazó csövekbe helyeztük, és az OD értékeket 600 nm-en mértük. A clearance indexet (K), a fagocita indexet ( ) és az immunszervi indexet a következőképpen számítottuk ki (1), a t2 és t1 7 percet, illetve 3 percet jelent.
2.5.2. Az antitestet termelő sejtszaporodás
Kunming egerek csoportjait (csoportonként ötöt) 2 x 107 SRBC intraperitoneális injekciójával immunizáltuk 1,0 ml PBS-ben, hozzáadva 50 ug tesztanyagot (egyik sem volt a kontrollban). Egy héttel később Kunming egerekből származó lépsejteket (2 ml-enként 106 sejt/lyuk) tenyésztettünk tesztanyaggal vagy anélkül 72 órán át 10% RPMI 1640 tápközegben 5% CO2 légkörben, tenyészetenként három párhuzamosban. Meghatároztuk az SRBC elleni PFC számát 106 lépsejtekre vonatkoztatva [25], [26].
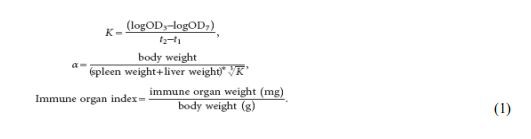
2.6. Statisztikai analízis
Az adatokat átlagértékek ±SD-ben fejeztük ki. A vizsgált csoportok és a kontroll közötti különbséget Student-féle t-próbával elemeztük. P < 0,05="" volt="">

3. Eredmények és megbeszélés
3.1. Oligoszacharidok izolálása és tisztítása
A CDO-kat a C. deserticola szárított testének lúgos kivonatából izoláltuk 3.07 százalékos hozammal. A CDOS-1 és CDOS-2 két frakcióját különítettük el desztillált vizes eluátumból a Sephadex G-100 oszlopon (1. ábra). A CDOS-1 és CDOS-2 tisztított frakciói egyetlen csúcsot mutattak a Sephadex G-25 oszlopon, ami azt jelzi, hogy a mintában nem volt jelen más oligoszacharid. A monoszacharid-összetételek eredményei azt mutatták, hogy a CDOS-1 csak szacharózból (2. ábra), a CDOS-2 pedig főként szacharózból, ramnózból és mannitból (3. ábra) állt, mólarány mellett. 1:0,73:3,61-ből.

3.2. A CDO-k immunbiológiai aktivitásai
Számos in vivo és in vitro bizonyíték igazolta, hogy a természetes oligoszacharidok immunmoduláló funkciót mutattak azáltal, hogy stimulálják mind a sejtes, mind a humorális.immunis válaszokat[27], [28]. Ebben a cikkben 100 mg/kg/ttkg CDO-k növelték az egér lépindexét, de nem volt szignifikáns különbség a csecsemőmirigy-indexben a kezelt és a kontrollcsoportok között (1. táblázat). A makrofágok fontos összetevői a gazdaszervezet vírusfertőzés elleni védekezésének, mivel gátolják a vírusok intracelluláris replikációját és elpusztítják a vírussal fertőzött sejteket [29]. Amikor aktiválódnak, számos oxigén vagy nitrogén köztitermék és citokin szabadul fel a makrofágokból, és számos fontos biológiai funkcióban vesznek részt, például gyulladásgátló és daganatellenes aktivitásban [30]-[32]. Ezért a makrofágok fagocitáló aktivitása a szervezet immunfunkcióinak fontos mutatója. Ebben a vizsgálatban a mérsékelt és nagy dózisú CDO-k növelték a makrofágok fagocitózis aktivitását (1. táblázat). A CDO-k által kiváltott antitest-termelő sejtproliferációt a hemolitikus PFC növekedésének vizsgálatával vizsgáltuk Kunming egerek lépében, amelyeket SRBC-vel és a tesztmintával immunizáltunk. Az eredmények azt mutatták, hogy a mérsékelt és nagy dózisú CDO-k szignifikánsan fokozzák az antitest-termelő sejtproliferációt (2. táblázat). A nagy dózisú CDO-k rendkívül jelentős növekedést okoztak a PFC-számban (P <>

Hivatkozások
[1] J. Li, Y. Jiang, R. Fan. Biológiai jelek vegyes felismerése hullámelemzés alapján. In: Y. Jiang és munkatársai (szerk.). Proc. az Egyesült Királyság-Kína Sportmérnöki Műhelytől. Liverpool: Akadémiai Világszövetség. 2007, 1-8.
[2] J. Ouyang, XD Wang, B. Zhao és mtsai. Ritkaföldfém elemek hatása a Cistanche deserticola sejtek növekedésére és a fenil-etanoid glikozidok termelésére. JB io-technol, 2003, 102 (2): 129-134
[3] Xu Zhaohui, Yang Junshan, Lu Ruimian és mások. A Cistanche deserticola YCMA új természetes terméke. Journal of Chinese Pharmaceutical Sciences, 1999, 8(2):61-63.
[4] X. Wang, L. Li, Muhuyati, X. Wanag, N. Du. A Cistanche glikozidjainak antioxidáns hatása az egerek szövetében. Zhongguo Zhong Yao Za Zhi. 1998, 23(9):554-5.
[5] Lin LW, Hsieh MT, Tsai FH, Wang WH, Wu CRA Cistanche deserticola által okozott antinociceptív és gyulladáscsökkentő aktivitás rágcsálókban. J Ethnopharmacol. 2002, 83(3):177-82.
[6] Choi, JG; Hold, M; Jeong, HU; Kim, MC; Kim, SY; Ó, az MS Cistanches Herba javítja a tanulást és a memóriát az idegnövekedési faktor indukálásával. Viselkedési agykutatás. 2011, 216 (2): 652–8.
[7] Zong G, He W, Wu G, Chen M, Shen X, Shi M. Cistanche deserticola YC Ma és C, tubulosa (Shenk) Wight összehasonlítása néhány farmakológiai hatásról.Zhongguo Zhong Yao Za Zhi. 1996, 21(7):436-7.
[8] He W, Shu XF, Zeng GZ és mások. A C. deserticola szexuális potenciájának fokozásának vizsgálata. J Chin Med. 1996, 21(9): 534- 537.
[9] Zeng GZ, He W, Wu GL et al. A Cistanche deserticola YC Ma és a C. tubulosa súlyának összehasonlítása egyes farmakológiai hatások tekintetében. J Chin Med. 1996, 21(7): 436-438.
[10] Zeng QL, Zheng YF, Lu ZL A Cistanche deserticola YC Ma poliszacharidjának immunmoduláló hatásai. J Zhejiang Univ, Med Sci. 2002, 31(4): 284- 287.
[11] Li Yuan, Song Yuanyuan, Zhang Hongquan. Előrelépések a kémiai összetevők kutatásában és a Cistanche gyógyászati tevékenységében. Chinese Wild Plant Resources, 2010, 29(1):7-11.
[12] Du NS, Wang H, Yi YH. Fenil-etanol-glikozidok izolálása és azonosítása Cistanche deserticolából. Nat Prod R&D, 1993, 5(4): 5- 8.
[13] Lu NS, Liu JL Fenil-etanol-glikozidok meghatározása Cistanche deserticolában makroretikuláris gyanta-spektrofotometriával. Nat Prod R&D, 1993, 5(3): 30-33.
[14] Xiong QB, Tezuka Y, Kaneko T és mások. A nitrogén-monoxid gátlása feniletanoidokkal aktivált makrofágokban.
European Journal of Pharmacology, 2000, 400: 137- 144.
[15] Zhao Wei, Yan Hong, Liang Zhong-Yan és mások. A Cistanche Deserticola Ma szárából izolált vízben oldódó poliszacharid SPA szerkezeti elemzése. Chemical Journal of Chinese Universities, 2005, 26(3):461-463.
[16] Wang Xiangyan. Tanulmány a Cistanche deserticola poliszacharidjainak immunfarmakológiájáról és abszorpciós jellegéről. 2011, No.S1, Medicine and Health Sciences, E057-235-1-70.
[17] Xiong Q, Hase K, Tezuka Y, Tani T, Namba T, Kadota S. Hepatoprotective activity of phenylethanoids from Cistanche deserticola. Planta Med. 1998, 64(2):120-5.
[18] Handbook of Amylases and Related Enzymes (szerk.: The Amylase Research Society of Japan), Pergamon Press (1988)
[19] Araya, S. (szerk.) Proceedings of the 5th Conference on Dental Caries and Coupling Sugar (japánul), National Institute of Health, Tokió (1980)
[20] Kodo Otaka. A funkcionális oligoszacharid és új aspektusa, mint immunmoduláció. J. Biol. Macromol. 2006, 6(1), 3-9.
[21] Navarini L, Gilli R, Gombac V, Abatangelo A, Bosco M, Toffanin R. Pörkölt Coffea arabica bab forró vizes kivonataiból származó poliszacharidok: Izolálás és jellemzés. szénhidrát. Polym.1999, 40:71–81.
[22] Dubois M, Gilles KA, Hamilton JK, Rebers PA, Smith F. Kolorimetriás módszer cukrok és rokon anyagok meghatározására. Anális. Chem. 1956, 28:350–356.
[23] Yang X, Zhao Y, Wang Q, Wang H, Mei Q. Angelica poliszacharidok monoszacharid komponenseinek elemzése nagy teljesítményű folyadékkromatográfiával. Anal Sci. 2005, 21:1177–1180.
[24] Yufang Hou, Yubao Hou, Liu Yanyan és mások. A lektin kivonása és tisztítása vörös vesebabból, valamint a lektin és négy kínai gyógynövény poliszacharid előzetes immunfunkciós vizsgálata. Journal of Biomedicine and Biotechnology, 2010:1-9.
[25] Cunningham, AJ és A. Szenberg. További fejlesztések az egyedi antitest-képző sejtek kimutatására szolgáló plakk technikában. Immunology.1968, 14:599-600.
[26] Haruhiko Takada, Tomohiko Ogawa, Fuminobu Yoshimura és mások. Fusobacterium nucleatum ATCC 10953 [J]-ból izolált porinfrakció immunbiológiai aktivitásai. Fertőzés és immunitás. 1988, 56(4): 855-863.
[27] Wang MQ, Guilbert LJ, Ling L, Li J, Wu YQ, Xu SR, Pang P, Shan JJ A CVT-E002 immunmoduláló hatása: az észak-amerikai ginzeng (Panax quinque folium) szabadalmaztatott kivonata. J Pharm Pharmacol.2001, 53:1515–1523.
[28] Nergard CS, Kiyohara H, Reynolds JC, Thomas-Oates JE, Matsumoto T, Yamada H, Patel T, Petersen D, Michaelsen TE, Diallo D, Paulsen BS Három mitogén és komplement-fixáló szerkezete és szerkezet-aktivitás kapcsolatai pektikus arabinogalaktánok a Cochlospermum tinctorium A. Rich mali fekélyellenes növényekből és a Vernonia kotschyana Sch Bip. ex Walp. Biomakromolekulák. 2006, 7:71–79.
[29] E.-M. Choi, A.-J. Kim, Y.-O. Kim és J.-K. Hwang, Az arabinogalaktán és a fukoidán immunmoduláló hatása in vitro. Journal of Medicinal Food. 2005, 8(4):446–453.
[30] Y. Chen, J.-A. Duan, D. Qian és mtsai. Az Angelica Sinensis négy vízoldható frakciójának immunregulációs aktivitásának értékelése és összehasonlítása in vitro peritoneális makrofágokon ICR egerekben. Nemzetközi immunfarmakológia. 2010, 10:422–430.
[31] YS Lee, OK Han, CW Park és társai. A vizes extrahált Astragali radix gyulladásos citokingén-expressziója és nitrogén-monoxid-szabályozása RAW 264.7 makrofág sejtekben. Journal of Ethnopharmacology. 2005, 100(3): 289–294.
[32] KY Lee és YJ Jeon. A Poria cocos sclerotiumból izolált poliszacharid NF-κB/Rel aktivációt és iNOS expressziót indukál rágcsáló makrofágokban. Nemzetközi immunfarmakológia. 2003, 3(10-11): 1353–1362.
