A Shenkang hatása a vesefibrózisra és a vese intersticiális fibroblasztjainak aktiválására a JAK2/STAT3 útvonalon keresztül
Feb 27, 2022
Háttér
A krónikus vesebetegség (CKD) számos különböző betegség eredménye, amelyek visszafordíthatatlanul károsítják a vesét, és különféle szövődményeket okoznak a betegekben [1]. A dialízis alatt álló betegek életminősége nagymértékben romlik, és az orvosi költségek is nagyon magasak [2]. Az elsődleges kóros folyamatvesekárosodásnormálishoz vezetvese-parenchyma pusztulása és progresszív hegszövetképződés, ami végső soron fibrózishoz vezet. Vesea fibrózis magában foglalja a tubuláris intersticiális fibrózist és a glomerulosclerosisot [3], amelyek arenális szövet és a funkció elvesztése.VeseA tubulointerstitialis fibrózis szinte minden CKD progresszív kifejlődésének tipikus útja, és a végstádium fő patológiás alapjavesebetegség,amelyet tubuláris epiteliális sejtsorvadás, gyulladásos sejtek infiltrációja, aberráns aktiváció és növekedés jellemez.vese-fibroblasztok és túlzott extracelluláris mátrix (ECM) felhalmozódása [4, 5]. Az effektor sejtek, a -simaizom aktin ( -SMA)-pozitív miofibroblasztok szintetizálják és szekretálják az ECM-et. Az intersticiális fibroblasztok myofibroblasztokká történő aktiválása segíthet a sérült szövetek helyreállításában. Ha azonban ez a helyreállítási folyamat abnormális, és túlzott ECM választódik ki, visszafordíthatatlan vesekárosodás következik be. Ennek megfelelően a myofibroblaszt aktivációt közvetítő jelátviteli útvonal célpont lehet avese-fibrózis.

A CISTANCHE JAVÍTJA A VESE-/VESEBETEGSÉGET
A Janus kináz/jelátalakító és transzkripciós aktivátor (JAK/STAT) útvonal egy pleiotróp jelátviteli kaszkád több növekedési faktor és citokin számára [6], amely számos sejtfunkciót közvetít, beleértve a sejtek túlélését és proliferációját [7]. A STAT3-at a Tyr705-nél a Janus-kinázon keresztüli tirozin (Tyr) foszforiláció aktiválja, válaszul számos növekedési faktorra és citokinre, beleértve a transzformáló növekedési faktort (TGF-) [8]. A foszforilált STAT3 dimereket képez, amelyek azután a sejtmagba kerülnek, ahol közvetlenül kötődnek a DNS-szekvenciához, és szabályozzák a célgének expresszióját [9]. A STAT3 és JAK2 aktivációja fokozódik a fibrogén vese interstitialis fibroblasztokban, amelyeket egyoldali ureterelzáródás (UUO) indukál [10, 11]. A STAT3 foszforilációjának növekedését a TGF- -kezelt NRK-49F sejtekben is megfigyelték [12].
A krónikus vesebetegség jelenlegi, széles körben alkalmazott kezelését gyakran nem kielégítő hatások [13] és gyakori mellékhatások kísérik. Ezért nagy jelentősége van a CKD előfordulásának és kialakulásának megelőzésére és ellenőrzésére szolgáló hatékony kezelési intézkedések vizsgálatának és azonosításának, a betegek prognózisának javítása érdekében. A Shenkang (SK) egy gyakran használt gyógynövény formula, amely rebarbarát (Rheum palmatum L. vagy R. tanguticum Maxim. ex Balf.), vörös zsályát (Salvia miltiorrhiza Bunge), pórsáfrányt (Carthamus tinctorius L.) és astragalust (Astragalus mongholicus) tartalmaz. Bunge). Az 1990-es évek óta az SK-t Kínában a krónikus vesebetegség és a kapcsolódó betegségek, köztük a diabéteszes nephropathia (DN) kezelésére használják.veseelégtelenség, glomerulonephritis, krónikus nephritis ésvese-elégtelenség. Nyilvánvaló terápiás hatásaival és kevés mellékhatásával az SK késleltetheti a betegség progressziójátvese-diszfunkció a CKD-ben. Egy 2200 ember bevonásával végzett klinikai vizsgálatban az SK hatékonysága a krónikus betegségek elleni védelembenvese-A hagyományos kínai gyógyászattal végzett kezelést követően a CKD-vel kapcsolatos kudarc és tünetek 73,05, illetve 98.{3}} százalék volt. Ezenkívül a kreatinin-clearance és a szérum kreatinin (SCr) szintje stabil maradt, ami azt mutatja, hogy az SK jó hatékonyságú és biztonságos a CKD kezelésére [14]. Bebizonyosodott, hogy az SK képes enyhíteni a CKD ésvese-fibrózis a fibrózis, gyulladás [15] és apoptózis [16] mérséklésével. A témával kapcsolatos jelenlegi tanulmányok többsége azonban nem volt kellően átfogó, és főként a TGF-re és a kapcsolódó útvonalakra összpontosított. Az UUO modell a vesefibrózis vizsgálatának kísérleti modelljeként ismert. Jelen tanulmányban az SK hatásait vizsgáltuk az NRK-49F fibroblaszt sejtaktivációra és a vesefibrózisra UUO egerekben. Kimutattuk továbbá, hogy az SK ezen gyógyító hatásait úgy érhettük el, hogy a JAK2/STAT3 útvonalat tenyésztett NRK-49F sejtekben és UUO egérmodellben célozták meg.
Kulcsszavak:Shenkang, Krónikus vesebetegség, Vesefibrózis, UUO, Vese fibroblaszt aktiváció, JAK2/STAT3 útvonal
Mód
Az SK vegyszereket és reagenseket a Shijishenkang Pharmaceutical Company, Ltd.-től (Xi'an, Kína) vásároltuk. A lozartán-kálium tablettákat a Merck Sharp & Dohme Pharmaceutical Company Ltd.-től (Hangzhou, Kína) vásároltuk.
Sejttenyésztés
A patkányvese fibroblaszt sejtvonalat (NRK{0}}F) az American Type Cell Collection-től (ATCC, Manassas, VA, USA) szereztük be. Az NRK-49F-sejteket komplett tápközegben, azaz Dulbecco módosított Eagle's-médiumában (Invitrogen, CA, USA) tenyésztettük, amely 5% magzati szarvasmarha-szérumot, 1% penicillint és sztreptomicint tartalmazott, 5% CO 2 és 95% atmoszférában. százalékos levegő 37 fokon. Ezután a sejteket kezeltük TGF- 1 (10 ng/ml) (Novoprotein, Sanghaj, Kína), angiotenzin receptor blokkolóval (ARB) (1 mg/ml) vagy anélkül TGF- 1-el (10 ng/ml) és a tapadást követő gradiens SK koncentrációkkal, és sejtek életképességét értékelték.
A sejtek életképességének vizsgálata
Az NRK{0}}F sejtek életképességét a Cell Counting Kit-8 (Dojindo, Kyushu, Japán) segítségével határoztuk meg a készlet utasításai szerint. Az NRK-49F sejteket 5 ×10 4 sejt/lyuk sűrűséggel szélesztettük 96-lyukú lemezekre. Minden kezeléshez 5 ismétlés volt. 24 vagy 48 órás tenyésztés után az egyes üregekben lévő tápközeget 100 μl CCK-8-ot tartalmazó szérummentes tápközeggel (10:1) cseréltük, és a sejteket további 2 órán át inkubátorban inkubáltuk. Az abszorbanciát 450 nm hullámhosszon mértük. A kezelés hatását az élő sejtek százalékos arányaként számítottuk ki a csak vivőanyaggal kezelt élő kontrollsejtekhez viszonyítva.
Állatok
A tanulmányban használt kísérleti eljárásokat a Pekingi Hagyományos Kínai Orvostudományi Egyetem Állatgondozási és Etikai Bizottsága hagyta jóvá (BUCM{{{{30}}}},018,{ {39}}60,419-2023), és megfelel a laboratóriumi állatok használatának és gondozásának nemzetközileg elismert elveinek. Harminchat 8-hetes C57BL/6 hím egeret a Beijing Vital River Laboratory Animal Technology Co., Ltd.-től vásároltunk (SYXK (Jing), 2017–0{) {51}}33). Az egereket egy speciális, kórokozóktól mentes állatlaboratóriumban helyezték el, légkondicionált helyiségben (fény: 12-h fény/sötét ciklus; szobahőmérséklet: 25±1 fok; relatív páratartalom: 50±). 10 százalék), és véletlenszerűen a következő hat csoportra osztották: az ál-csoport, az UUO-csoport, az ARB-csoport és a magas, közepes és alacsony dózisú SK-csoportok. Az UUO-t az UUO-csoportban, az ARB-csoportban, valamint a magas, közepes és alacsony dózisú SK-csoportokban az egerekben egy korábban megállapított eljárás szerint indukáltuk. Az érzéstelenítést 2% izofluránnal indukáltuk, és 1,5% izofluránnal tartottuk fenn. Egy 1--2- cm-es hosszirányú bemetszést ejtettünk a bal oldali hasban, és a bal húgycsövet tompán elválasztottuk, két helyen lekötöttük, majd a két elkötés között elvágtuk. Ezután a hasüreget lezárták, majd 3 napig fájdalomcsillapítást kaptak. Az ál-csoportba tartozó egereken hasonló műtéti eljárásokon estek át, beleértve a műtét előtti és posztoperatív érzéstelenítést, a laparotomiát és az ureter tompa elválasztását, ureter lekötés és vágás nélkül. Az elzáródás utáni második naptól kezdődően a lozartánt intragasztrikusan adták be az ARB csoport egereinek 0,13 mg/10 g (0,15 ml/10 g) dózisban. Az SK-t nagy, 0,08 g/10 g (0,13 ml/10 g), mérsékelt, 0,04 g/10 g (0,13 ml/10 g) vagy alacsony, 0,02 g/10 g (0,13 ml/10 g) dózisban kapták. az SK csoportba tartozó egereket a farokvénán keresztül 14 napig az ureter lekötése után. Sóoldatot (0,13 ml/10 g) adtunk a farokvénán keresztül az ál, UUO és ARB csoportokban lévő egereknek, és sóoldatot (0,15 ml/10 g) szondán keresztül az ál, UUO és SK csoportokban lévő egereknek a csökkentése érdekében. Elfogultság. Az MRI után szívpunkcióval vért vettünk az egerekből, miután a 14. napon mély érzéstelenítésben (2%-os izofluránnal indukálva és fenntartva) leölték, és összegyűjtöttük a veseszöveteket. A szérumot teljes vérből nyertük 1000 (× g) (4 fok) 10 perces centrifugálással. A szérum vér karbamid-nitrogén (BUN), SCr és cisztatin C (Cys-C) szintjét kolorimetriás módszerrel mértük. Hematoxilin és eozin (HE) festést, illetve Sirius red festést végeztünk az érintett vese stromális struktúráiban a kórszövettani és a kollagén kimutatására. A HE-festéshez a szeleteket viaszmentesítés után desztillált vízbe áztattuk, hematoxilin festőoldatba áztattuk (Solarbio Science & Technology, Kína), majd 1 százalékos sósav-alkohol oldatot adtunk a színek szétválasztásához, csapvízzel mostuk, kékre színeztük és megfestettük eozin festék. A festett szeleteket desztillált vízzel mostuk, dehidratáltuk, megtisztítottuk és semleges gumival lezártuk. A Sirius vörös festéshez a szeleteket viaszmentesítettük, Harris hematoxilinnal megfestettük, mostuk, Sirius vörössel (Solarbio Science & Technology, Kína), közvetlenül elválasztottuk és abszolút etanollal dehidratáltuk, xilollal megtisztítottuk és lezártuk. Öt vizuális mező avese-a kéreg és a proximális tubulus területét véletlenszerűen választottuk ki minden egérnél. A vörös terület kiszámításához ImageJ szoftvert használtunk, a Sirius vörösre festett terület meghatározásához pedig az átlagos vörös területet.
In vivo MRI a vesefibrózis mértékének értékeléséreAz egereken az SK beadását követő 13. napon MRI-t végeztek 7T kisállat-MR-rendszerrel (Agilent 7T MRI rendszer) és testtekerccsel. Az érzéstelenítést 2% izofluránnal indukáltuk, és 1,5% izofluránnal tartottuk fenn. Az egereket hason fekvő helyzetbe helyeztük úgy, hogy a hasukat a rádiófrekvenciás tekercs középpontjához képest középen helyeztük el, és egy légzésérzékelőhöz csatlakoztattuk a légzés figyelésére. A rádiófrekvenciás gerjesztéshez és jelérzékeléshez RAPID Rat Head Systemet használtak. Minden vizsgálatot szabad légzés mellett végeztünk. A képeket diffúziós tenzoros képalkotási (DTI) szekvenciákkal készítettük, és a paraméterek a következők voltak: irányok =30 (b=1004.7s/mm 2 ) plusz null (b=0s/mm) 2 ), Δ=4ms és δ=16ms. A képrögzítési paraméterek a következők voltak: TR/TE=3000ms/50,73 ms, =60 fok, mátrix=128×128, FOV=2×2 cm és a képi szelet vastagsága =1mm. A diffúziós előkészítés teljes időtartama 4 ms volt. A szkennelések között 16 ms-os pásztázási késleltetést alkalmaztunk, és két b=0s/mm 2 -es vizsgálatot építettek be a T1 relaxáció hatásainak korlátozása érdekében. A teljes szkennelési idő körülbelül 1 óra volt. A hidronephrosis miattvese sAz ureter elzáródása okozta szerkezeti eltéréseket csak a patkány veseszövetének külső kéregét és külső velőjét vizsgáltuk képalkotó elemzéshez. A frakcionált anizotrópia (FA) térképeket VNMRJ4.{2}} szoftverrel számítottuk ki. Az MRI-jel intenzitásának pontos mérése és a különböző csoportok közötti fibrózis mértékének meghatározása érdekében minden vesemintához öt szkennelési síkot választottunk, és véletlenszerűen választottunk három kis érdeklődésre számot tartó régiót minden pásztázási síkra.

A CISTANCHE JAVÍTJA A VESE/VESE MŰKÖDÉSÉT
Western blot analízisA teljes fehérjét 500μL RIPA fehérje lízis pufferrel (Solarbio, Peking, Kína) extraháltuk a sejtekből. 10 perces 10 000 (× g) centrifugálás után Bradford protein assay készletet (Applygen, Peking, Kína) használtunk a fehérje mennyiségi meghatározásához. Ekvivalens mennyiségű fehérjét (40 ug) denaturáltunk 100 fokon 10 percig töltőpufferben (Applygen, Peking, Kína), elektroforézissel elválasztottuk 8-10 százalékos SDS-PAGE gélen a relatív molekulatömeg szerint, és elektrotranszferáltuk 0-ra.{{ 10}}μm-es polivinilidén-difluorid membránok (Millipore, Bedford, MA, USA). Ezután a membránokat blokkoló pufferben (Nacalai Tesque, Japán) blokkoltuk 25±5 fokon, és primer antitestekkel inkubáltuk, beleértve az -aktint (Proteintech Group, USA, 1:5000), -SMA-t (Proteintech Group, USA, 1: 1000), kollagén III (I. oszlop) (Abcam, UK, 1:5000), STAT3 (Proteintech Group, USA, 1:2000), p-STAT3 (Tyr705) (Cell Signaling Technology, USA, 1:2000), JAK2 (Cell Signaling Technology, USA, 1:1000), p-JAK2 (Cell Signaling Technology, USA, Tyr1007) (1:1000) és Peroxiredoxin 5 (Prdx5) (Proteintech Group, USA, 1:800), 4 fok éjszaka. TBST-ben történő mosás után a membránokat másodlagos antitesttel (Cell Signaling Technology, USA, 1:10000) inkubáltuk 1 órán át szobahőmérsékleten, majd ismét mostuk TBST-vel. Ezt követően ECL-detektáló készleteket használtak az expozícióhoz. Ezután a fehérjesávok optikai sűrűségét leolvastuk, és az Image Lab™ szoftverrel kvantitatív elemzés céljából elemeztük. A denzitometriás értékeket az -aktin sáv sűrűségére normalizáltuk.
Kvantitatív valós idejű PCRA teljes RNS-t a sejtekből, illvese-szövetet a Monarch® Total RNA Miniprep Kit segítségével a gyártó utasításai szerint. Ezután a GoScript Reverse Transcription System-et használták az első szálú cDNS szintetizálására a kézikönyv szerint. A valós idejű kvantitatív reverz transzkripciós PCR-t 20-μL reakcióban végeztük. A genetargeting primereket az NCBI által közzétett mRNS szekvenciák alapján tervezték meg, és az 1. táblázatban találhatók. A relatív mRNS abundanciát a specifikus mRNS expresszió és az -aktin mRNS expresszió aránya alapján határoztuk meg ugyanabban a mintában, valamint az ehhez viszonyított többszörös változás alapján. az ál-csoport egereiben vagy a 0ng/mL TGF- 1 csoport sejtjeiben a 2 -ΔΔCt módszerrel számítottuk ki.
Statisztikai analízisA legalább három független kísérletből származó összes adatot az átlag ± standard hibájaként (SEM) fejezzük ki. A statisztikai elemzést az SPSS 20.0 szoftvercsomag segítségével végeztük. Normalitásvizsgálatokat és homogenitási varianciavizsgálatokat végeztünk. Ha az adatok normális eloszlásúak voltak, akkor Student-féle t-próbát használtunk a két csoport közötti különbségek összehasonlítására, az egytényezős varianciaanalízist (ANOVA) (LSD teszt az egyenletes szórásokra és Dunnett-teszt az egyenetlen szórásokra). csoportok közötti különbségek. Ha az adatok nem voltak normális eloszlásúak, akkor a nem-paraméteres Mann-Whitney U tesztet használtuk a két csoport közötti különbségek összehasonlítására, a nem paraméteres Kruskal-Wallis tesztet pedig a több mint két csoport közötti különbségek összehasonlítására. P<0.05, p=""><0.01 or="" p="" <="" 0.001="" indicates="" a="" significant="">
Eredmények
Az SK hatása az NRK{0}}F sejtek életképességére TGF- 1 kezelés után
A TGF- egy kulcsfontosságú fibrogenetikai citokin, amely részt vesz a vesefibrózisban. Először különböző dózisú TGF- 1-ot (0, 10, 20, 40 és 80 ng/ml) alkalmaztunk az NRK- 49F sejtek növekedésének serkentésére. A 24 órás TGF- 1-kezelés dózisfüggő módon növelte a sejtek életképességét (1a. ábra), ami összhangban van az MTT vizsgálattal kapott korábbi eredményekkel [17]. Az SK gradiens koncentrációi (1, 2, 4 és 8 mg/ml) szignifikánsan csökkentették a 10 ng/ml TGF- 1 által kiváltott életképesség-növekedést (1b. ábra), valamint a 48 órás kezelés hatását. nyilvánvalóbb volt, mint a 24 órás kezelés. Ez az eredmény arra utalt, hogy az SK gátolja a TGF- 1-indukált vesefibroblaszt növekedést és fokozza az életképességet in vitro.


Az SK gátolta a TGF- -indukált -SMA expressziót és az ECM komponensek lerakódását az NRK-49F sejtekbenA myofibroblasztok aktív fibroblasztok, amelyeket -SMA és ECM lerakódás expressziója jellemez. A TGF- 1 egy fontos citokin, amely részt vesz a myofibroblasztok ECM-termelésében és a fibrózisban [18]. Amint a 2a és 2b ábrán látható, mind a -SMA, mind a col. A III nagymértékben expresszálódott az NRK-49F sejtekben a TGF- 1 kezelés után, ami azt jelzi, hogy a tenyésztett sejtek aktivált miofibroblasztokká alakultak át TGF- 1 beadásakor. Annak további vizsgálatára, hogy az SK képes-e elnyomni a vese intersticiális fibroblasztjainak aktiválódását, megvizsgáltuk az SK hatását az -SMA és a kollagén III expressziójára NRK-49F sejtekben. Az SK beadása jelentősen csökkentette az -SMA expresszióját (dózisfüggő módon) (2. és 3a. ábra) és col. III (2. ábra), ami arra utal, hogy az SK közvetlenül elnyomhatja az NRK-49F sejtek TGF- 1-indukálta aktivációját. Az volt a tendencia, hogy a 4 ng/ml SK hatása a -SMA TGF- 1-indukálta expressziójának és az ECM-komponensek lerakódásának csökkentésében jobb volt, mint a lozartáné (1 mg/l).

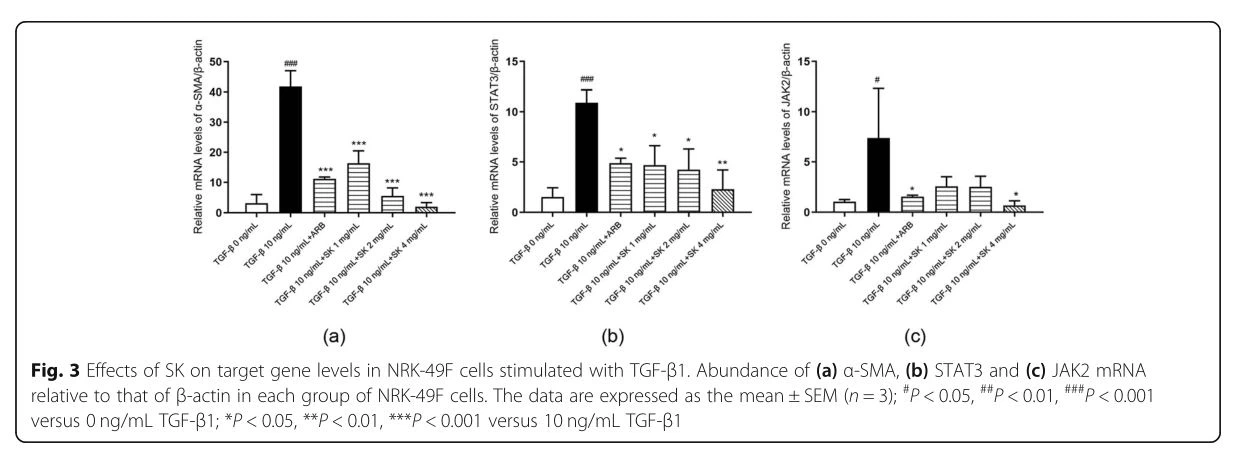
Az SK gátolta a TGF- 1-indukálta STAT3, JAK2 aktivációt és a Prdx5 expressziót NRK-49F sejtekbenAnnak érdekében, hogy feltárjuk azokat a lehetséges mechanizmusokat, amelyekkel az SK gátolja a fibroblasztok aktivációját, további STAT3 és JAK2 génexpressziót és fehérjeszinteket detektáltunk NRK-49F sejtekben RT-qPCR, illetve Western blotting segítségével. Az NRK-49F sejtek magasabb szintű STAT3 és JAK2 mRNS-t expresszáltak TGF- 1 stimuláció után, mint a kezelés előtt. Az SK drámaian gátolta a TGF- 1--indukált STAT3 és JAK2 mRNS expresszióját 24 órán belül (3b. és c. ábra). A STAT3 foszforilációja a Tyr705-nél és a JAK2 a Tyr1007-nél megnövekedett TGF- 1 jelenlétében. Az SK szintén elnyomta e két molekula foszforilációját (2. ábra). A Prdx5, a JAK2/STAT3 útvonal szabályozója TGF- 1 jelenlétében felerősödött, és ezt a felszabályozást az SK kezelés is megfordította (2. ábra). Szinte az összes hatás, kivéve a JAK2 foszforilációjára és a col. A III. csoport robusztusabb volt a nagy dózisú SK csoportban, mint az alacsony dózisú SK csoportban. Következésképpen egyértelműnek tűnik, hogy az SK gátolhatja az NRK- 1-F fibroblasztok TGF- 1-indukálta aktivációját a JAK2/STAT3 aktiváció szabályozásán keresztül. 2 ng/ml vagy 4 ng/ml dózisban az SK jobb hatást fejtett ki a TGF- 1- által kiváltott STAT3 és JAK2 aktiváció és Prdx5 expressziója terén, mint a lozartán.
Az SK enyhítette az UUO által kiváltott veseműködési zavarokat és a vesemorfológiai változásokatUUO indukálásával vesefibrózisos egérmodellt hoztak létre. A 4. a, b, c ábra az ál-csoport, az UUO-csoport, az ARB-csoport, valamint a magas, közepes és alacsony dózisú SK-csoportok veseelégtelenségi indexeit mutatja 14 napos kezelés után. A nagy dózisú SK szignifikánsan csökkentette a Cys-C szintet (P kisebb vagy egyenlő, mint 0.05; 4a. ábra) és az SCr szintet (P Kisebb vagy egyenlő, mint {{12} }.01; 4c. ábra), és az SK jelentősen csökkentette a BUN szintet minden dózisnál (P kisebb vagy egyenlő, mint 0,05 vagy P kisebb vagy egyenlő, mint 0,01; 4b ábra). A fenti eredmények arra utalnak, hogy az SK javította a vesefunkció károsodását és a vesefibrózist, és az SK hatása hasonló volt a lozartánéhoz. A vese HE festése feltárta, hogy az ECM felhalmozódása, a gyulladásos sejtek infiltrációja, a vesetubulusok tágulása és/vagy atrófiája, a vese tubulus epiteliális sejtjeinek degenerációja és nekrózisa a glomeruláris szerkezet nyilvánvaló változása nélkül az UUO csoportban (4d. ábra). A vesefunkció károsodása különböző mértékben enyhült a különböző kezelési csoportokban az UUO csoporthoz képest; a mérsékelt és nagy dózisú SK érte el a legjobb hatást, bár a vesefunkció mértékét az álműtétes csoportban egyik kezelési csoportban sem érte el.
Az SK csökkentette a fibrózissal kapcsolatos FA-értéket, amelyet DTI-vel detektáltunkAmint az 5. ábra szemlélteti, az FA-értéket, amely lineáris kapcsolatban van a fibrózis mértékével a valódi szövetben, in vivo DTI-vel határoztuk meg. A színlelt csoporthoz képest az FA-érték az UUO csoportban jelentősen megnőtt (P<0.01). the="" increase="" in="" in="" the="" fa="" value="" in="" the="" presence="" of="" ureteral="" obstruction="" conditions="" was="" significantly="" reversed="" in="" the="" arb="" and="" high-,="" moderate-,="" and="" low-dose="" sk="" groups="" compared="" to="" the="" uuo="" group="">< 0.01="" or="" p=""><0.001), with="" moderate-dose="" sk="" having="" the="" most="" significant="" effect="" (p=""><>
Az SK gátolta a fibroblaszt aktivációt és az ECM komponensek lerakódását UUO egerekbenEzen kívül értékeltük a fibroblaszt aktivációs marker -SMA, fibroblaszt-specifikus protein-1 (FSP-1) és a klasszikus ECM-komponensek fibronektin (FN) expresszióját. III és kollagén I (col I) az ál-, UUO- és közepes dózisú SK-csoportokban valós idejű PCR-rel. Mivel az SK mérsékelt dózisa megegyezik a klinikailag ajánlott dózissal, és mivel a közepes dózisú csoport általános javulása jobb volt, mint a magas és alacsony dózisú csoportokban, az SK mérsékelt dózisát alkalmaztuk az mRNS expressziójának értékelésére. Amint a 7a. és 7b. ábrán látható, a mérsékelt dózisú SK szignifikánsan enyhítette az -SMA, FSP, FN, col. III és col. I szintet. Ezek az eredmények összhangban voltak a Siriusred festési eredményekkel, amelyek azt mutatták, hogy a fibrózis vörös területe az érintett vesében az ARB csoportban és a közepes és alacsony dózisú SK csoportban szignifikánsan kisebb volt, mint a kezeletlen csoportban (P<0.05) (fig.="" 6),="" indicating="" that="" sk="" decreased="" the="" number="" of="" col-="" lagen="" bundles="" in="" the="" affected="">
Az SK hatása a STAT3, JAK2 és TGF-mRNS szintekre, valamint a szabályozó molekulák expressziójára és a SOCS1 és SOCS3 citokin jelátviteli (SOCS) fehérjék szuppresszorára UUO egerekbenAmint a 7c. ábrán látható, a TGF-, JAK2 és STAT3 mRNS szintjei szignifikánsan megemelkedtek az UUO csoportban az ál-csoporthoz képest a 14. napon. Az ál egerekkel összehasonlítva a közepes dózisú SK-val kezelt UUO egerekben a JAK2 és a TGF-mRNS szintje jelentős csökkenést mutatott az obstrukció utáni 14. napon, de az SK nem csökkentette szignifikánsan a STAT3 mRNS szintjét UUO után. Ez az eredmény azt sugallja, hogy az SK hatása a vesefibrózisra és a fibroblaszt aktivációra UUO egerekben a JAK2 és STAT3 aktiváció szabályozásán keresztül jelentkezhet anélkül, hogy a teljes STAT3 mRNS expressziójában megváltozna. A STAT3 downstream molekulájának, a TGF-nek a szintjét szintén csökkentette az SK az ureter lekötésével összefüggésben. A SOCS fehérjék létfontosságúak a JAK/STAT jelátvitel negatív szabályozásában [19]. Az UUO-ra válaszul a SOCS1 és SOCS3 szintek szignifikánsan megemelkedtek, és szignifikánsan csökkentek az SK csoportban a modellcsoporthoz képest (7d. ábra). Ez az eredmény azt sugallja, hogy az SK elnyomhatja a JAK/STAT útvonalat, hogy visszacsatolásként csökkentse negatív szabályozó molekuláinak expresszióját.

A CISTANCHE JAVÍTJA A VESE-/VESEFÁJDALÁST
Vita
A vese tubulointersticiális fibrózisa a végstádiumú vesebetegség végső közös útja. A miofibroblasztok, amelyek számos sejtből származnak, beleértve a hámsejteket, az endoteliális sejteket és a pericitákat epiteliális-mezenchimális transzdifferenciáció (EMT) vagy endoteliális-mezenchimális transzdifferenciáció (EndoMT) révén, segíthetnek a sérült szövetek helyreállításában azáltal, hogy ECM-et és -SMA-t termelnek. kontraktilis feszültséget generálnak [20]. E különböző sejttípusok közül az aktivált intersticiális fibroblasztok a miofibroblasztok fő forrásai, ezek a sejtek 50 százalékát teszik ki [21]. Az -SMA mellett az aktivált fibroblasztok is specifikusan expresszálják az FSP-t-1. A TGF-et a vesefibrózis fő mozgatórugójaként határozzák meg, és kimutatták, hogy aktiválódik különböző vesebetegség-modellekben és vesesejtekben. Az aktivált TGF- kötődik a TGF-receptorhoz, és indukál downstream jelátviteli molekulákat, beleértve az EMT-vel, EndoMT-vel, fibroblaszt aktivációval, ECM-termeléssel és az ECM-degradáció gátlásával kapcsolatos molekulákat és transzkripciós faktorokat a Smad-on keresztül, beleértve a TGF-et is [23], STAT3 a Tyr foszforilációja aktiválja a Tyr705-nél Janus kinázokon keresztül. Az aktivált STAT3 fehérje dimer formájában jut be a sejtmagba és kötődik a célgénhez. Ezenkívül a STAT3 indukálja a TGF-útvonal jelátvitelét [24]. Valójában az UUO modellben a STAT3 aktiválódása a Tyr705-nél a vese intersticiális fibroblasztjaiban, a hisztopatológiai elváltozásokkal és a fibroblaszt aktivációval együtt, az első naptól kezdve megnövekszik, 7 napnál tetőzik, és 14 napig emelkedik [25]. A STAT3 valószínűleg sokféle vesebetegségben vesz részt a célgének expressziójának szabályozásán keresztül, különösen a CKD kialakulásában szerepet játszó transzkripciós faktorokon keresztül. Jelen vizsgálatunkban az obstrukció utáni 14. napon a -SMA, JAK2 és STAT3 mRNS szintjei szignifikánsan megemelkedtek a megnövekedett vesefibrózis mértékével.
Korábbi kutatások szerint az SK és komponensei csökkentik a kóros károsodást, gátolják az endothelsejtek proliferációját, enyhítik a proteinuriát és a glomerulosclerosis-t, védik a reziduális vesefunkciót és lassítják a betegség progresszióját, így beavatkoznak a CKD és a vesefibrózis progressziójába; fibroblaszt aktivációról azonban nem érkezett jelentés. Korábbi tanulmányok és CCK{0}} eredményeink szerint 10 ng/ml TGF- 1-ot használtak a fibroblasztok aktiválására; 1, 2 és 4 mg/ml-t választottunk az SK alacsony, közepes és nagy dózisaiként; és a 48 órát választottuk beavatkozási időként jelen tanulmányban. Az NRK-49F sejtekben a TGF- 1 stimulációt követően az -SMA felszabályozása és a sejtproliferációval és -aktivációval kísért morfológiai változások, amelyek a sejtek életképességének és ECM-termelésének növekedésében nyilvánultak meg [26, 27]. Ebben a tanulmányban megerősítették, hogy a TGF- 1 szabályozta az -SMA és az ECM génexpresszióját az upstream JAK2/STAT3 útvonal aktiválásával. Adataink azt mutatták, hogy az SK közvetlenül gátolta a TGF- 1-indukálta NRK-49F sejtaktivációt és az ECM-termelést in vitro. Továbbá kimutattuk, hogy az SK mérsékelheti a vesefibrózist UUO egerekben in vivo, csökkentve az intersticiális ECM-felhalmozódást az obstrukció utáni 14. napon. Ezek az eredmények azt mutatták, hogy az SK jelentősen gyengítheti a vesefibrózist az intersticiális fibroblaszt aktiváció gátlásával és az -SMA expresszió csökkentésével. Az SK antifibrotikus hatásának lehetséges mechanizmusa a fibroblasztok aktivációjának gátlása a JAK2/STAT3 jelátviteli útvonal szabályozásán keresztül mind in vitro, mind in vivo. A mérsékelt dózisú SK szignifikánsan megfordította a TGF- 1 UUO által kiváltott felszabályozását is, ami arra utal, hogy az SK hatása a TGF-hez kapcsolódik. Mivel a TGF- és a STAT3 kölcsönhatásba lép egymással, az SK gátolhatja a STAT3-at a TGF- megcélzásával, leszabályozhatja a TGF-et a STAT3 megcélzásával, vagy mindkettőt gátolhatja. Korábbi rendszerfarmakológiai vizsgálatunk a STAT3-at jósolta az SK egyik lehetséges célmolekulájaként [28], és ezt a megállapítást jelen tanulmány is igazolta. Mi lozartánt használunk, egy ARB-t

jelentősen gyengítheti a vesefibrózist és a vesetubuláris sejt apoptózist azáltal, hogy gátolja a STAT3 jelátviteli fehérje foszforilációját UUO patkánymodelljében [29], mint pozitív kontroll gyógyszer. A korábbi megállapítások összhangban vannak adatainkkal. A peroxiredoxinok a merkaptán-függő peroxidázok családja, amelyek a hidrogén-peroxid redukciójának katalizálásával csökkenthetik az oxidatív stresszt. A Prdx5 szintje a patkányvesében csökkent az UUO utáni első napon. Megfigyelték, hogy a Prdx5 expressziója fokozatosan növekszik a TGF-kezelés után 5 napig. Kimutatták, hogy a Prdx5 túlzott expressziója gátolja a STAT3 TGF- - által kiváltott foszforilációját, és csökkenti a TGF-indukálta -SMA és FN expressziót az NRK-49F sejtekben, ami azt jelzi, hogy a Prdx5 negatívan szabályozza a TGF- - STAT3 aktivációt és fibrózist indukált NRK-49F sejtekben [12]. Az endogén STAT3 jelátvitel hátterében álló fő szabályozó mechanizmus a SOCS fehérjecsaládot foglalja magában. Miután a STAT3 citokinek aktiválódik, a STAT3 dimer a nukleáris indukció downstream célgénjébe kerül, beleértve a SOCS-t is [30]. Pontosabban, a SOCS1 közvetlen kötődésének kinázgátló régiója jelentősen gyengítheti a vesefibrózist és a vesetubuláris sejt apoptózist azáltal, hogy gátolja a STAT3 jelátviteli fehérje foszforilációját UUO patkánymodelljében [29], mint pozitív kontroll gyógyszerként. A korábbi megállapítások összhangban vannak adatainkkal. A peroxiredoxinok a merkaptán-függő peroxidázok családja, amelyek a hidrogén-peroxid redukciójának katalizálásával csökkenthetik az oxidatív stresszt. A Prdx5 szintje a patkányvesében csökkent az UUO utáni első napon. Megfigyelték, hogy a Prdx5 expressziója fokozatosan növekszik a TGF-kezelés után 5 napig. Kimutatták, hogy a Prdx5 túlzott expressziója gátolja a STAT3 TGF- -indukálta foszforilációját, és csökkenti a TGF- --indukálta -SMA és FN expressziót az NRK-49F sejtekben, ami azt jelzi, hogy a Prdx5 negatívan szabályozza a TGF{{ 38}}indukált STAT3 aktivációt és fibrózist NRK-49F sejtekben [12]. Az endogén STAT3 jelátvitel hátterében álló fő szabályozó mechanizmus a SOCS fehérjecsaládot foglalja magában. Miután a STAT3 citokinek aktiválódik, a STAT3 dimer a nukleáris indukció downstream célgénjébe kerül, beleértve a SOCS-t is [30]. Pontosabban, a SOCS1 kinázgátló régiója közvetlenül tud kötődni
JAK2-re és gátolja a STAT3 foszforilációját [31]. Az UUO által kiváltott JAK/STAT aktiváció SOCS expressziós emelkedést okoz [32]. 48 órás 10 ng/ml TGF- 1-os stimulációt követően a Prdx5 fehérje expressziója szignifikánsan megnőtt az NRK-49F sejtekben, ami összhangban van a korábbi eredményekkel. Az SK (4 mg/ml) szignifikánsan csökkentette a Prdx5 fehérje szintjét 48 órás beavatkozás után. Az UUO utáni 14. napon a SOCS1 és SOCS3 mRNS szintje az érintett vesében szignifikánsan megemelkedett az UUO csoportban a kontroll csoporthoz képest, ami azt jelzi, hogy a STAT3 jelátvitel UUO utáni aktiválása indukálta a SOCS1 és SOCS3 expresszióját. negatívan szabályozza a túlaktivált STAT3 jelet. 14 napos SK beavatkozás után a SOCS1 és SOCS3 mRNS szintje jelentősen csökkent. Ezek az eredmények azt mutatták, hogy ahelyett, hogy közvetlenül megemelték volna a negatív szabályozókat a JAK2/STAT3 jelátvitel gátlására, az SK gátolta a JAK2/STAT3-at, ami a Prdx5, SOCS1 és SOCS3 negatív szabályozók leszabályozását eredményezte. Így a JAK2/STAT3 az SK közvetlen terápiás célpontja lehet a vesefibrózisban.

Az MRI nagyon biztonságos módszer a vese szerkezeti és fiziológiai változásainak értékelésére intravénás kontrasztanyag alkalmazása nélkül [33, 34]. A diffúziós súlyozott képalkotás (DWI) egy jól ismert MRI-módszer, amelyet a biológiai szövetek mikroszerkezetében bekövetkezett változásokat tükröző molekuláris mozgások vagy diffúziók leképezésére használnak [35]. A DTI egy diffúziós súlyozott képalkotáson (DWI) alapuló új képalkotó technológia, amely nemcsak a vízmolekulák sebességét, hanem mozgásuk irányát is le tudja írni, nevezetesen az anizotrópiát. A DWI-vel összehasonlítva a DTI érzékenyebben és pontosabban tükrözi a vízdiszperzió változását. A DTI további információkkal is szolgálhat az FA alapján mért diffúzió irányáról és mértékéről. Hueper et al. [36] kimutatta, hogy DN patkányokban az FA összefüggésben áll a glomerulosclerosissal, az intersticiális fibrózissal és a vese tubuláris sérülésével. Yan és mtsai. [37] azt találta, hogy az FA a korai DN biomarkere lehet. Kaimori et al. [38] lineáris kapcsolatot figyelt meg az FA-érték és a valódi szöveti fibrózis mértéke között UUO patkánymodellben. Ebben a tanulmányban optimalizáltuk a paramétereket, hogy csökkentsük a szkennelési időt, az érzéstelenítési időt és a kísérleti erőforrások felhasználását. A DTI eredmények összhangban voltak a Sirius vörös festéssel az UUO által okozott vesefibrózis mértékét és az SK vesefibrózist enyhítő képességét tekintve. Bizonyos mértékig ezek az eredmények azt mutatták, hogy az SK valós hatással van a vesefibrózisra in vivo. Ebben a tanulmányban bemutattuk azt a mechanizmust, amellyel az SK szabályozza a vese intersticiális fibrózisát mind in vivo, mind in vitro. A jövőbeli vizsgálatokban e mechanizmus további ellenőrzéséhez inhibitorok vagy siRNS-ek alkalmazása szükséges a JAK2/STAT3 gátlására.
Következtetések
Összefoglalva, adataink azt sugallják, hogy az SK hatékonyan gátolja a vese fibroblasztok aktivációját és a vesefibrózist UUO egerekben a JAK2/STAT3 jelátviteli útvonal szabályozásával. Eredményeink jól megértik az SK mechanizmusát a vesebetegség kezelésében. Azonban az SK kezelésének részletes molekuláris mechanizmusai vesefibrózisban további feltárást igényelnek.
