Az integráló omika elemzés feltárja a mikrovaszkuláris gyulladással kapcsolatos utakat a vese allograft biopsziákban
Mar 24, 2022
A szilárd szervtranszplantáció során a mikroRNS-ek (miRNS-ek) kulcsszereplővé váltak az allograft sejtműködés szabályozásában a sérülésekre válaszul. Ahhoz, hogy betekintést nyerjünk a miRNS-ek szerepébe az antitest által közvetített kilökődésben, amely a mikrovaszkuláris gyulladás által szövettanilag meghatározott kilökődési fenotípus,vese az allograft biopsziákat miRNS, de hírvivő RNS (mRNS) profilalkotásnak is alávettük. A BIOMARGIN vizsgálatra jellemző egyedi többlépcsős szelekciós eljárást alkalmazva (felfedezési kohorsz, N=86; szelekciós kohorsz, N=99; validációs kohorsz, N=298), hat differenciálisan kifejeződő miRNS-t azonosítottunk következetesen: miR-139-5p (lefelé) és miR-142-3p/150-5p/155-5p/{ {7}}p/223-3p (fel). Expressziós szintjük fokozatosan korrelált a mikrovaszkuláris gyulladás intenzitásával. A miRNS-ek célgének sejtspecifitását úgy vizsgáltuk, hogy in vivo mRNS-célpontjaikat integráltuk egysejtes RNS-szekvenálással egy független allograft biopsziás kohorszból. Az endothel eredetű miR{11}}p expresszió negatívan korrelált az MHC-vel kapcsolatos gének expressziójával. Ezzel szemben az epitheliális eredetű miR-222-3p túlzott expressziója erősen összefügg a vese elektrolit-homeosztázisának romlásával és az immunrendszerrel kapcsolatos folyamatok elfojtásával. Immunsejtekben a miR-150-5p szabályozta az NF-kB aktivációját a T-limfocitákban, míg a miR-155-5p szabályozta az mRNS-splicingot az antigénprezentáló sejtekben. Összességében az integrált omika lehetővé tette a mikrovaszkuláris gyulladásban szerepet játszó új útvonalak feltárását, és azt sugallja, hogy a tubuláris epiteliális sejtekben az antitestek által közvetített kilökődés következményeként az anyagcsere módosulásai a közeli endoteliális kompartmenten túlmenően következnek be.
Kulcsszavak:vesetranszplantáció, mikroRNS, multi-omika, mikrovaszkuláris gyulladás, antitest-mediált kilökődés

A CISTANCHE JAVÍTJA A VESE-/VESEBETEGSÉGET
BEVEZETÉSBan benveseátültetés(KT) az alloimmun sérülést általában kétféle allograft kilökődésre osztják az immuninfiltráció térbeli eloszlása és a donor-specifikus anti-HLA antitestek jelenlétére vagy hiányára vonatkozó információk alapján. A diagnózis az allograft biopszián alapul, a szövettani elváltozások Banff International Consensus osztályozása (1) szerinti osztályozásával. A tubulitis ("t" lézió) és az intersticiális gyulladás ("I" lézió) a T-sejt-közvetített kilökődés (TCMR) jellegzetes szövettani jellemzői, és a tubulointersticiális kompartmentre gyakorolt közvetlen citotoxicitáshoz kapcsolódnak. Az antitest-mediált kilökődés (ABMR) leggyakrabban keringő anti-HLA antitestekhez kapcsolódik, amelyek gyulladása a mikrovaszkuláris kompartmentet célozza meg. Az aktív ABMR szövettani elváltozások közé tartozik a mononukleáris sejtek jelenléte a glomeruláris kapillárisokban ("g" elváltozás) és a peritubuláris kapillárisokban ("ptc" lézió), amelyeket együttesen "mikrovaszkuláris gyulladásnak" (MVI) neveznek. A krónikus aktív ABMR-ben a krónikus szövetsérülések, például a transzplantációs glomerulopathia vagy az artériás intimafibrózis összeadódnak ezekhez az akut elváltozásokhoz (1). A jelenlegi T'-sejt-célzott immunszuppresszív szerek alkalmazásával a TCMR korlátozott prognosztikai hatással bír, míg az ABMR a graft kudarcának fő oka, ami a hatékony terápiás megközelítések hiányával függ össze (2).
Ahhoz, hogy jobb terápiákat találjunk az MVI-re és az ABMR-re, jobb betekintésre van szükség a sérülési folyamatok mögött meghúzódó biológiai mechanizmusokba. Úgy tűnik, hogy a nagy áteresztőképességű omika technológiák megfelelnek a célnak, mivel több ezer gén, fehérje és metabolit pontos és egyidejű szűrését teszik lehetővé (3). Teljes átiratos kihallgatásaveseAz allograft biopsziák mélyreható mRNS génexpressziós változásokat mutattak ki a sérült rezidens sejtekben vagy a beszűrődő sejtpopulációkban az ABMR során (4). Eközben a mikroRNS-ek (miRNS-ek) kulcsszereplővé váltak a sejtmetabolizmusban azáltal, hogy a hírvivő RNS-t (mRNS) poszttranszkripciós szinten szabályozzák. Valójában a miRNS-ek forradalmasították a test proliferációban, apoptózisban, differenciálódásban és fejlődésben részt vevő fiziológiai folyamatainak finomhangolásának megértését (5). Nem meglepő, hogy a szabályozatlan miRNS-expresszió számos patológia kialakulásához vezet, beleértvevesebetegség(6). Mivel a miRNS-expressziós profilok különböznek a beteg és az egészséges állapotok között, számos tanulmány elemezte a miRNS-eket akár önmagában, akár más hagyományosabb markerekkel kombinálva, nemcsak a betegség diagnosztizálására és a betegség progressziójának prognosztizálására, hanem a lehetséges terápiás alkalmazások tervezésére is (7).
A szilárd szervtranszplantáció keretében a miRNS-ek szerepet játszhatnak a kilökődésben az immunsejtek működésének szabályozásában és az allograftban rezidens sejtek sérülésekre adott válaszában (6, 8). Számos tanulmány vizsgálta az allograft miRNS-eket, mint biomarkereket és/vagy effektorokat a TCMR beállításaiban (8,9), de ez idáig egyik sem foglalkozott az MVI-vel és az ABMR-rel. Ebben a tanulmányban az volt a célunk, hogy integráljuk a különböző omika szinteketveseallograft biopsziák, hogy betekintést nyerjünk a miRNS-ek szerepébe ebben a káros kilökődési fenotípusban.
ANYAG ÉS MÓDSZER TanulmánytervezésEz a tanulmány az FP{0}}finanszírozott BIOMAmarkers részeVeseA Graft Injuries kutatási program (BIOMARGIN, https://cordis.europa.eu/project/id/305499, ClinicalTrials.goy, NCT02832661), amelyet egy európai kutatókonzorcium vezet, amely az allograft immunrendszeri elváltozások biomarkereit keresiveseátültetésrecipiensek, diagnosztikai és/vagy prognosztikai értékkel. A BIOMARGIN egy többközpontú, prospektív, többfázisú vizsgálat, amelyet négyen végeznekveseátültetésközpontok Európában (Necker Kórház, Párizs, Franciaország; Egyetemi Kórházak, Leuven, Belgium; Hannover Medical School, Hannover, Németország; és Egyetemi Kórház, Limoges, Franciaország). A mintákat 2013 áprilisa és 2015 júniusa között a szűrés és indikációs biopsziák idején prospektívan vették (IA ábra). Minden transzplantációt negatív komplement-függő citotoxicitási keresztegyezéssel végeztünk. Ebben a négy klinikai központban az indikációs biopsziák mellett a transzplantáció után 3, 12, néha 24 hónappal a helyi centrum gyakorlata szerint protokollbiopsziát végeztek. Az egyes helyszíneken működő intézményi felülvizsgálati bizottság jóváhagyta a vizsgálatot, és minden beteg írásos beleegyezését adta.
Tanulmányi kohorszokA vizsgálatot három fázisra osztottuk (1A. ábra). Az első eset-kontroll felfedezési fázisban N=88 biopsziás mintát használtunk a globális miRNS expressziós elemzéshez (N=754 miRNS, kivéve a potenciálisan normalizáló miRNS-eket) . A mintákat a rendelkezésre állás és a szövettani kritériumok alapján választottuk ki (kivéve a glomerulonephritis vagy polyomavirus-asszociált nephropathia diagnózisát, valamint a nem egyértelmű diagnózisú eseteket). A helyi biopsziás leolvasások alapján történt az első szelekció, amelyet az eredeti központtól független patológuscsoport központi leolvasással tovább finomított. Statisztikai elemzést (lásd miRNS szelekció) használtunk a miRNS-ek kiterjesztett listájának kiválasztására, amelyek a szövettani fenotípusok között a legkülönbözőbben fejeződnek ki, és amelyeket ezt követően a 2. fázisban számszerűsítettek.
Hasonló eset-kontroll vizsgálati elrendezést alkalmaztunk a második (szelekciós) fázisban is, ahol célzott miRNS expressziós elemzést (N=143) végeztünk N=99 biopsziás mintán. Ugyanezt a statisztikai adatfolyamot alkalmaztuk a miRNS-ek még szűkebb listájának kiválasztására, amelyet ezt követően a 3. fázisban számszerűsíteni kell. Végül a harmadik (validációs) kohorszban a BIOMARGIN protokoll szerint 2014. június 24. és 2015. július 2. között prospektíven és egymást követően gyűjtött összes minta megfelelő mennyiségben.veseallograft biopszia minőségét a második szelekciós fázis eredményeként kiválasztott 38 miRNS tekintetében értékelték. Ebben a valós életkörülmények között a szövettan, a demográfiai adatok, az idő vagy a minta elérhetőségén és a minőség-ellenőrzési kritériumokon (a biopszia és az RNS-hozam megfelelősége) kívüli egyéb tényező alapján nem végeztek szelekciót.

miRNS szelekcióA BIOMARGIN tanulmányhoz kifejezetten az R(R Core Team(10) 1.0.44-es verziójában készült robusztus statisztikai folyamatot fejlesztettek ki a biosignal R csomag(1l) kiterjesztéseként. Röviden, a felfedezési szakaszban egy jellemző kiválasztási stratégiát hajtottunk végre, amely egy- és többváltozós megközelítéseket tartalmazott. Az egyváltozós kiválasztáshoz nemparametrikus tesztet (Wilcoxon-Mann-Whitney teszt) és parametrikus tesztet (Student's t-test), valamint Discovery kohorszt (BIOS-03-0023, BIOS-06-0238) használtunk. Az egyes miRNS-transzkriptumok előrejelzési pontszámait minden többváltozós modellben integráltuk, hogy „többváltozós pontszámot” kapjunk. Ezen egyváltozós és többváltozós elemzések eredményeinek kombinálásával sikerült rangsorolni és kiválasztani a miRNS-jelöltek egy részhalmazát, hogy része legyen a következő fázisban számszerűsítendő kiterjesztett listának.Ebben a VMI útvonalakra összpontosító posthoc elemzésben az egyes miRNS-ek átlagos normalizált expresszióját hasonlítottuk össze az esetek és a kontrollok között Wilcoxon teszttel mindhárom kohorszban. A többszörös tesztelést a Benjamini & Hochberg hamis felfedezési arány (FDR) módszerével ellenőriztük.
Klinikai patológiai értékelésAz egyes szövettani elváltozások pontszámait a Banff 2019 kritériumai szerint félkvantitatívan értékelték (16). A "mikrovaszkuláris gyulladás" (MVI) kifejezést a glomerulitis (g) és/vagy a peritubularis capillaritis (ptc) bármilyen fokú kombinációjára használták. Minden ABMR-eset megfelelt a Banf 2015 vagy Banff 2017 osztályozás első 2 kritériumának (szövettani). az akut szövetsérülés bizonyítéka és a vaszkuláris endotéliummal való jelenlegi/legutóbbi antitest-kölcsönhatás bizonyítéka), de nem mindegyik felelt meg a harmadik kritériumnak [a donor-specifikus antitestek (DSA) és/vagy CAd-festődés szerológiai bizonyítéka]. A transzplantáció utáni DSA-kat a helyi központ gyakorlata szerint határoztuk meg, a DSA-pozitivitást úgy határoztuk meg, mint kimutatható donor-specifikus szérum anti-HLA antitesteket, amelyek átlagos fluoreszcencia intenzitása (MFI) 500 volt a biopszia időpontjában vagy bármikor korábban.
RNS extrakció biopsziás mintákból mRNS és miRNS profilalkotáshozMindegyiknél két tűmagot vettünkveseallograft biopszia. Az egyiket a hagyományos szövettani osztályozáshoz használták, a másik felét pedig azonnal Allprotect Tissue Reagentben tárolták (Qiagen Benelux BV, Venlo, Hollandia). Az Allprotect csöveket 4 °C-on tárolták (minimum 24 óra és maximum 72 óra). , majd -20 fokon tároljuk az RNS-kivonásig. A teljes RNS-t izoláltuk aveseallograft biopsziás minták az Allprep DNS/RNS/miRNA Universal Kit (Qiagen Benelux BV) segítségével egy QIAcube készüléken (Qiagen Benelux BV). Az izolált RNS mennyiségét (abszorbancia 26{{20}} nm-en) és tisztaságát (230,260 és 280 nm-en mért abszorbancia aránya) NanoDrop ND-1000 spektrofotométerrel (Thermo) mértük. Fisher Scientific/Life Technologies Europe BV, Gent, Belgium). Az RNS integritásszámát (RIN) az Eukaryote nano/pico RNA Kit-tel (Agilent Technologies Belgium NV, Diegem, Belgium) értékelték ki a Bioanalyzer 2100 készüléken (Agilent Technologies BelgiumNV). A minőség-ellenőrzési indexek nem különböztek szignifikánsan a VMI és a No között. MVI-csoportok [RIN(átlag±SD):5,6±1,96vs 5,4±1,97,P=0.66;260/280 arány (átlag±SD):1,87±0,06 vs 1,87±0,1l,P{{26 }}.40]. Alacsony RIN(<6.5), we="" excluded="" samples="" with="" a="" 260/280=""><1.6. the="" extracted="" rna="" was="" subsequently="" split="" and="" stored="" at="" -80℃℃.half="" of="" the="" rna="" extract="" was="" used="" for="" mirna="" profiling="" and="" the="" other="" half="" for="" mrna="" transcriptomic="" analysis.="" the="" associated="" data="" are="" available="" from="" the="" gene="" expression="">

A CISTANCHE JAVÍTJA A VESE/VESEDIALÍZIS
miRNA profilozásSpecific reverse transcription of 150ngof total RNA was performed using Megaplex"RT Primers Human Pool A v2.1(Step 1)or Custom RT Primers Human Pool (Step 2 and 3)(Thermo Fisher Scientific, Les Ulis, France), on a Veriti Thermal Cycler (Applied Biosystems, Thermo Fisher Scientific). No complementary(c)DNA preamplification was required. miRNA expression was assessed by qPCR, using TaqManArray Cards (Applied Biosystems", Thermo Fisher Scientific), where the primers and probe of each miRNA were spottedanddried in duplicate wells of a microfluidic card. We used TaqMan"Array Human MicroRNA A +B Card Sets v3.0 for the discovery cohort(a two-card set enabling quantitation of 754 unselected human miRNAs)and Custom TaqManArray MicroRNA Cards for the selection and validation cohorts. Data analysis was performed by using Expression Suite software version 1.0.3. Assays with a cycle threshold(CT) values >35 nem tekinthető kifejezettnek. Az RNU44 és az RNU48 konzisztens expressziót mutatott az összes mintában, az átlagos (RNU44 plusz RNU48) variációs együttható 3,73 százalék volt az A tömbkártyában és 3,79 százalék a B tömbkártya esetében, és háztartási génekként használták az adatok normalizálására az összes alvizsgálatban.
mRNS transzkriptomikai analízisA transzkriptomikai analízist microarray segítségével végeztük a már leírtak szerint (17). Röviden, a biopsziás mintákból kivont teljes RNS-t először amplifikáltuk és komplementer RNS-vé (cRNS) biotiniláltuk a GeneChip 39 IVT PLUS Reagent Kit (Affymetrix) segítségével, majd hibridizáltuk az Affymetrix GeneChip Human Genome U133 Plus 2-vel.0 Arrays( Affymetrix), amely a teljes genomot lefedő 54 675 próbakészletből állt. Robust Multichip Average (RMA) normalizálást alkalmaztunk. Az egyes mRNS-ek átlagos normalizált expresszióját Wilcoxon teszttel hasonlítottuk össze az esetek és a kontrollok között. A Benjamini & Hochberg téves felfedezési arány (FDR) módszerével szabályoztuk a kockázati alfa többszöri tesztelés miatti inflációját. A microarray-adatokat a Microarray-kísérletre vonatkozó minimális információra vonatkozó irányelveknek megfelelően kezeltük.
In Silico AnalyzesBiological Interpretation Of Multiomics EXperiments (BIOMEX) szoftvert használtak a transzkriptomikus adatok differenciálelemzésére, Ensembl ID annotációval (18). Az Ingenuity Pathway Analysis (IPA, Build: 478438M Content version:44691306, Qiagen) és az OMICSnet(19) segítségével meghatároztuk a kiválasztott miRNS-ek által szabályozott génkészleteket. Az OMICSnet segítségével génontológiai elemzést végeztünk a Reactome útvonaladatbázissal, a teljes útvonal felhasználásával (20). A génhálózatok kiépítése teljesen felügyelet nélkül zajlott, és minden egyes gén és a hálózat összes többi génje közötti molekuláris kölcsönhatások számán alapult. A legtöbb interakciót bemutató gének automatikusan a hálózat középpontjába kerültek, míg a kisebb interakciószámú gének a perifériára terjedtek. A kiválasztott miRNS-ek sejtes eredetét a Fantom5 projekttel (21) vizsgálták, amely az emberi sejtekben és szövetekben végzett génexpresszió cap-analízisét adja meg. A miRNS expressziós elemzéséhez mindent figyelembe vettünkvese-rokon strukturális sejteket és minden keringő hematopoietikus sejtet, további szelekció nélkül.
Egysejtű RNS szekvenálási adatok elemzéseKorábban publikált humán egysejtes RNS szekvenálási (siRNA-seq) adatokat használtak két ABMR biopsziából és négy egészséges referenciát, amelyek megfelelnek a transzplantációs megfigyelési biopsziáknak. A kapcsolódó nyers számokat vagy mátrixokat a GEO-ról (GSE145927, https://www.ncbi.nlm. nihgov/geo)(22) ésVesePrecision Medicine Project (KPMP, https://atlas.kpmp.org/repository). A mintánként generált nyers génexpressziós mátrixokat összevontuk és a Seurat V4 csomag segítségével elemeztük (23). A Seurat-objektumok létrehozására és szűrésére alkalmazott paraméterek a következők voltak: 500 és 10000 közötti detektált gént és kevesebb, mint 25 százaléknyi mitokondriális transzkriptumot expresszáló sejtek bevonása. A szűrést követően az összes objektumot a Seurat SCTransform integrációs munkafolyamatával integráltuk (24). Röviden, 3000 szolgáltatást használtak az integrációhoz a PrepSCTIntegration funkcióval, és a FindIntegrationAnchors funkciót használták a kötegelt hatás korlátozására. Egy teljes Uniform Manifold Approximation and Projection (UMAP) adatkészletet állítottunk elő a DimPlot függvény és a 16 legfontosabb összetevő használatával. A fürtök a FindNeighbors és a FindClusters függvényekkel készültek 0,6-os felbontással. A klaszterek azonosítását a FeaturePlot függvény segítségével végeztük, az egyes klaszterekben lévő specifikus markerek kifejezésének értékelésével. A pontdiagramokat a DotPlot és a FeaturePlot ábrázolási függvények segítségével állítottuk elő, az RNS-vizsgálat normalizált számlálásával bemeneti adatként.

A CISTANCHE JAVÍTJA A VESE/VESE FERTŐZÉSÉT
Statisztikai analízisA betegek és a donor jellemzőit számokkal, százalékokkal és a kategorikus változók gyakoriságával írták le. Folyamatos változókat jelentettünk az átlagok és a normál eloszlású standard deviációk (SD), a mediánok és az interkvartilis tartományok (IQR) felhasználásával a torz eloszlású változók esetében. Összehasonlítottuk jellemzőiket a Fisher- vagy a Wilcoxon-teszttel, ha szükséges. Az MVI intenzitás szerinti medián miRNS expresszió összehasonlítására Kruskal-Wallis tesztet, korrelációs elemzéshez Spearman tesztet használtunk. A statisztikai szignifikanciát a 0-nál kisebb P-értékeknél.05. A statisztikai elemzéshez és az adatok megjelenítéséhez a GraphPad Prism (8-as verzió; GraphPad Software, San Diego, CA) és az RStudio (4-es verzió.{14}}.3) szoftvert használtuk. A következő R-csomagokat használtuk: heatmap3 (heatmap3_1.1.9) hőtérkép-elemzésekhez, fmsb(fmsb_0.7.0) és skálák (skálák_1.1.1) csomagok radarrajzokhoz, ggplot2 (ggplot2_3.3.5) oszlopdiagramokhoz és complot(corrplot_0.90) a korrelációs mátrix elemzéséhez.
EREDMÉNYEK
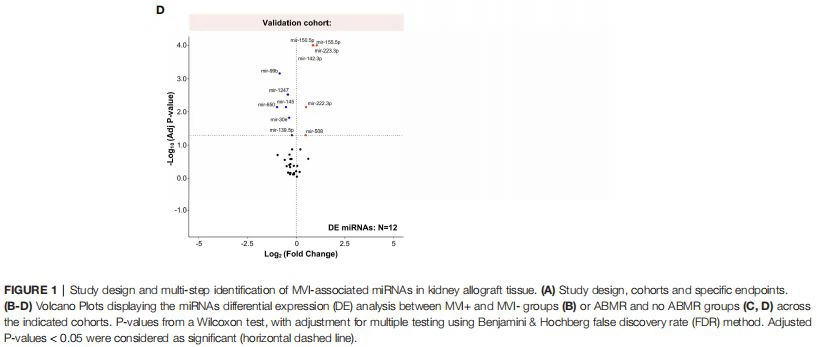
MVI-asszociált miRNS-ek többlépcsős azonosításaBetween April 2013 and July 2015,646 patients enrolled in the BIOMARGIN study provided 716 indication or surveillance biopsies. Inadequate biopsies (N=49), biopsies with no paired sample for research use(N=135)or samples not passing molecular biology QC(N=49) were excluded, leaving 483 samples from 441 individuals available for this study (Figure 1A). Baseline and clinical characteristics of the study groups are provided in Supplementary Tables S1-3, and the histological characteristics of the biopsies are provided in Supplementary Tables S4-6. In the discovery cohort, a total of 27 patients met the MVI composite endpoint(MVI+), defined as clinical ABMR diagnosis and/or any level of MVI(g and/or ptc>0). A másik 59 beteg (MVI-) különböző diagnózisokat mutatott be, amelyek magukban foglalták a T-sejtek által közvetített kilökődést (TCMR, N=8), az intersticiális fibrózist és a tubuláris atrófiát (IFIA,N=20), valamint a normál biopsziát (N{{6). }}), butno MVI. A 754 miRNS-jelölt közül 18 miRNS expresszálódott differenciáltan az MVI plusz és MVI- csoportok között (1B. ábra). A szelekciós kohorszban 143 miRNS-ből álló korlátozott listát határoztak meg 99 mintában. Ebben a szelekciós kohorszban 14 miRNS expresszálódott eltérően az (N=28) és az (N=71)ABMR nélküli esetek között (1C. ábra). Végül, a legnagyobb keresztmetszeti kohorszban 38 miRNS-t határoztak meg 298 mintában, amelyek közül 12 miRNS expresszálódott differenciálisan az ABMR(N=29) és a nem ABMR (N=269) biopsziák között (1D ábra). ).
6 MVI-asszociált MiRNS következetes azonosítása és összefüggés a szövettannalEzt követően kereszteztük a differenciálisan expresszált miRNS-ek 3 listáját, és azonosítottunk 6 olyan miRNS-t, amelyek következetesen kapcsolódnak MVI-hez vagy ABMR-hez a 3 független kohorszban (2A. ábra).miR-142-3p,miR-150-5p,miR A -155-5p, a miR-222-3p és a miR-223-3p túlzottan kifejeződött az MVI/ABMR-ben, míg a miR-139-5p expressziója csökkent. A radardiagramok (2B. ábra) minden lépésnél megmutatják a 6 miRNS esete és kontrollja közötti különbséget, és alátámasztják a miRNS-profilok robusztusságát a három független kohorszban. Ezután azt tanulmányoztuk, hogy a 6 miRNS expressziója hogyan kapcsolódik az egyes szövettani elváltozásokhoz mind a 483 allograft biopsziában együttvéve. Az 5 felfelé szabályozott miRNS expressziója fokozatosan nőtt az MVI léziók intenzitásával, míg a miR-139-5p expressziója negatívan korrelált (2C. ábra). MiR-139-5p/142-3p/ A 150-5p/155-5p/223-3p nemcsak az ABMR-rel kapcsolatos jellemzőkkel (g, ptc, C4d lerakódás), hanem a TCMR-rel kapcsolatos elváltozásokkal is nagymértékben társult (i, t ) és IFTA elváltozások (ct, ci), ami arra utal, hogy részt vesznek a gyakori, nem ABMR-specifikus, gyulladásos és hegesedési folyamatokban. Alternatív megoldásként a léziók között természetüknél fogva előfordulhat bizonyos belső kollinearitás, ami azt eredményezi, hogy képtelenek vagyunk azonosítani egy lézió valódi specifitását. A MiR-222-3p nem korrelált a TCMR vagy az IFTA szövettani elváltozásaival (2D. ábra).
Multi-Omics integráció: mRNS-miRNS kölcsönhatás MV-benEzt követően a korábban publikált felfedezési sorozatban (25) értékeltük az MVI plusz és MVI- esetek között eltérően kifejeződő géneket. Az 54 675 próba közül összesen 2755 differenciálisan expresszált gént (DEG) azonosítottunk az MVI plus és MVI- között.


csoportok, amelyek 1085 lefelé szabályozott és 1670 felfelé szabályozott gént tartalmaznak (3A. ábra). Az MVI plusz mintákban a leginkább differenciáltan expresszált mRNS a CXCL9 és a CXCL10 volt, összhangban a korábbi jelentésekkel (17, 26), miszerint ezek a gének a leginkább túlexpresszáltak az ABMR-ben. Ezután IPA-t és OMICSnet-et használtunk, hogy in silico azonosítsuk az egyes miRNS-ek feltételezett célgénjeit. Az előrejelzések szerint összesen 4504 mRNS-t céloz meg a 6 miRNS közül legalább az egyik. Ezután integráltuk ezeket a 4504 megjósolt célpontot a DEG-ekkel az allograft biopsziákban. Az integrált miRNS/mRNS analízis a miR-139-5p által megcélzott 61 DEG-et azonosított, amelyek szignifikánsan megnövekedtek az MVI plusz biopsziákban. Azt is kimutatta, hogy a miR-142-3p, miR-150-5p, miR-155-5p, miR{ által célzott MVI plusz biopsziákban 28, 58, 52, 43 és 27°-kal szignifikánsan csökkent. {22}}p és miR-223-3p (3B. ábra).

Az MV-asszociált miRNS-ek sejtes eredeteA hat miRNS sejtes eredetét különféleképpen jellemeztékvese-sejt és hematopoetikus sejt altípusok online elérhető miRNS atlasz segítségével [Fantom adatbázis (27)]. A felügyelet nélküli klaszterezés megkülönböztetettvese-sejteredetű miRNS-ek immunsejt-eredetű miRNS-ekből (4A. ábra). Minden miRNS-hez egy vagy két domináns sejttípust is feltárt. Úgy tűnt, hogy a MiR-139-5p főként glomeruláris endothelsejtekben (EC) expresszálódik. A MiR-222-3p, bár expressziója nem korrelált a tubuláris gyulladással (Banff-léziók"t", 2D. ábra), elsősorban avese-hámsejtek. A fennmaradó négy miRNS elsősorban perifériás vér mononukleáris sejtekben (PBMC) vagy granulocitákban expresszálódott, a miR-142-3p NK-sejtekben és monocitákban, a miR-150-5p CD4 pluszban és CD8 plusz T-sejtekben, miR -155-5p a CD19 plusz B-sejtekben és makrofágokban, és miR-223-3p a neutrofilekben.
Az egysejtű RNS szekvenálás minden vesesejteket és beszűrődő immunsejteket azonosított Az egyes MVI-asszociált miRNS-ek potenciális szerepének jellemzésére két nyilvánosan elérhető sc-RNAseq adatokat elemeztünk.vese-allograft biopsziák ABMR-rel és magas MVI pontszámokkal (g2, ptc3)(22). Ezeket az adatkészleteket 4 egészséges referencia biopsziával integráltuk, MVI nélkül. Minőségellenőrzés és szűrés után 31545 sejtet detektáltunk, és a felügyelet nélküli klaszterezés 12 klasztert tárt fel (4B. ábra). Jól bevált markereket (28) használtunk az összes fő rezidens és beszivárgó sejtaltípus azonosítására és címkézésére (S2 kiegészítő ábra). Ezután azokra a sejtpopulációkra összpontosítottunk, amelyekből a hat miRNS-ünk feltételezhetően származik. Ebből a célból a sejteket 4 fő klaszterbe csoportosítottuk, amelyek megfelelnek az endotéliumnak, a hámnak, a limfocitáknak és az APC-knek (4C. ábra). Ezen adatok korábbi elemzésével összhangban (22) sem neutrofil, sem NK sejtpopulációkat nem mutattak ki az sc-RNASeg adatkészletekben.
A miR-139-5p szabályozza az EC-aktiválást és az antigén-prezentációs útvonalat az MVI alattA MiR-139-5p volt az egyetlen csökkentett miRNS a vizsgálatunkban MVI/ABMR esetén (2A. ábra), és azt találtuk, hogy főként glomeruláris EC-ből származik (4A. ábra). Hatvanegy célgénjéről megerősítették, hogy az MVI plusz esetekből származó bulk microarray-ben felszabályozott (3B. ábra), és expressziójukat tovább vizsgálták egysejt felbontásban a 3 korábban azonosított EC alklaszterben (4B, C ábra). Amint az 5A. ábrán látható, az aktivált ECcluster csak MVI plusz mintákban volt kimutatható. Emellett a 61 gén fele (N=30) következetesen növekedett az sc-RNAseq MVI plusz biopsziákban, függetlenül a három EC alklasztertől. Ezek közül a GBP5 volt a leginkább megnövekedett gén. Ezt követően a génontológiai elemzés ezen 30 endothel-eredetű átirat felhasználásával azonosította az UBE2D1-et és az YWHAG-ot a génhálózat központi szereplőiként (5B. ábra). Pontosabban, az immunrendszerrel kapcsolatos útvonalak és a fő hisztokompatibilitási komplex (MHC) által közvetített antigén-feldolgozási és -prezentációs útvonalak gazdagodtak (5C. ábra). Pseudotime analízist végeztünk az EC aktiváció során bekövetkező génexpressziós változások jobb jellemzésére, az Across sejtek állapotpályája (5D, E ábra), az UBE2D1, YWHAG és GBP5 folyamatosan nőtt az MVI-hez kapcsolódó endoteliális aktiváció során. Nagyon hasonló pályákat találtak az MHC-vel rokon HLA-A,-B és -DRA gének esetében, de a bonafid endoteliális aktiváció és gyulladás markerek esetében is, mint például a VCAM1, CXCL9 és CXCL10, ami arra utal, hogy ezek a gének egyidejűleg expresszálódnak az endothel aktiváció során. Összességében ezek az eredmények azt sugallják, hogy a miR-139-5p csökken az MV léziók során, és már nem represszálja az MHC antigén prezentációs útvonalat aktivált EC-ben.


miR-222-3p Mindkettőt károsítjaVeseFiziológiai és immunrendszeri utak epiteliális sejtekben Az MVI Next során a miR-222-3p-re összpontosítottunk, amely egy felszabályozott miRNS az MVI-mintákban.vese-hámsejtek eredete és exkluzívabb korreláció az ABMR-rel kapcsolatos szövettani elváltozásokkal (2A, D, 4A ábra). A tömeges allograft szövetben 43 célgén expressziója csökkent (3B. ábra), és továbbértékelődött egy egyszeri sejtfelbontás a különbözővese-korábban azonosított hámpopulációkat (4B., C. ábra). A 43 (95 százalék) gén közül 41 masszív csökkenése az összes azonosított génbenvese-hámsejt klaszterek géncsendesítésre utalnak


profil a VMI-ben (6A. ábra). Érdekes módon 4 gén vesz résztvese-fiziológiai útvonalakat (ERBB4, ATPIB1, TIMM50 és KIF3B), de az immunrendszerrel kapcsolatos géneket (TRAPI és PEBPI) is központi génekként azonosították a hálózatban (6B. ábra). A 43 gének génontológiája feltárta az ErbB jelátviteli útvonalak feldúsulását, de az immunrendszerrel összefüggő útvonalakban és a citokinválaszban (6C. ábra) és az ERBB4 expressziójában is megerősítést nyert minden esetben.vese-sejteket (6D. ábra). Összességében ezek az eredmények arra utalnak, hogy a VMI során magas szintű -222-3p invese-A hámsejtek mind a gének erős elnyomásával járnak együttvese-elektrolit homeosztázis útvonalak és az immunrendszerrel kapcsolatos útvonalak a hámban.

A miR-150-5p szabályozza az NF-kB aktivációt a T-limfocitákban MVI alatt. Hasonlóképpen vizsgáltuk a (megnövekedett) miR-150-5p szabályozó szerepét az MVI során a T-sejt klaszterben, ahol a legdominánsabban expresszálódott. (4A. ábra). Ábrázoltuk az ömlesztett allograft biopsziás mintákban azonosított 58 csökkent MVI-asszociált DEG-t (3B. ábra), és szembesítettük az sc-RNAseq T-sejt klaszter génexpressziójával (7A. ábra). A miR150-5p által megcélzott és a T-sejtekben specifikusan alulexpresszált gének aránya az MVI során meglepően alacsony volt (15/58,25,9 százalék), ami arra utal, hogy e gének globális csökkenése in vivo nem kizárólag a T-limfocita rekesz. Mindazonáltal ebből a 15 génből álló, rendkívül válogatott listából és az OMICSnet platform segítségével létrehoztunk egy génhálózatot (7B. ábra), és elvégeztük a génontológiai elemzést (7C. ábra). Megfigyeltük, hogy a miR-150-5p túlzott expressziója az NF-hez társult. -KB szabályozás a T limfocitákban MVI alatt.
miR-155-5p Szabályozza az mRNS-splicingot az APC-kben az MV során Végül pontosan ugyanezt a stratégiát alkalmaztuk az 52miR-155-5p-célgénekre is, amelyek alulexpresszáltak az MVI során (3B. ábra). A miR-150-5p-vel ellentétben a T-limfocitákban azt tapasztaltuk, hogy csaknem kétharmaduk a miR-155-5p célzott gének konzisztensen csökkentek az APC sc-RNAseq klaszterben (31/52,59,6 százalék, 8A ábra). A génhálózat elemzése kimutatta, hogy az AIFMI és a CIAO1 központi gének voltak (8B. ábra). Ezenkívül a génontológia erős feldúsulást mutatott ki az mRNS splicinghez kapcsolódó útvonalakban (8C. ábra).

VITAEgyedülálló kialakítása révén a BIOMARGIN tanulmány a tipikus keretrendszer a multi-omic adatintegrációhoz. Valójában nagyon robusztus csővezetékeket használtak mind a felfedezési, mind a kiválasztási, mind a validálási csoportokban, amelyek nagyszámú beteget tartalmaztak különböző transzplantációs központokból. A három független kohorszban egyidejűleg megfigyeltük és megerősítettük 6 miRNS sajátos expressziós profilját az MVI során: a miR-139-5p csökkent, míg a miR-142-3p/150-5p/{{5} }p/222-3p és miR-223-3p nőtt. Fontos, hogy a 6 miRNS mindegyikének szintje korrelált az MVI súlyosságával, ami dózisfüggő szabályozási mechanizmusra utal. Ezt követően szilíciumplatformokon vizsgáltuk az egyes miRNS-sejtek eredetét. Meglepő módon a miRNS-ek két különálló csoportját figyelték meg: az első a beszűrődő immunsejtekből, a másik pedig a rezidensekre specifikusabb.vese-sejteket. Ezután a miRNS-eket és az mRNS-eket is megmértük ugyanabban a biopsziás mintákban, lehetővé téve az MVI-hez kapcsolódó, in vivo validált, differenciálisan expresszált mRNS-ek/miRNS-ek integrált elemzését. Végül, miután leírtuk az mRNS-ek/miRNS-ek asszociációját a tömeges szöveti felbontásnál, megerősítettük az mRNS/miRNS-ek kölcsönhatását az egysejt felbontásban a 6 azonosított miRNS-ből négy esetében.

Érdekes módon a miR-139-5p volt az egyetlen miRNS, amely negatívan korrelált az MVI-léziókkal. Főleg az EC-ből származik, és arról számoltak be, hogy szabályozza az MHC-vel kapcsolatos géneket. Célgénjei közül az UBE2D1 erősen felszabályozott az MVI-vel kapcsolatos endothel aktiváció során. Az UBE2D család egy E2 ubiquitin-konjugáló enzimcsalád az ubiquitin-proteaszóma rendszerben (29, 30), és az UBeD1-ről kimutatták, hogy fokozza a March-I ubikvitinációt, ami az MHC II. osztályú fehérjék fokozott szabályozásához vezet (31). Ezenkívül a GBP5 volt a leginkább reprezentált géninaktivált EC az MVI során, ami összhangban van a legutóbbi jelentéseinkkel, amelyek azt mutatják, hogy a GBP5 erősen felszabályozott az ABMR-biopsziákban (17), de a vérmintákban is (32). Érdekes módon kimutatták, hogy a GBP5 expressziója indukálható a II-es típusú interferonnal humán méh mikrovaszkuláris endothel sejtjeiben, a CXCL9 és CXCL10 sejtekkel együtt (33). E két proinflammatorikus kemokin korai szerepe az akut kilökődési folyamatokban jól dokumentált, és a vizeletben való szintjüket javasolják az akut kilökődés kockázatának monitorozására a vesetranszplantált betegek rutinszerű monitorozása során (34). Egy másik miR-139-5p célpont az YWHAG.YWHAG, amely a HLA-F fehérjecsaládját kódolja, és leírják, hogy a diabéteszes nephropathia aktív profibrotikus folyamata során eltérően expresszálódik (35). A miR-139-5p lehetséges szerepe a fibrózisban, amely a gyulladást követő utolsó közös útvonal, annál is fontosabb, hogy az IFTA-t a közelmúltban beépítették egy összetett pontszámba, hogy előre jelezzék a vese allograft túlélését az ABMR után (36). Összességében ezek az eredmények azt sugallják, hogy a miR-139-5p már nem gátolja az MCH antigén expresszióját az Anethum felszínén MVI alatt, és részt vesz a kemoattrakciós és fibrózisos folyamatokban, de ezeket a mechanizmusokat még kísérletileg meg kell erősíteni az endotélium felszínén az MVI során és részt vehetnek a kemoattrakciós és fifibrózisos folyamatokban, de ezek a mechanizmusok még kísérletileg megerősítésre várnak.
A másodikvese-Az általunk azonosított -eredetű miRNS a miR-222- 3p, amelynek expressziója specifikusabb az MVI léziókra: a g- és PTC-pontszámokhoz, valamint a C4d-lerakódáshoz kapcsolódik, de nem az i vagy t léziókhoz. Főleg hámsejtekből származott azonban. A sejtfelbontásnál végzett multi-omikus integrációt követően megállapítottuk, hogy a miR-222-3p főként az ErbB jelátvitelt gátolja, ami kulcsfontosságú az alapvető sejtfunkciók, például a proliferáció, a migráció, a növekedés és a differenciálódás szempontjából (37). Az emberi biológiában fiziológiás ErbB jelátvitelre van szükségvese-elektrolit homeosztázis és a vese integritásának fenntartása (38). Eredményeink azt is azonosították, hogy az ADAM22, NRG1, ZNF91 ErbB-szignálhoz kapcsolódó gének, amelyek jelentősen elnyomták a hámban az MVI során. Más, a vese fiziológiájához nélkülözhetetlen géneket, például az ATP1B1-et és a KIF3B-t szintén elnyomta a vese epitéliumában a miR{8}}p az MVI során. Korábban Baker et al. kimutatta, hogy az ATP1B1 (a Na plusz /K plusz -ATPáz b1 alegysége) hajtvese-a nátrium tubuláris reabszorpciója (39). Ezenkívül Aguado-Fraile et al. azonosították a kinezin család 3B tagját (KIF3B), amely részt vesz a patkány proximális tubulussejtek sejtforgalmában. A KIF3B kulcsfontosságú közvetítőként jelenik meg a proximális epiteliális tubulussejtek ischaemiára/reperfúzióra adott válaszában, és potenciálisan alkalmazhatóvese-ischaemiás károsodás kezelése (40). Így feltételezhetjük, hogy a miR-222-3p elnyomja az alapvető élettani utakat az MVI során a hámban. Ezen túlmenően, az immunrendszerrel kapcsolatos utakat a miR-222-3p túlzott expressziója is szabályozza: az olyan fontos gének, mint a TRAP1 és PEBP1, teljes mértékben gátolva voltak az erős MVI-vel rendelkező mintákban. Érdekes módon a TRAP1-ről kimutatták, hogy javulvese-tubulointersticiális fifibrózis egerekben egyoldali ureterelzáródásban, védelemmelvese-tubuláris epiteliális sejt mitokondriumok (41). Ezenkívül a PEBP1 gyulladáscsökkentő hatást fejt ki a MAPK és az NF-kB útvonalak gátlásán keresztül homeosztatikus/alap körülmények között (42). Ban benvese-epithelium, Marko et al. elegánsan kimutatta, hogy a poszt-ischaemiás NF-kB aktiváció súlyosbítja a tubuláris sérülést és súlyosbítja a gyulladást (43). A mi kezünkben a PEBP1-et teljesen elnyomta a miR-222-3p, ami arra utal, hogy az NF kB útvonal felszabadul az MVI során. Összességében ezek az eredmények azt mutatják, hogy az epiteliális biológia zavart okoz az MVI ésvese-Az epiteliális sejtek aktívan reagálnak az MVI-sérülésekre, míg ennek a szövetnek az MVI-ben való részvételével ritkán foglalkoznak. Ezek a molekuláris eredmények új megvilágításba helyezhetik az akut tubuláris sérüléseket, amelyek egy jól bevált, de régóta elhanyagolt ABMR-kritérium. Emellett kimutatták, hogy az epiteliális sejtek exoszomális miR-222-3p-t szekretálnak, és M2 fenotípust indukálnak makrofágokban (44). Eközben Li és mtsai. a közelmúltban arról számoltak be, hogy az M2 makrofágok túlzottan expresszálják a miR{6}}-et, és ezt a miRNS-t a mikrokörnyezetbe szállítják, szintén exoszómák szekretálásán keresztül. Vesetranszplantáció során a miR{7}} emelkedett különböző körülmények között (IFTA, akut kilökődés és TCMR), valamint a testnedvekben vagy a szövetekben (45). Érdekes módon a miR- 155 elősegítheti az epiteliális-mezenchimális átmenetet azáltal, hogy megcélozza a RASSF4-et epiteliális sejtekben (46). Ez a miRNS alapú áthallás a makrofágok ésvese-az epiteliális sejteket még fel kell mérniveseátültetésés különösen az MVI összefüggésében. Ezekkel az eredményekkel összhangban megfigyeltük, hogy a miR{0}}p-t főként monocitákat és makrofágokat tartalmazó APC-k fejezték ki. Ebben a bizonyos részhalmazban a miR- 155-5p-célgének ontológiája a premRNS splicing útvonalak feldúsulását tárta fel. Érdekes módon Janssen et al. beszámolt arról, hogy a tüdőgyulladás pre-mRNS splicing útvonalakat indukált az alveoláris makrofágokban. Ezenkívül a pre-mRNS splicing aktiválása különbözött a szövetben rezidens makrofágokban a (vérre toborzott) monocita eredetű makrofágokhoz képest. Beszámoltak a maganyagcsere változásairól a toborzott makrofágokban, a glikolízis következtében megnövekedett kiáramlással és a trikarbonsavcikluson (TCA-ciklus, azaz Krebs-ciklus) keresztüli kiáramlás csökkenésével (47). A miR-150-5p esetében azt találtuk, hogy az MVI alatti túlzott expressziója a limfocita klaszterben lévő NF-kB útvonalhoz kapcsolódik, amely magában foglalja mind a veleszületett NKT-sejteket, mind az adaptív T-sejteket. Érdekes módon a miR-150-5p kulcsfontosságú az érett és működőképes NK-sejtek létrehozásában (48), és a miR-150-5p-hiányos CD8 plusz T-sejtek kevésbé citotoxikusak (49). Emellett a CD8 T-sejtek exoszómákban is szekretálhatnak miR-150-5p-t (50), ami viszont elősegítheti a fibroblasztok aktivációját a tubuláris epiteliális sejtekben, és ezt követőenvese-fifibrosis, amint azt a legutóbbi jelentések (51, 52) sugallják.

A CISTANCHE JAVÍTJA A VESE/VESE MŰKÖDÉSÉT
Tanulmányunknak vannak bizonyos korlátai. Kutatásunkat 6 miRNS-re összpontosítottuk, amelyeket következetesen azonosítottunk többlépcsős tervezésünk során. Azonban lépésről lépésre végzett miRNS-szelekciót folytattunk, és az összes ismert miRNS-nek csak egy töredéke volt számszerűsítve a validációs kohorszban. A miRNS-ek kiválasztásának statisztikai útvonala a BIOMARGIN kezdeti tervén alapult, amely alkalmas volt több végpont diagnosztikai biomarkereinek azonosítására (ABMR, de TCMR és IFTA is). Ennélfogva, bár szignifikánsan megnövekedett a felfedezési és szelekciós kohorszban (2A. ábra), a miR-146a nem volt számszerűsítve a validációs kohorszban. Ezáltal a miR{5}a-t de facto kizártuk kiválasztási folyamatunkból, bár a szakirodalom azt sugallja, hogy szerepet játszik a vesetranszplantációban előforduló ischaemiában/reperfúzióban (53) és az alloimmun válaszok Treg-közvetített szabályozásában (54). Ezenkívül nem zárhatjuk ki, hogy egy nagyobb mintaméret több miRNS-t eredményezett volna, mint például a miR-138 (lefelé) és a miR-511 (felfelé), amelyek eltérően fejeződtek ki a szelekciós kohorsz ABMR eseteiben és azonos irányú tendenciát mutatott a felfedezési kohorszban. Emellett nem saját biopsziás mintáinkon végeztünk sc-RNAseq elemzést, hanem egy online elérhető sc-RNAseq adatkészletet használtunk. A vizsgálat tervezése és a biopsziás minták gyűjtése idején az scRNAseq technológia még nem állt rendelkezésre, és a frissen gyűjtött minták iránti igény nem tette lehetővé a fagyasztott vagy paraffinba ágyazott minták retrospektív felhasználását. Hasonlóképpen, az mRNS-profilalkotást microarray-ek segítségével végezték, amely akkoriban az akkori benchmark technológia, amelyet mára felülmúlt a következő generációs RNS-seq. Az online elérhető sc-RNAseq adatkészlet használata korlátozza a betegek alapvető demográfiai jellemzőinek jelentését. Ez a hiányzó információ aggodalomra adhat okot a lakossági csoportok reprezentativitását illetően. Sőt, a szekvenálás semmilyen technikai vonatkozását sem ellenőriztük. Ezért a választott felbontás mellett az sc-RNAseq analízisünk nem mutatott ki neutrofil vagy NK sejtklasztert ezekben a mintákban. Ezért a miR-142-3p és miR-223-3p downstream elemzése a megfelelő célgénhálózat és ontológia kiépítésére korlátozódott (S2 kiegészítő ábra), és nem tette lehetővé egyetlen sejt felbontású feltárását. A miR-223-3p 27 célgénjének génhálózata és ontológiája azonban a TCA-ciklus feldúsulását tárta fel (S2 kiegészítő ábra) az ERBB jelátvitellel együtt. Feltételezhetjük tehát, hogy mind a monociták miR-155-5p-je, mind a neutrofilekben a miR-223-3p szerepet játszanak az e sejtek által az MVI során kifejtett metabolizmusban és gyulladásos válaszban. Emellett a miR-142-3p-ről már kimutatták, hogy megnőtt a vese allograft kilökődésében (9, 55, 56), de ez idáig nem volt specifikusan összefüggésbe hozható az ABMR-rel. Vizsgálatunk másik korlátja, hogy a ritka infiltráló sejtekben a specifikus génexpressziós változások elfedhetők a tömeges génexpressziós elemzés során. Ezért további vizsgálatokra van szükség, amelyek több mintát is tartalmaznak, hogy lehetővé tegyék az összes, még a ritka sejtaltípusok megfelelő vizsgálatát is, de jelenleg korlátozza a technika viszonylag magas költsége.
Összefoglalva, itt megvizsgáltuk az MVI-hez, az ABMR-hez kapcsolódó fő szövettani károsodáshoz kapcsolódó molekuláris útvonalakat. Az alkalmazott integrált omika megközelítés lehetővé tette számunkra, hogy új utakat tárjunk fel az MVI-ben, és azt sugallja, hogy az ABMR következtében a tubuláris epiteliális metabolizmus módosulásai a közeli endothel kompartmenten túlmenően fordulnak elő. Tanulmányunk szemlélteti a multi-omikákban rejlő nagy lehetőségeket a betegségek mechanizmusainak feltárására, és megnyitja az utat az új vizsgálatok előtt, amelyek tovább tisztázzák az egymás közötti áthallást.vese-rezidens és allograft-infiltráló sejtalcsoportok.
