A ritka Rs35667974 IFIH1 génpolimorfizmus és az autoimmun betegségek társulása az RNS epigenetikai esete?
Jul 13, 2023
vizualizáció – AA, AP és EEE, felügyelet – EEE és finanszírozás megszerzése – EEE. Minden szerző elolvasta és elfogadta a kézirat közzétett változatát. Absztrakt
A helikáz C domént tartalmazó protein 1 (IFIH1) génnel indukált interferon egy citoplazmatikus RNS-helikázt kódol, amely más néven melanoma differenciációhoz társult 5 (MDA5), egy RIG-1-szerű RNS-helikáz, amely felismeri a vírus RNS-t és részt vesz a veleszületett folyamatokban. immunitás a vírus RNS felismerése révén. A kettős szálú (ds) RNS-hez kötődve az MDA5 fonalas szerkezetet képez a dsRNS hossza mentén, és molekuláris aláírásokat használ az önmaga és a nem saját megkülönböztetésére a dsRNS hossza és metilációja alapján. Az rs35667974 missense változata védelmet nyújt az 1-es típusú cukorbetegség, a pikkelysömör és a pikkelysömörű ízületi gyulladás ellen, de úgy találták, hogy összefüggésbe hozható a spondylitis ankylopoetica, a Crohn-betegség és a fekélyes vastagbélgyulladás fokozott kockázatával. Annak érdekében, hogy betekintést nyerjünk ennek a változatnak a komplex szerepébe, molekuláris dinamikai szimulációk segítségével strukturális elemzést végeztünk az MDA5 dsRNS-sel komplexben.
Adataink arra utalnak, hogy míg az rs35667974 variáns Ile923Val mutációja nem befolyásolja szignifikánsan a natív dsRNS-hez való kötődést, destabilizáló hatást fejt ki 2'-O uridin metiláció jelenlétében. Így a 2'-O-metiláció jelenléte a dsRNS-ben olyan érzékelő aláírást vezet be, amely a teljes MDA katalitikus aktivitás szelektív csökkenéséhez vezet. Ez a tanulmány az IFIH1 autoimmun lókusz megosztott rs35667974 variánsának szerepét értékeli, amely a jelentések szerint szelektíven csökkenti a módosított MDA5 fenotípus katalitikus aktivitását, és ennek következtében csökkenti a negatív visszacsatolást a citokin és kemokin jelátvitelre, valamint az autoimmunitás elleni szelektív védelmet. .
A helikáz C domén egy fontos enzimfehérje, amely képes feloldani a DNS kettős hélix szerkezetét. Segíthet a DNS-nek a megfelelő replikáció, szerkesztés és szállítás befejezésében a sejtreplikáció, -javítás és -átírás folyamatában, és a sejtek normális működésének egyik kulcsa. Ugyanakkor az immunitás nagyon fontos védekező mechanizmus az emberi szervezetben, amely hatékonyan védhet meg minket a kórokozóktól, például baktériumoktól és vírusoktól.
Tanulmányok kimutatták, hogy a helikáz C domén fontos szerepet játszik az immunitásban. Először is, a helikáz C domén biztosíthatja a gének stabilitását és kódolási hatékonyságát azáltal, hogy segíti a sejtes DNS normál replikációját, javítását és transzkripcióját, ezáltal javítja az emberi szervezet immunitását. Másodszor, a helikáz C domén elősegítheti a fehérje heterogenitás molekulák sejt általi felismerését, és szabályozhatja az immunrendszer jelátvitelét, ezáltal támogatja a szervezet védekező funkcióját. Mindkét fenti módszer pozitív szerepet játszott az immunitás fenntartásában és fokozásában.
Emellett a helikáz C domén és az immunitás közötti kapcsolat mélyreható vizsgálata is fontos inspirációt ad számunkra, hogy új gyógyszereket fedezzünk fel a rák és az immunrendszeri betegségek kezelésére. A helikáz C domént megcélzó gyógyszerfejlesztés és génterápia javíthatja a szervezet rákkal és más immunrendszeri eredetű betegségekkel szembeni ellenálló képességét, és segíthet a betegeknek jobban megbirkózni a kapcsolódó betegségek kezelésével és gyógyulásával.
Összefoglalva, a helikáz C domén és az immunitás közötti kapcsolat nagyon szoros, és létfontosságú szerepet játszik a génstabilitás biztosításában, a sejtes immunitás elősegítésében és a szervezet védekezésének támogatásában. Reméljük, hogy a megfelelő kutatási és kezelési módszerekkel jobban meg tudjuk őrizni és javítani tudjuk az emberi immunitást, és egészségesebb és jobb életet teremtünk számunkra. Ebből a szempontból erősítenünk kell a személyes immunitást. A Cistanche jelentős hatással van az immunitás javítására, mivel a húspaszta számos antioxidáns anyagban gazdag, például C-vitaminban, C-vitaminban, karotinoidokban stb. Ezek az összetevők megkötik a szabad gyököket és csökkentik az oxidatív stresszt. Stimulálja és javítja az immunrendszer ellenálló képességét.

Kattintson a cistanche tubulosa előnyeire
Kulcsszavak
Egynukleotidos polimorfizmus (SNP) · Molekuláris modell · Helikáz C domén 1-gyel indukált interferon (IFIH1) · Melanoma differenciálódással összefüggő 5 (MDA5) · RNS-metiláció.
Bevezetés
Az autoimmun betegségekben szerepet játszó gének és mechanizmusok, amelyek a lakosság mintegy 5 százalékát érintik, továbbra is megfoghatatlanok, de a felgyülemlett adatok erősen arra utalnak, hogy a különböző autoimmun betegségeknek közös genetikai háttere lehet, ami rámutat a különböző autoimmun betegségekre jellemző változatok létezésére. (Zhernakova et al. 2009). Az a kísérlet, hogy ezt a genetikai információt biológiailag jelentőségteljes, betegségekhez vezető mechanizmusokká bontsák fel, az ok-okozati gének azonosítására utal. A betegséget okozó variánsok azonosítása nehéz, de szükséges feladat a betegségek előrejelzésére, megelőzésére és beavatkozására szolgáló hatékony módszerek kidolgozásában (Biros et al. 2005).
Különböző típusú RNS-molekulák vesznek részt számos biológiai folyamat szabályozásában, beleértve a hírvivő RNS-t (mRNS), a transzfer RNS-t (tRNS), a riboszomális RNS-t (rRNS), a mikroRNS-t (miRNS) és a hosszú, nem kódoló RNS-t (lncRNS). Az RNS-molekulák számos (több mint 150) kémiai módosítást tartalmaznak (Machnicka et al. 2013; Boccaletto et al. 2018). Ezek a módosítások funkcionálisan kapcsolódnak az RNS-metabolizmus minden szakaszához, például szerkezethez, stabilitáshoz és kölcsönhatásokhoz, és számos biológiai folyamatban játszanak kritikus szerepet, például a vírusok replikációjának modulálásában és az antivirális immunválaszokban (Machnicka et al. 2013). Közülük a ribóz-metiláció az RNS-ben található leggyakoribb módosítások közé tartozik. A 2′-O-metiluridin megtalálható az archaeák, baktériumok és eukarioták rRNS-ében, snRNS-ében, snoRNS-ében és tRNS-ében (Aučynaitė et al. 2018). A ribóz-2′-Ometiláció növeli a nukleotidok hidrofóbságát és megvédi őket a nukleázok hatásától (Yildirim et al. 2014).
A felhalmozódó bizonyítékok azt mutatják, hogy a virális RNS 2'-O-metilációja (2'OMe-RNS) fontos szerepet játszik a sejtes veleszületett immunválaszok elkerülésében a gazdasejtekben (Dimitrova et al. 2019). Züst és munkatársai kimutatták, hogy a vírus RNS 2′ OMe-je hozzájárult az interferon (IFN) által közvetített antivirális válasz elkerüléséhez, ezáltal elősegítve a vírus replikációját (Züst et al. 2011). Vitali és Scadden azt is javasolta, hogy az IU-dsDNS elnyomja az MDA5 IFN stimuláló útvonalat (Vitali és Scadden 2010).
A helikáz C domén 1 (IFIH1) génnel indukált interferon egy citoplazmatikus RNS-helikázt kódol, más néven MDA5 (Melanoma differenciációval összefüggő protein 5), és ez egy RIG-I-szerű receptor (RLR), amely vírusellenes funkciót lát el a veleszületett immunitásban. vírus RNS-ek kimutatásával. Az MDA5 felismer egy 0,5–1 kb méretű RNS duplex szárszerkezetet, amely általában a picornavirális replikáció során képződik, és vírusfertőzéssel szembeni immunválaszt közvetít (Nejentsev és mtsai. 2009; Crow 2011). Az MDA5 a picornavírusok replikációja során keletkező hosszú vírus kettős szálú RNS-ek (dsRNS) kimutatásakor aktiválja az I. típusú interferon jelátviteli útvonalat. Tanulmányok kimutatták, hogy az MDA5 filamentumot képez a dsRNS hossza mentén, és az ATP-függő filamentek dinamikáját használja fel, hogy a dsRNS hossza alapján különbséget tegyen saját és nem én között (Toro et al. 2015). Kimutatták, hogy az MDA5 részt vesz a sejtek és a veleszületett/adaptív immunrendszer közötti áthallás modulálásában a citokinek és kemokinek helyi termelésével.
Az MDA5 expressziójában és/vagy aktivitásában bekövetkező változások kiválthatják a sejtválaszokat a dsRNS-re, amely a vírus replikációjának mellékterméke (Colli et al. 2010). Azt is kimutatták, hogy a flamentképződéshez kapcsolódó maradékok mutációja a filamentumképződés elvesztését és az MDA{5}}függő jelátvitelt eredményezi, kivéve egy pár mutációt, amelyek mérsékelten fokozzák a jelátvitelt. Ezek az eredmények arra utalnak, hogy az ATP-független mechanizmusok, azaz a szorosabb RNS-kötés és/vagy a stabilabb fehérje-fehérje kölcsönhatás valószínűleg felelősek az MDA5 filamentum képződésének megfigyelt stabilitásáért in vitro és a sejtekben a magasabb jelátviteli aktivitásért (Sohn és 2016.).
Smyth et al. (2006) és Nejentsev et al. (2009) leírták az IFIH1 gén egy ritka allélját, amely védelmet nyújt az 1-es típusú cukorbetegség (T1D) ellen. Ez az rs35667974 IFIH1 egynukleotidos polimorfizmus (SNP), ahol a konzervált izoleucin (kodon [ATT]) a #923. pozícióban valinná változik (kodon [GTT]), ritka változat, mivel a minor allélgyakoriság (MAF) C {{ 9}}.010031 (2655 egyed a 264690 fős teljes mintában) a TOPMED (Taliun et al. 2021) és a C = 0.016267 (3343 egyed összesen 205514 mintában) ALFA alapján (Phan et). 2020; Sherry et al. 2001). Az 1. táblázat a polimorfizmus gyakoriságának humán biogeográfiáját mutatja be a különböző kontinentális régiókban az ALFA projekt adatai alapján (Phan et al. 2020; Sherry et al. 2001). A későbbi vizsgálatok megerősítették, hogy ez a ritka allél ugyanolyan hatással volt a T1D-re, a pikkelysömörre (PS) (Li et al. 2010) és a psoriaticus arthritisre (PsA) (Budu-Aggrey et al. 2017). Éppen ellenkezőleg, ezt az SNP-t a spondylitis ankylopoetica (AS) (Ellinghaus és mtsai 2016), a Crohn-betegség (CD) kialakulásának kockázati tényezőjeként társították (Ellinghaus et al. 2016; Budu-Aggrey et al. 2017). ), valamint a colitis ulcerosa (UC) (Ellinghaus et al. 2016; Budu-Aggrey és mtsai 2017).
Chistiakov et al. (2010) kimutatták, hogy az MDA5 E627X és I923V funkcióvesztéses mutációi az 1-es típusú cukorbetegségben szenvedő betegek perifériás vér mononukleáris sejtjeiben alacsonyabb poli(I:C)-indukált interferontermeléssel járnak, és ezért T1D-védő hatásúak. Azt is állítják, hogy az MDA5 molekulában az I923V aminosav szubsztitúció egy H927 aminosav közelében található, ami hozzájárul a dsRNS kötődéséhez (Yoneyama és Fujita 2008). Az MDA I923V-változatról azonban kimutatták, hogy normálisan képes dsRNS-t kötni, de a katalitikus aktivitás 2{15}}szeresére csökkent (Shigemoto et al. 2009). Ezért úgy tűnik, hogy ez a polimorfizmus nem befolyásolja jelentős mértékben ennek a citoplazmatikus RNS-t érzékelő helikáznak a nukleotid-savkötő tulajdonságait, de megváltoztatja működését egy még ismeretlen mechanizmus révén.

Összefüggést találtak az IFHI1 polimorfizmus és az enterovírus fertőzés incidenciája között T1D-ben, valamint az MDA5 I923V variáns és az enterovírus RNS gyakorisága közötti összefüggést T1D betegekben (Looney et al. 2015). Ezenkívül az MDA{6}} és MAVSknockout egereken végzett közelmúltbeli vizsgálatok kimutatták, hogy ezek a fehérjék kritikus szerepet játszanak a Coxsackie B vírus elleni 1-es típusú interferonválasz közvetítésében (Wang et al. 2010). A mengovírus vezető fehérjéről kimutatták, hogy megakadályozza az IFN-expressziót azáltal, hogy blokkolja az IRF3 dimerizációját, amely ennek a faktornak az aktiválásához szükséges (Hato et al. 2007). Ez a megfigyelés arra utal, hogy azokat a változatokat, amelyek megzavarják az IFIH1 funkcióját a gazdaszervezet antivirális válaszában, negatívan választották ki, nem pedig pozitívan, mert védelmet nyújtanak a T1D ellen (Crow 2011).

Chow et al. (2018) széles körben elemezték többek között a RIG-I-szerű receptorokat, míg Brisse és Ly (2019) az MDA5 és a kapcsolódó RIG-I evolúcióját és speciációját vizsgálták átfogóan. A megváltozott aminosavak elhelyezkedése az RNS-kötő és ATP-kötő helyeken vagy a filamentum határfelületén vagy annak közelében arra késztetett bennünket, hogy feltételezzük, hogy a megfigyelt mutációk fokozhatják az IFIH1 filamentum stabilitását az IFIH1 és a dsRNS vagy az IFIH1 közötti belső affinitás növelésével. molekulák a filamentumban, vagy az ATP hidrolízis hatékonyságának és ezáltal a filament szétszedésének sebességének csökkentésével (Rice et al. 2014).
Ez a munka az IFIH1 autoimmun lókusz megosztott rs35667974 variánsának potenciális szerepének szerkezeti tanulmányát mutatja be, amely a jelentések szerint gátolt funkciójú fenotípushoz vezet, amely Ile923Val aminosav szubsztitúciót kódol az MDA5 IFIH1 génfehérje termékében. Ez utóbbi egy biológiailag valószínűsíthető ok-jelölt gén, amely számos betegségben megoszlik, és befolyásolja az autoimmunitás ellen védő citokinek és kemokinek lokális expressziójának szabályozását (Colli et al. 2010). E munka célja annak az ismeretlen mozdulatlan mechanizmusnak a feltárása, amellyel az Ile923Val szubsztitúció csökkenti a humán MDA5 katalitikus aktivitását. Ebben a tanulmányban az MDA5 és a dsRNS közötti kölcsönhatásban mutatkozó különbségeket vizsgáltuk a natív és a ritka Ile923Val variáns között a gyulladásos mechanizmus beindításában. Ennek megfelelően az volt a célunk, hogy megvizsgáljuk a humán MDA5/dsRNS komplex dinamikus viselkedését vizes környezetben Ile923 vagy Val923 jelenlétében, ha az uracil 2'-O metilált vagy nem. A ritka, közös genetikai fogékonyság vagy protekciós lókuszok szerkezeti elemzése betekintést nyújthat az autoimmun betegségek patofiziológiájának megértéséhez, és a kutatási eredmények befolyásolhatják a vizsgált betegségek jobb kezelését.
Anyagok és metódusok
Szekvencia-visszakeresés, filogenetikai faépítés és pozitív szelekciós elemzés
A Homo sapiens fehérjeszekvenciáját (szekvenciaazonosító: NP_071451.2) az UniProt adatbázisból (The UniProt Consortium 2021) kértük le. A fajok közötti homológok megtalálásához BLAST-keresést végeztünk a Mega BLAST-tal (National Center for Biotechnology Information, NCBI, Bethesda, MD, USA) a RefSeq és NR fehérje adatbázisban (valamint a PDB és az UniProt) Blastp (protein-protein BLAST) segítségével. alapértelmezett paraméterek (Altschul et al. 1997). Kezdetben a humán MDA5 fehérjék 1000 homológját választották ki, és a humán I923V szubsztitúció körüli szekvenciát tartalmazó C-terminális doménre összpontosító fajokon átívelő szelekciót alkalmaztak a variáció azonosítására más fajokban. A Clustal Omegát, a többszörös szekvencia-illesztési programot (Clustal-O) (Sievers és mtsai, 2011) és a T-Cofee többszörös szekvencia-illesztési szervert (Notredame et al. 2000; Di Tommaso et al. 2011) használták a fehérjeszekvencia-illesztéshez és az Unipro UGENE platform bioinformatikai szoftvere (Okonechnikov et al. 2012) több igazítás szelektív megjelenítésére.
Az evolúciós elemzést a fajok között erősen konzervált fehérjeszekvenciák pozícióinak azonosítására használják, jelezve a szerkezeti fontosságot (Andreou et al. 2018). A filogenetikai fát a Maximum Likelihood módszerrel (Nei és Kumar 2000) és a Tamura–Nei modellel (Tamura és Nei 1993) 500 bootstrap ismétléssel (Felsenstein 1985) állítottuk össze. A heurisztikus keresés kezdeti fája(ka)t automatikusan megkaptuk a Neighbor-Join és BioNJ algoritmusok alkalmazásával a Tamura–Nei modell segítségével becsült páronkénti távolságok mátrixára, majd kiválasztottuk a felsőbbrendű log-likelihood értékkel rendelkező topológiát. A filogenetikai analízis a humán IFIH1 gén 52 homológ nukleotid szekvenciáját (39 ortológot és 13 paralógot) érintette. A benne foglalt kodonpozíciók az 1. plusz 2. plusz 3. plusz Noncoding voltak. A végső adatkészletben összesen 3729 pozíció volt. Az evolúciós elemzéseket a MEGA11 szoftvercsomag segítségével végeztük (Tamura et al. 2021).
Annak kimutatására, hogy az IFIH1 gén adaptívan fejlődött-e, a PAML v4.9j szoftvercsomag codeml programját használtuk (Yang 2007). A nukleotidszekvenciát és a megfelelő fehérjeszekvencia-illesztési fájlt benyújtottuk a PAL2NAL-nak (Suyama et al. 2006), hogy létrehozzák a megfelelő CODEML bemeneti nukleotid-illesztési fájlokat. Az ortológ MDA5 gének pozitív szelekciós analízisét hely- és elágazóhely-modellek segítségével végeztük (Yang et al. 2005; Yang és Bielawski 2000). A nem szinonim/szinonim szubsztitúciós arány arány (ω=dN/dS) a szelektív nyomás mértékét adja az aminosavak szintjén. A dN/dS (ω) értékének nagysága a kiválasztás típusait jelenti: ω<1 for negative selection, ω=1 for neutral selection, and ω>1 a pozitív szelekcióra (Yang et al. 2005). A CODEML-ben a telephely-modelleket (M0, M1, M2, M3, M7 és M8) és a fióktelep-modelleket (A és C osztály) választottuk ki a pozitív szelekciós elemzés elvégzésére (Bielawski és Yang 2004; Yang és Nielsen 2002). A helyszíni modellekben a valószínűségi arány tesztet (LRT) használták a pozitív szelekció tesztelésére a három modellpár (M0/M3, M2/M1 és M7/M8) összehasonlításával. Az elemzést mind a teljes hosszúságú szekvenciára, mind a C-Terminal Domain (CTD) szekvenciára elvégeztük.
Strukturális elemzés és molekuláris dinamikai szimulációk
A hMDA5–dsRNS filamentum krioelektronmikroszkópos (krio-EM) szerkezetét ATP jelenlétében (PDB ID: 6GKM) (Yu et al. 2018) (Berman et al. 2000) használták modellrendszerként a molekuláris dinamikához ( MD) szimulációk. Minden fehérjemaradék feloldódott (307–1020), a 14 bázispár kétszálú RNS (dsRNS) és a koordinált cink megmaradt, míg a hiányzó maradékokat a SWISS-MODEL szerverrel modellezték (Waterhouse et al. 2018). Az erőtér paramétereit és a hidrogénatomokat az AMBER 18 XLEaP moduljával adtam hozzá (Case et al. 2005). Az F14SB (Maier et al. 2015) és az f99OL3 (Zgarbová et al. 2011) AMBER erőtereket használtuk a fehérje, illetve az RNS esetében, a modrna08 (Aduri et al. 2007) paraméterekkel a módosított nukleozidok esetében. Az I923V mutációt az I923 Cδ metilcsoportjának manuális eltávolításával vezették be az MDA5-be, míg az U12 módosított ribózt 2′-O-nál metilálták a modrna08 könyvtár maradékának MRU használatával. A cinkiont a 4 cisztein-maradékhoz (907, 910, 962 és 964) kötötték, megfelelő erőtér-paraméterek alkalmazásával a tetraéderes koordinációs gömb megtartása érdekében (2,35 Å Zn–S kötéshosszak 50 kcal·mol–1·Å–1·Å) erőállandók és 109,5 fokos S–Zn–S szögek 25 kcal·mol–1·rad–2).
Ily módon 4 rendszert készítettünk elő az MD szimulációkhoz: (i) a natív MDA5–dsRNS, (ii) MDA5(V923)–dsRNS, (iii) MDA5–dsRNS(2′OMe) és (iv) MDA5( V923) – dsRNS(2′OMe). Az összes rendszert csonka, oktaéderes oldószeres dobozokban, előre kiegyensúlyozott TIP3P vízmolekulákban szolvatáltuk, a komplex körül legalább 10 Å pufferrel, majd a szükséges számú elleniont hozzáadtuk a rendszerek töltéssemlegesítéséhez. Az MD szimulációkat a PMEMD (Salomon-Ferrer et al. 2013) modul GPU-gyorsított változatával, AMBER 18-ban és 2 fs-os időlépéssel végeztük. A hőmérséklet szabályozása Langevin termosztáttal történt 1,0 ps–1 ütközési gyakorisággal, míg a nyomás szabályozása Berendsen barosztáttal történt 1,0 ps nyomásrelaxációs idővel. A SHAKE-et a hidrogénatomokat tartalmazó kötések 10-6 Å tűréssel történő korlátozására használták, míg a nem kötött kölcsönhatásokat 10 Å közvetlen térhatárral számítottuk.
Az energiaminimalizálást kezdetben 1{{20}},000 lépésben, 100 kcal·mol–1·Å–2 erőállandós helyzetkorlátozással végeztük. az MDA5–dsRNS nem hidrogénatomjain. Az oldószert ezután 300 K-en és 1 atm-en egyensúlyba hoztuk rövid szimulációs körökkel az NVT és NPT együttesekben, 100 ps, illetve 400 ps, miközben megtartottuk az oldott anyag nem hidrogénatomjaira vonatkozó korlátozásokat. Ezt követően 10,000 lépésben energiaminimalizálást végeztünk, de 10 kcal·mol–1·Å–2 pozíciókorlátozással csak az MDA5 C atomjain és a dsRNS foszfát gerincén. 3 subban fokozatosan ellazítottuk (10,0, 1,0, 0,1 kcal·mol–1·Å–2) 1 ns-on keresztül, majd 9 ns korlátlan egyensúlyozás következett állandó nyomáson. A kezdeti 10 ns-os (az elemzésben nem használt) kiegyensúlyozás után 100 ns-os termelési szimulációt végeztünk az NPT-együttesben minden rendszernél 300 K-n és 1 atm-en, miközben a rendszer pillanatfelvételeit 5,0 ps-ként tároltuk a CPPTRAJ segítségével történő elemzéshez. AMBER 18 modulja (Roe és Cheatham 2013). Az összes 3D modellt ábrázoló ábra a PyMOL molekuláris grafikus rendszerrel (v.2.3 nyílt forráskódú build) készült.
Eredmények
Az MDA5 Ile923Val szubsztitúciójának filogenetikai elemzése
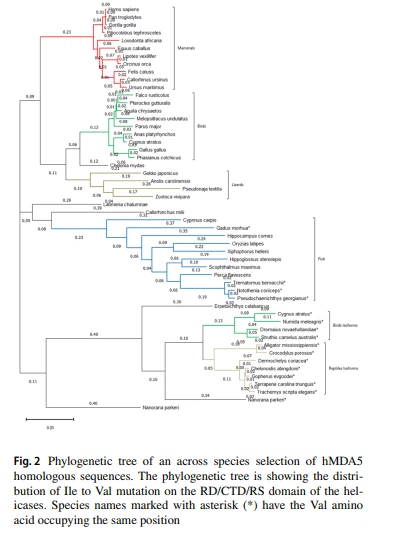
Az MDA5 és a kapcsolódó RIG-I fejlődését és specifikációját részletesen áttekinti (Brisse és Ly 2019). Itt az IFIH1 evolúciót alkalmazták az MDA5 szekvenciában az adott polimorfizmusra vonatkozó konzervációs elemek meghatározására. Az evolúciós analízis erős szekvencia-konzervációt mutatott ki a különböző fajok MDA5-je között (1000 vizsgált szekvenciából 984-ben van izoleucin a hMDA #923 ekvivalens pozíciójában) az RD/CTD doménben, ami szerkezeti/funkcionális fontosságot mutat. Az rs35667974 polimorfizmus a humán gén 14. exonjában konzervált aminosavmutációt okoz a hMDA5 Ile-től Val 923-as pozíciójában. Azonban van egy másik tizenhat távoli faj, amelyek ugyanazt a pozíciót foglalják el egy valinnal (1. ábra), ami jelzi, hogy ez a változás a fajok között életképes az MDA5 RD/CTD doménjében és az X1 izoforma szorosan homológ RS/GY doménjében, X3 és DHX58 helikázok (2. ábra). Ezenkívül a hMDA #923 pozíció körüli régió szekvencia-illesztése (az MDA-k CTD interakciós hurok) egy mérsékelten vagy erősen konzervált szekvenciát tár fel a távoli fajok között, jelezve a régió fajok közötti funkcionális jelentőségét.
Pozitív szelekció észlelése
Annak kimutatására, hogy az IFIH1 gén adaptívan fejlődött-e, helymodelleket és elágazási modelleket használtunk a teljes gén és a CTD domén ortológjainak pozitív szelekciós elemzésére. A helyszínmodellekben nem azonosítottak pozitív szelekciós helyeket a CTD doménhez (2. táblázat). M0 állandó evolúciós sebességet jelent (ω=dN/dS=0.2) (2. táblázat). Néhány pozitív szelekción átesett helyet az M2- és M8-helymodell módszerrel azonosítottunk a teljes génre vonatkozóan (1. táblázat), bár nem az RNS-sel kölcsönható régiókban és a CTD doménben. A helyszínmodellekben ω (dN/dS) az<1 which indicates a highly conserved gene (Table 2, Suppl. Table 1). In the branch-site model, the human branch (as well as the primate's branch) was used as the foreground clade, the ω value was low, and no sites with posterior probability greater than 0.85 were identified (Suppl. Table 2).

A CTD tartomány C fióktelep-modellje esetében (3. melléklet) a webhelyek 33 százaléka az ω0=0 kategóriában fejlődik. 036. Mivel az ebbe a kategóriába tartozó lelőhelyek nem tesznek különbséget az ágtípusok között, mindkét ágtípus ω értéke azonos az ebbe a kategóriába tartozó lelőhelyekre. Ráadásul a helyszínek 55 százaléka az ω2 kategóriába tartozik. Mégis, ezeknek ω értékei vannak, amelyek az ág típusától függenek (ω20=0.25 és ω21=0). Ezenkívül a 39 ortológ MDA5 gén C elágazóhely-modellje esetében (kiegészítő 4. táblázat) a helyek 33 százaléka az ω0=0 kategóriában fejlődik. 027. Ezzel szemben a lelőhelyek 41 százaléka ω2 kategória alatt fejlődik. Mégis, ezeknek ω értékei az ág típusától függenek (ω20=0.25 és ω21=15.32).
Szerkezeti elemzés
Az elvégzett evolúciós elemzés azt mutatja, hogy az Ile923Val szubsztitúció nem egyedi variáns az emberi fajban, mivel a Val más fajokban is megtalálható az MDA5 szekvencia pozíciójában. Az MDA5 egy vírusos kettős szálú RNS (dsRNS) receptor, amely kulcsszerepet játszik az antivirális immunitásban a vírus RNS-re vonatkozó külön specifitása révén (Wu et al. 2013). Kimutatták, hogy a vírus mRNS 2′-O-metilációja fontos a veleszületett immunválaszokhoz, ezért azt feltételezték, hogy a 2′-O-metiláció egy molekuláris aláírás a saját és nem saját mRNS megkülönböztetésére. (Zust et al. 2011). Az Ile923Val szubsztitúció lehetséges szerepének vizsgálata az rs35667974 missense IFIH1 variánsban, elemeztük az MDA5–dsRNS filament krioelektronmikroszkópos (krio-EM) szerkezetét ATP jelenlétében (PDB ID: 6GKM) (Yu et al. 2018). A 923. pozíció a 921–927 hurkon található, amely közvetlenül kölcsönhatásba lép a dsRNS-sel (3A. ábra). Az Ile923 az U12 uridin 2'-ΟΗ-tól 4,8 Å-re helyezkedik el, és kölcsönhatásukat a szomszédos His927 és az uracilbázis közötti hidrogénkötés stabilizálja. Az Ile923 Val-val való helyettesítése az rs35667974 variánsban várhatóan nem vezet be sztérikus ütközéseket, ahelyett, hogy minimalizálná az U12 uridin 2'-ΟΗ-jával való kölcsönhatásokat (3B. ábra). Abban az esetben, ha az RNS az U12 ribózánál metilálódik, akkor az Ile923-mal rendelkező természetes MDA5-változat kedvező van der Waals-kontaktust mutat az U12 2'-OMe-csoportjával 3,6 Å-nél (3C. ábra), míg az rs35667974-es változat Val923-a. 5,0 Å-nél található (3D. ábra). Ezek a különbségek nem utalhatnak az Ile923Val szubsztitúció jelentős hatására önmagában; azonban a finom szerkezeti változások gyakran jelentős funkcionális változásokhoz vezetnek a rendszer szerkezeti dinamikájának megzavarása révén.
Molekuláris dinamikai számítások
Az MDA5 I923V mutációjának a natív és 2'-Ο-metilált dsRNS-sel való kölcsönhatásának vizsgálatára 4 rendszer molekuláris dinamikai szimulációit alkalmaztuk 100-ns időskálán. A rendszerek dinamikáját az egyes fehérjemaradékok négyzetes ingadozásainak (RMSF) és a H927 U12-vel való hidrogénkötési távolságának felhasználásával követtük (4. ábra). Számításaink azt sugallják, hogy az I923-nak V923-ra mutációja az MDA5-ben kisebb zavarokat okozott a dinamikában az RNS érintkezési régión belül (923-934. aminosavak) és a natív dsRNS-sel alkotott komplex fehérjék közötti interakciós hurkában (950-955) (4C. ábra). . Ez a megfigyelés hasonló volt az U12 2'-O-metilációja esetén, bár az MDA5 V923 mutáns karboxi-terminális régiójának általános dinamikájában kifejezettebb hatás volt megfigyelhető (4D. ábra).
Figyelembe véve a szomszédos H927-maradék és az uracilbázis kulcsfontosságú hidrogénkötési kölcsönhatását, MD-szimulációink azt sugallják, hogy a 2′-O metiláció nem befolyásolja azt a natív MDA5-ben (4E. ábra). A V923 mutáció azonban nem befolyásolja a H927 hidrogénkötését a natív dsRNS-ben, de destabilizáló hatást mutatott 2'-O-metiláció jelenlétében (4F. ábra). Összességében az MD szimulációink azt sugallják, hogy bár az MDA5 I923V mutációjának hatása a natív dsRNS-sel való kölcsönhatásban marginális, az MDA5/RNS komplex dinamikájára és stabilitására gyakorolt hatása jelentősebb, ha az uracil 2′-O-metilezett. .

Vita
Ez a tanulmány az IFIH1 autoimmun lókusz megosztott rs35667974 variánsának szerepének evolúciós és strukturális vizsgálatát mutatja be, amely a jelentések szerint az MDA5 módosított funkcionalitású fenotípusához vezet (Downes et al. 2010). Az evolúciós hely és elágazási hely modellek alkalmazása pozitív szelekciós elemzés elvégzésére azt jelzi, hogy az RNS-kölcsönhatási helyeken, ahol az rs35667974 polimorfizmus található, nincsenek pozitív szelekciós helyek. Sem a fióktelep-modellek nem utalnak arra, hogy a CTD doménben egy adott helyszín pozitív szelekción ment volna keresztül.
Ez összhangban van az Ile923Val variáns nagyon alacsony megjelenési gyakoriságával még az emberi populációban is (1. táblázat). Ennek ellenére az európai populáció a többihez képest egy nagyságrendnyi különbséggel rendelkezik a C allél gyakoriságában. A kis mintaszám figyelmen kívül hagyása nélkül a vizsgált polimorfizmus földrajzi eloszlása azt mutatja, hogy az európai populációban való megjelenése kiindulópontként az elmúlt években megváltozott életkörülményeknek és táplálkozásnak köszönhető. A vizsgált SNP szerepének szerkezeti vizsgálatát a dsRNS–MDA5 (natív és mutáns) komplex szerkezetének vizsgálatával végeztük.
A dsRNS-MDA5 komplexképződés szintjén az Ile923Val mutáció bejutása befolyásolja a protein C-terminális domén (CTD) kölcsönhatását a dsRNS-sel, a dsRNS egyszálának ribózcukra mellett hidrofób üreg beépítésével. . Kimutattuk, hogy az egyik szál foszforibozil láncánál metilált RNS esetén további dinamikus hatások befolyásolhatják a mutáns kölcsönhatását, míg a vad típust nem. Ez összhangban van a kísérleti tanulmányokkal (Looney et al. 2015; Brisse és Ly 2019), amelyek azt mutatják, hogy az MDA5–dsDNS kölcsönhatási pont közelében azonosított Ile923Val polimorfizmus hatása nem befolyásolja a natív dsRNS-kötő tulajdonságokat, de megváltoztatja 2.{10}}szeresére csökkenti a katalitikus aktivitást (Shigemoto et al. 2009). Ezenkívül a molekuláris dinamikai vizsgálatok kimutatták a metiláció kritikus szerepét a mutánsban az MDA5 941–959. és 970–977. hurkok mobilitását és stabilitását illetően, amelyek részt vesznek a dsRNS kölcsönhatásban és az interprotein kölcsönhatásban az MDA filamentum kialakulásában. Az ilyen hatások akadályozhatják az MDA5 filamentum szerelvényt, az MDA5-MAVS asszociációt és a MAVS filamentum összeállítást, amelyek tovább aktiválják az I. típusú interferon gének (IFN1: IFN és IFN ) expresszióját. A T1D és a PsA esetében ennek következtében az MDA5 fehérje aktivitásának csökkenése és ezáltal az alacsonyabb IFN termelés véd az autoimmunitás ellen. Ezek a megfigyelések arra utalnak, hogy számos IFIH1 variáns, amelyek az előrejelzések szerint befolyásolják az MDA5 és a MAVS közötti interakciót és az IFN termelés csökkenését, csökkentik a betegségek kockázatát, miközben a normál MDA5 funkció társul hozzájuk (Shigemoto et al. 2009).
Ez arra enged következtetni, hogy a virális RNS-hez hasonlóan az ön-dsRNS-metiláció, egy RNS által azonosított mutáció, fontos szelekciós/aktivációs faktor bizonyos autoimmun betegségekben a védőhatások bevezetéséhez. A jelen tanulmány eredményei bővítik az IFIH1 lókusz rs35667974 SNP biológiai jelentőségével kapcsolatos ismereteket a fent említett betegségek kialakulásában, és rávilágítanak a közös gének több autoimmun betegség általi vizsgálatának fontosságára. Azonban az SNP-k autoimmun betegségekkel való genetikai asszociációjára irányuló populációs vizsgálatokban, például PCR-RFLP-k, szekvenálás vagy genotipizálás chipek alkalmazásával, az RNS-metiláció esetét nem veszik figyelembe. Ezért fontos ismerni a kölcsönható dsRNS metilációs állapotát és az MDA5 allélra gyakorolt hatását. Akárcsak a virális dsRNS-felismerés (Wu et al. 2013) és a saját- és nem-mRNS megkülönböztetése (Züst et al. 2011), a metilcsoport elvesztése a kölcsönhatásba lépő MDA5-ből, mint a mutáns Ile923Val MDA5, befolyásolhatja a filamentum kialakulását és az I. típusú interferon indukcióját.
Megjegyzendő, Plenge et al. (2013) korábban megvitatták, hogy egy ok-okozati betegség gén egy ritka változata a gyógyszeres beavatkozás feltételezett terápiás célpontja lehet. Ennek érdekében ismerni kell a kiváltó variáns biológiai funkcióját minden olyan kísérlet során, amely a genetikai leleteket új terápiás célponttal összekapcsolja. Ezért a kórokozó variáns helyzetének meghatározása az adott fehérje 3D szerkezetében, és szerepének szerkezeti/funkcionális szempontból történő vizsgálata egy autoimmun betegséghez vezető patogenetikai úton kulcsfontosságúnak tűnik a fehérje további kezelése és jobb kezelése szempontjából. a betegek. Továbbra is nagy szükség van arra, hogy a kapcsolódó SNP-k felfedezésén túl a kiváltó variánsok mélyebb megértése felé haladjunk, hogy tisztázzuk a betegségek molekuláris mechanizmusait és útvonalait. További szerkezeti-funkcionális elemzésre van szükség a ribóz-2′-Ο-metilált ön-dsRNS MDA5-höz való kötődésének, valamint az MDA5 fibrillum-összeállításának hatásának vizsgálatához. A 2'-Ο-metilált mRNS megfoghatatlan biológiai szerepe a vírus és a saját mRNS közötti különbség érzékelőjeként az I. típusú interferon indukálásában bizonyos autoimmunpátiák esetén védőérzékelőre is kiterjeszthető.


Következtetés
A ritka rs35667974 IFIH1 gén polimorfizmusa véd a T1D, PS és PsA ellen, míg a populáció többsége által hordozott IFIH1 allél hajlamosít a betegségekre. Az a finanszírozás, hogy a mutáns Ile923Val MDA5 eltérően működik a saját dsRNS-sel és különösen a 2'-O-metilált kölcsönhatásban, arra utal, hogy bizonyos esetekben a metilált dsRNS-sel kölcsönhatásba lépő változatok megzavarják az MDA5 filamentum képződését, a MAVS kölcsönhatást és a filamentum kialakulását, és Az IFN jelátvitel, akárcsak a gazdaszervezet antivirális válasza, negatívan szelektálható, mert védelmet nyújt a betegségek ellen.
Szerzői hozzájárulások
Koncepció – AA, AP, EEE és GNG, módszertan – AA, AP és EEE, érvényesítés – AA, AP, MIZ, GNG és EEE, vizsgálat – GNG, AA, AP és MIZ, források – GNG, AA, AP és MIZ, adatok gondozása – AA és AP, írás és eredeti piszkozat elkészítése – EEE, GNG, AA, AP és MZ, a kézirat írása, áttekintése és szerkesztése – AA, AP, MZ, GNG és EEE, vizualizáció – AA, AP és EEE, felügyelet – EEE és finanszírozás megszerzése – EEE. Minden szerző elolvasta és elfogadta a kézirat közzétett változatát.
Finanszírozás
A nyílt hozzáférésű finanszírozást a HEAL-Link Greece biztosítja. Ezt a munkát az "INSPIRED-The National Research Infrastructures on Integrated Structural Biology, Drug Screening Eforts and Drug Target Functional Characterization" című projekt (Grant MIS 5002550) támogatta, amely a "Kutatási és innovációs infrastruktúra megerősítése" alprogram keretében valósul meg. a „Versenyképesség, vállalkozói szellem és innováció” operatív program (NSRF 2014–2020), valamint Görögország és az Európai Unió (Európai Regionális Fejlesztési Alap) társfinanszírozásával.
Adatok elérhetősége
A jelenlegi vizsgálat során felhasznált és/vagy elemzett adatkészletek kérésre elérhetők a megfelelő szerzőtől.
Nyilatkozatok
Összeférhetetlenség
A szerzők nem nyilatkoznak összeférhetetlenségről. A finanszírozóknak nem volt szerepük a tanulmány megtervezésében; az adatok gyűjtésében, elemzésében vagy értelmezésében; a kézirat megírásában, vagy az eredmények közzétételéről szóló döntésben.
Etikai jóváhagyás
Nem alkalmazható.
Hozzájárulás a részvételhez
Nem alkalmazható.
Hozzájárulás a közzétételhez
Nem alkalmazható.

Nyílt hozzáférésű
Ez a cikk a Creative Commons Nevezd meg 4.{1}} Nemzetközi Licenc, amely lehetővé teszi a felhasználást, megosztást, adaptálást, terjesztést és reprodukálást bármilyen médiában vagy formátumban, feltéve, hogy megfelelő elismerést ad az eredeti szerző(k)nek. ) és a forrás, adjon meg egy hivatkozást a Creative Commons licenchez, és jelezze, ha változtatásokat hajtottak végre. A cikkben szereplő képek vagy egyéb harmadik féltől származó anyagok a cikk Creative Commons licencébe tartoznak, hacsak az anyag hitelkeretében másként nem szerepel. Tegyük fel, hogy az anyag nem szerepel a cikk Creative Commons licencében, és az Ön tervezett felhasználását nem engedélyezi a törvényi szabályozás, vagy meghaladja a megengedett felhasználást. Ebben az esetben közvetlenül a szerzői jog tulajdonosától kell engedélyt kérnie.
Hivatkozások
1. Aduri R, Psciuk BT, Saro P és munkatársai (2007) AMBER erőtér paraméterei az RNS-ben természetesen előforduló módosított nukleozidokhoz. J Chem Theory Comput 3:1464–1475.
2. Altschul SF, Madden TL, Schäfer AA és mtsai (1997) Gapped BLAST és PSI-BLAST: a fehérjeadatbázis-kereső programok új generációja. Nucleic Acids Res 25:3389–3402.
3. Andreou A, Giastas P, Christoforides E, Eliopoulos EE (2018) Strukturális és evolúciós betekintések a bacillus anthracis és a bacillus cereus poliszacharid-dezacetiláz géncsaládjába.
4. Aučynaitė A, Rutkienė R, Tauraitė D et al (2018) Identification of a 2'-O-methyluridin nucleoside hydrolase using the metagenomic libraries. Molekulák.
5.Berman HM, Westbrook J, Feng Z et al (2000) The protein data bank. Nucleic Acids Res 28:235–242.
6. Bielawski JP, Yang Z (2004) Maximális valószínűségi módszer az egyes kodonhelyek funkcionális eltéréseinek kimutatására, a géncsalád evolúciójára történő alkalmazással.
7. Biros E, Jordan MA, Baxter AG (2005) A környezeti interakciókat közvetítő gének 1-es típusú cukorbetegségben.
8. Boccaletto P, Machnicka MA, Purta E, et al (2018) MODOMICS: az RNS-módosítási útvonalak adatbázisa. 2017-es frissítés. Nucleic Acids Res 46:D303–D307.
9. Brisse M, Ly H (2019) A RIG-I-szerű receptorok: RIG-I és MDA5 összehasonlító szerkezet- és funkcióelemzése.
10. Budu-Aggrey A, Bowes J, Stuart PE et al (2017) Egy ritka kódoló allél az IFIH1-ben protektív a psoriaticus arthritis ellen. Ann Rheum Dis 76:1321–1324.
For more information:1950477648nn@gmail.com
