A melatonin megakadályozza a magas sótartalmú étrend által kiváltott T-limfociták beszűrődését a hipertóniás patkányok veséjébe azáltal, hogy megakadályozza a CXCR3 ligandum kemokinek expresszióját
Mar 14, 2022
További információ:ali.ma@wecistanche.com
Ariel Bier1, Rawan Khashab2, Yehonatan Sharabi1,2,3, Ehud Grossman1,2,3és Avshalom Leibowitz1,2,3,*
1Medicine D, The Chaim Sheba Medical Center, Tel-Hashomer 5262000, Izrael; arielbier@gmail.com (AB);Yehonatan.Sharabi@sheba.health.gov.il (YS); Ehud.Grossman@sheba.health.gov.il (EG)2 Hypertension Unit, the Chaim Sheba Medical Center, Tel-Hashomer 5262000, Israel;rawankhasbab@gmail.com3Sackler Orvostudományi Kar, Tel-Aviv Egyetem, Tel-Aviv 6997801, Izrael*
Absztrakt: Egy korábbi tanulmányunkban ezt bizonyítottukmelatoninmegakadályozzavesekárosodás a só által kiváltott magas vérnyomás modellben az oxidatív stressz csökkentésével. Feltételeztük, hogy ez a hatás magában foglalja a melatonin immunmoduláló tulajdonságait. In vivo Study-Dahl sóérzékeny (DSS) patkányokat normál étkezéssel, magas sótartalmú diétával (HSD) vagy HSD-vel ésmelatonin(30 mg/ttkg/nap) a vizükben nyolc hétig.Vesebegyűjtöttük a limfocita azonnali izolálása és jellemzése áramlási citometriával (CD3 plusz CD4 plus és CD3 plus CD8 plus), valamint limfocita kemoattraktáns (főleg CXCL) céljából.kemokinek) génexpressziós vizsgálatok. In vitro vizsgálat patkányokon mezangiális sejteket (RMC) tenyésztettünk magas sótartalmú táptalajban anélkül,melatonin. A HSD a CD4 plusz és CD8 plusz T limfociták jelentős renalinfiltrációjával járt a kontrollhoz képest. A melatonin jelentősen csökkentette a vese limfocita infiltrációját. A HSD szignifikánsan növelte a CXCL mRNS expressziójátkemokinek.A melatonin hozzáadása a HSD-hez megszüntette ezt a hatást. Az RMC sejtek sóval történő kezelése növelte a CXCL10 és CXCL11 expresszióját, de nem a CXCL9 expresszióját. Hozzáadásmelatonina táptalajhoz megakadályozta ezt a növekedést. A HSD-vel táplált patkányok melatoninnal történő kezelése csökkentette a vese limfocita kemoattraktáns mRNS expresszióját, és jelentősen csökkenti a vese T limfocita infiltrációját. A só közvetlen hatással lehet a kemokin-termelő vesesejtekre, amit a melatonin kezelés tompít.
Kulcsszavak:melatonin; só; T-limfociták; magas vérnyomás;vese; CXCL 9; CXCL 10; CXCL 11
1. Bemutatkozás
A hipertónia (HTN) a vezető módosítható kardiovaszkuláris kockázati tényező. A népesség elöregedése miatt a HTN prevalenciája folyamatosan növekszik, előrehaladott korban eléri a 30 százalékot [1]. A különféle orvosi terápiás lehetőségek ellenére a HTN globális kontrollja gyenge. Az ellenőrizetlen HTN következményei pusztítóak, és hatalmas negatív hatással vannak a közegészségügyre [2].
Különféle viselkedési, környezeti és genetikai tényezők vesznek részt a HTN patogenezisében. A nyugati étrend magas sótartalmát a HTN fő tényezőjeként tartják számon, és a megnövekedett megbetegedéssel és mortalitással jár. Az irányelvek és a nyilvános kezdeményezések a sóbevitel csökkentését javasolják a lakosság körében. Mindazonáltal nem mindenki részesülhet ebből a korlátozásból, mivel a sóérzékenységet a HTN-nel összekötő patofiziológiát nem ismerik teljesen, és jobb mechanikai ismereteket igényel [3]. Így az új stratégiák kulcsfontosságúak a HTN jobb megértéséhez és ellenőrzéséhez, ami azonnali igényt tesz új kutatási paradigmákra.
Úgy találták, hogy a gyulladás és az oxidatív stressz szerepet játszik az esszenciális HTN patogenezisében. A folyamatokat elindító és folytató triggerek kutatása során számos kísérleti HTN modell az adaptív immunválasz szerepére utal [4].

Kattintson ideA Cistanche előnyei és mellékhatásai a veseműködésre
Az adaptív immunitást a HTN-nel összekötő nyomok már az 1960-as évek óta léteznek. Azonban csak mostanában, az immunrendszer jobb megértésével lehetett előrelépést elérni ebben az irányban. Guzik és munkatársai úttörő tanulmánya. kimutatták, hogy az angiotenzin (Ang) II vagy a dezoxikortikoszteron (DOC) só HTN tompult rag1-/- egerekben, amelyekben hiányosak a T- és B-limfociták, és a T-sejtek, de nem a B-sejtek adoptív átvitele helyreállíthatja a vérnyomás-választ [5]. A jelen tanulmány óta a legtöbb általános állatmodellben különböző adoptív immunitáskomponensek relevánsak a HTN patogenezisében. A T-sejtek szerepét a só által kiváltott HTN-modellben szintén alaposan tanulmányozták. In vitro vizsgálatok azt mutatják, hogy a só a naiv T-sejtek differenciálódását TH17-sejtekké tolhatja [6]. Számos in vivo munka a magas sótartalmú diéta (HSD) által kiváltott HTN modellekben, mint például a Dhal-só-érzékeny (DSS) patkányokban, kiterjedt vese T-sejt-infiltrációt mutat [7–9].
A számos élettani folyamat közülmelatoninA vérnyomás szabályozásában való részvétel némileg intuitív. A vérnyomás cirkadián mintázata a melatonin és a HTN alapos kutatására ösztönöz. A múltban számos emberben és kísérleti modellben végzett munka kötötte az alacsony melatoninszintet a HTN-hez [10]. Vannak klinikai adatok, amelyek arra utalnak, hogy a melatonin-kiegészítés kezelheti a HTN-t, főként az éjszakai HTN-ben szenvedő betegeknél [11]. Ezen adatok következetlensége azonban felveti a kérdést, hogy a nem cirkadián melatonin tulajdonságai is szerepet játszanak-e a vérnyomás szabályozásában.
A melatonin gyulladásgátló és antioxidáns tulajdonságai azt sugallják, hogy a melatonin kölcsönhatásba lép az immunrendszerrel. Az újonnan feltárt adatok a melatonin jelátvitelének szerepét a T-sejtek fejlődésében, aktiválásában, differenciálódásában és a memóriában befolyásolják. Bizonyíték van rámelatoninmembrán és nukleáris receptorok jelen vannak a T-sejteken [12,13].Melatoninszámos, az immunválaszban részt vevő citokin termelődését befolyásolja, mint például az asinterferon (IFN) – amely a Th1 válasz kulcsfontosságú szabályozója [14].
Egyes kutatók szerint az oxidatív stressz és a T-sejtes válasz együttesen segíti elő a HTN és a szervi hipertóniás károsodás kialakulását [15]. Korábbi munkánkban ezt demonstráltukmelatonincsökkenti a helyi (vese) oxidatív stresszt és megelőzi a só által kiváltott vesefibrózist és proteinuriát egy sóérzékeny HTN patkánymodellben (a DSS-modellben) [16]. Mivel az oxidatív stressz döntő szerepet játszik a HTN-hez kapcsolódó adaptív immunválaszban, feltételeztük, hogy a melatonin immunmoduláló tulajdonságai felelősek a HSD által kiváltott HTN-ben betöltött védő szerepéért.
A tanulmány célja annak értékelése, hogymelatonincsökkenti a só által kiváltott T-sejt-választ, és tisztázza az e hatásért felelős mechanizmusokat.
2. Anyagok és módszerek
2.1. Állatok és vizsgálati jegyzőkönyv
A vizsgálati protokollt az izraeli Sheba egészségügyi központ intézményi állatetikai bizottsága hagyta jóvá. Egészségi állapotukat testtömeg méréssel, valamint az egyes állatok mozgásának és egészségi állapotának napi általános megfigyelésével követték nyomon. Négy hetes hím Dahl-sóérzékeny patkányok (RGD Cat# 1582190, RRID: RGD_1582190) állati létesítményben, szabályos ketrecekben (ketrecenként két patkány) 22 ◦C-on, 14 h világos/10 órás sötét ciklussal. A patkányokat normál sódiétán tartották, és ad libitum csapvizet kaptak inni ötnapos akklimatizációs időszakon keresztül. A patkányokat ezután három csoportra osztották (n=8), diéta szerint, 8 hetes időszak alatt. Az etikai bizottság szerint a betegség és a szenvedés jeleit mutató állatokat fel kellett áldozni.
A kontrollcsoport standard patkánytápot (2018 SC; Teklad Envigo, Madison, WI, USA) és csapvizet kapott; a magas sótartalmú diétás (HSD) csoport hozzáillő dúsított sótartalmú étrendet (4 százalék) (TD.120485; Teklad Envigo, Madison, WI, USA) és csapvízzel etetett, és amelatonincsoport ugyanazt a sóval dúsított étrendet (4 százalék) melatoninnal (M5250; Sigma, Rehovot, Izrael) (30 mg/kg/nap) etették az ivóvizükben. Rendszeresen mértük a testsúlyt és a vízfogyasztást. A megfelelő mennyiségű melatonint oldottuk fel a gyufa vízszükségletében minden ketrecben, hogy minden állat számára a megfelelő adagot adjuk ki. A nulladik nap a HSD és a melatonin fogyasztás megkezdésének napja. A vizsgálat végén a patkányokat 3 százalékos izofluránnal végzett mély érzéstelenítéssel leölték (az érzéstelenítés mélységét a hátsó láb szorítása igazolta), és avesebetakarították. Mindkét vesét eltávolították és félbevágták. A veséket áramlási citometriás analízishez vettük, kivéve néhány részt, amelyeket gyorsan eltávolítottunk, és folyékony N2-ben lefagyasztottuk, és –80 ◦C-on tároltuk. Fagyasztott anyagokat használtunk az RNS extrakciójához.

Cistanche-vesebetegség tünetei
2.2. Valós idejű kvantitatív reverz transzkripciós PCR
A gének mRNS expressziós szintjeit avesevalós idejű kvantitatív reverz transzkriptáz-PCR (qRT-PCR) segítségével. A teljes RNS-t a veseszövetből NucleoSpin RNA Kit (MACHERY-NAGEL, Düren, Németország) segítségével vontuk ki. A reverz transzkripciót Applied Biosystems High-Capacity cDNAReverse Transcription Kit (Applied Biosystems, Foster City, CA, USA) segítségével végeztük. A qRT-PCR reakciókat a Power SYBR Green PCR Master Mix (Applied Biosystems, Warrington, Egyesült Királyság) és az Applied Biosystems 7500 valós idejű PCR rendszerrel hajtották végre. A ciklus körülményei a következők voltak: egy első lépés 95 ◦ C-on 0,20 percig, majd 40 olvadási ciklus 3 másodpercig 95 ◦ C-on és egy meghosszabbított 30 s-os szakasz 60 ◦ C-on. A 40 ciklus végén olvadási görbét hajtottunk végre. Belső kontrollként a riboszomális fehérje laterális szár alegységének P0 (Rplp0) mRNS-ét használtuk. A primereket az 1. táblázat tartalmazza.
1. táblázat: A vizsgálatban használt patkányprimerek listája.

2.3. T-sejtek izolálása a vesékből
A vesekapszula eltávolítása után a kétveseledarálták és egy 2 ml-es fecskendő dugattyújával egy 100 µm-es sejtszűrőn keresztül ingerelték RPMI 1640-ben, amely 2 mML-glutamint, 10% FBS-t, 10 ug/ml DNáz 1-et (Stem Cells Technology, Cambridge, MA) tartalmazott. 0,1 százalék IV típusú kollagenáz (CLS 4, Worthington Decatur, AL, USA). Az oldatot 25 percig 37 °C-on inkubáltuk. Mosóoldatot (DPBS/2% FBS/2 mM EDTA) adtunk ezután a vesehomogenizátumhoz, hogy elérjük a 45 ml-t, és egy 70 µm-es cellaszűrőn szűrjük. Az oldatot 400 × g/7 perc sebességgel centrifugáltuk. és a pelletet 5 ml-es mosóoldatban szuszpendáltuk, 40 µm-es sejtszűrőn szűrtük, és 400 x g/7 perc sebességgel újra centrifugáltuk. A pelletet 3 ml FBS-ben (10 mM EDTA) újraszuszpendáltuk, Histopaque -1083 (Sigma, Rehovot, Israel) rétegre rétegeztük, majd kikapcsolt fék mellett 20 ◦C-on 400×g/30 perc sebességgel centrifugáltuk. A Histopaque feletti mononukleáris sejtréteget eltávolítottuk, kétszer mostuk mosóoldattal, és 5 ml-es mosóoldatban szuszpendáltuk áramlási citometriás analízishez.
2.4. Áramlási citometria
Minden csoportból,vese5-7 patkányból elemeztünk. Minden mintához 1 × 106 sejtet vettünk. Az izolált mononukleáris sejteket extracelluláris markerekkel inkubáltuk: anti-CD3-mal (Thermo Fisher Scientific Cat# 12-0030-82, RRID:AB_465493) és izotípus kontrolljával (Thermo Fisher Scientific Cat# 12-4742-41, RRID) :AB_10753770), anti-CD4 (Thermo FisherScientific Cat# 17-0040-80, RRID:AB_1210581) és izotípuskontrollja (Thermo Fisher Scientific Cat# 17-4724-81, RRID: AB_470188), anti-CD8 (Thermo Fisher Scientific Cat# 25-0084-82, RRID:AB_10548361) és izotípuskontrollja (Thermo Fisher Scientific Cat# 25-4714-80,RRID: AB_657914). Minden sejtet áramlási citometriával (BD FACSCalibur Flow Cytometry System, RRID: SCR_000401) elemeztünk a FlowJo szoftver (FlowJo, RRID: SCR-008520) segítségével.

Cisztanche-vesefunkció
2.5. Sejtkultúra
A mezangiális patkánysejtvonalat, az RMC-t (ATCC Cat# CRL{{0}}, RRID: CVCL_0506), az ATCC®-től szereztük be. A sejtet Dulbecco módosított Eagle tápközegében (01-055-1A, Biological Industries, Beit HaEmek, Izrael) tenyésztettük 4 mM L-glutamint 1,5 g/l nátrium-hidrogén-karbonátra és 4,5 g/l glükózra kiegészítve. 0,4 mg/mLG418 és 15% magzati szarvasmarha szérum. A melatonint a Sigmától (M5250 Rehovot, Izrael) szerezték be. A 250 mMmelatoninetanolban készült. A sejteket normál vagy magas sótartalmú (80 mM NaCl hozzáadása a táptalajhoz) körülmények között melatonin nélkül vagy melatoninnal (0,5 mM) tenyésztettük. A melatonin kezelést 45 perccel időzítettük, mielőtt NaCl-t adtunk a táptalajhoz. Az összes kísérletet 6 lyukú lemezeken végeztük, üregenként 3 × 105 sejttel, és 6 független vizsgálattal végeztük.
2.6. Statisztikai analízis
Az adatok átlag ± SEM formában jelennek meg. A statisztikai elemzéseket IBMSPSS Statistics (RRID: SCR_019096) segítségével végeztük. Az egytényezős varianciaanalízis (ANOVA) és a posthoc Tukey-módszer a csoportok közötti különbségeket vizsgálta. A valós idejű qPCR-adatokat DataAssist, RRID: SCR_014969 segítségével elemeztük.
3. Eredmények
3.1. A melatonin megvédi a HSD-t fogyasztó patkányokat
A patkányok életkora ebben a vizsgálatban 4-13 hetes volt. Ebben az életkorban a patkányok jólétét a súlygyarapodás jelzi, amelyet a kontrollcsoport mutatott ki [17]. A HSD-csoport azonban elérte a platót a 30. napon, és a hozzáadássalmelatonina HSD javította ezt a jelenséget (1A. ábra). A HSD csoport magas mortalitást mutatott, ahol a patkányok 50 százaléka elpusztult vagy olyan klinikai állapotba került, amely az állatetikai bizottság szabályai szerint eutanáziát igényelt a kísérleti időszakban. A melatonin-kiegészítők szignifikánsan megakadályozták a patkányok mortalitását, ahol nyolc patkányból csak egy pusztult el az 58. napon, a kísérleti időszak végén (1B. ábra).
1.ábra.Melatoninjavult a vérnyomás és a túlélés HSD-ben. A DSS-patkányokat 9 hétig kezelték HSD-vel melatoninnal és anélkül. A magas sótartalmú étrend csökkentette a testsúlyt a 36. naptól kezdve, és a melatonin mérsékelte ezt a hatást (A). A HSD növelte a halálozási arányt a 4. naptól 0. A HSD-fedrátok melatoninnal történő kezelése javítja túlélésüket. (B). (n=8) *-p Kisebb vagy egyenlő, mint 0,05 só és só plusz melatonin kontra kontroll. #-p Kevesebb vagy egyenlő, mint 0,05 só kontra kontroll és só plusz melatonin. HSD – magas sótartalmú étrend.

3.2. A melatonin megakadályozza a HSD által kiváltott vese T-sejtek beszűrődését
Sejteket izoláltunk aveseés a T-sejt-markerhez, a CD3-hoz kapuzta őket. A CD3 plusz sejteket CD4-re és CD8-ra kapuzták. Mind a CD3 plusz CD4 plus, mind a CD3 plusz CD8 plus szignifikánsan magasabb volt a HSD-ben (5,18 ± 1,62 és 4,6 ± 0,75 százalék) a kontrollhoz képest (0,16 ± {{18}). }.{{20}}2 illetve 0,95 ± 0,15 százalék) ésmelatonina HSD kiegészítése a CD3 plusz CD4 plus és a CD3 plusz CD8 plus sejtek visszacsökkent a kontroll szintre (0.68 ± 0.21 és 1.37 ± 0.45) (ábra 2A–D).
2. ábra. A melatonin megakadályozza a T-sejtek beszűrődését avese. A T-sejteket patkányok veséjéből izoláltuk, és CD3-ra kaptuk. A CD3-pozitív sejteket CD4-re és CD8-ra korlátoztuk. A melatonin (C) csökkentette mind a CD3 plusz CD4 plusz, mind a CD3 plusz CD8 pluszt a melatonin nélküli HSD-hez (B) képest, és nem különbözött a kontrollcsoporttól (A). Az összes patkány elemzését a (D) mutatja (n=7–8). HSD – magas sótartalmú étrend. *-p Kisebb vagy egyenlő, mint 0.05 versus kontroll. #-p Kisebb vagy egyenlő, mint 0,05, szemben a só plusz melatoninnal.

3.3. A melatonin csökkenti a vese bizonyos kemokinjait, amelyeket a HSD-ben felfelé szabályoztak
A T-sejtek gyulladásos szövetekbe való toborzását helyi kemokinexpresszió szabályozza. Ezért két kemokincsalád expresszióját mértük a patkányokbanvese: a kemokin (CXC motívum) ligandum (CXCL) család és a kemokin (C-Cmotif) ligand (CCL) család.
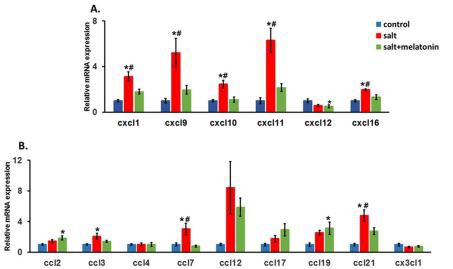
A CXCL család esetében a CXCL 9, 10 és 11, amelyek a T-sejteken lévő CXCR3 receptort használva vonzzák a T sejteket a célszöveteikhez, szignifikánsan felszabályozottak voltak HSD patkányokban. A kiegészítésemelatoninUgyanezt a mintát észleltük a CXCL 1 és 16 esetében. A CXCL12 esetében azonban nem észleltünk felszabályozást a HSD-ben (3A. ábra).
A CCL család esetében a CCL 2, 4, 12, 17, 19 és a CX3CL1 nem mutatott felszabályozást a HSD-ben. A CCL3 emelkedett volt HSD-ben, de nem észleltek szignifikáns változást a melatonin étrendhez való hozzáadásával. A CCL7 esetében jelentős felszabályozás a HSD-ben és jelentős leszabályozás a hozzáadásávalmelatonina HSD-hez (3B. ábra).
3. ábra FelszabályozásavesekemokinekHSD-ben melatoninnal és anélkül. Meghatároztuk a kemokin (CXC motívum) ligandum (CXCL) család (A), kemokin (CC motívum) ligandum család és a CX3CL1 (B) expresszióját patkányokban. (n=7–8) *-p Kisebb vagy egyenlő, mint 0.05 versus kontroll. #-p Kevesebb, mint 0,05 vagy egyenlő a só plusz melatonozással szemben. HSD – magas sótartalmú étrend.
3.4. A melatonin közvetlen hatása az RMC mesangiális sejtvonalra
Ezután a CXCL9-re, 10-re és 11-re összpontosítottunk, amelyek a CXCR3 receptorhoz kötődve vonzzák a T-sejteket. Meghatároztuk ezek kifejezésétkemokinekRMC sejtekben, amelyek patkány mezangiális sejtvonal.
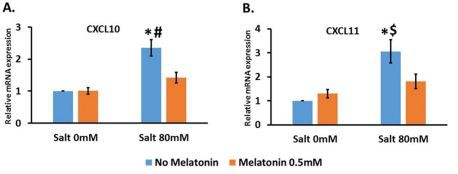
A sejteket 80 mM NaCl-dal kezeltük 0,5 mM nélkül és 0,5 mM-talmelatonin. Ez a NaCl-koncentráció szignifikánsan, 2,4 ± 0.26--szeresére növelte a CXCR10 expresszióját a kontrollhoz képest, és a hozzáadott 0,5 mM melatonin szignifikánsan csökkentette ez a kifejezés 1,4 ± 0.{{10}}-szeresére nőtt a kontrollhoz képest (4A. ábra). A CXCL11 esetében a 80 mM NaCl szignifikánsan, 3 ± 0.{16}}szeresére növelte az expressziót a kontrollhoz képest, 0,5 mM melatonin hozzáadása pedig szignifikánsan 1,8 ± 0-ra csökkentette ezt az expressziót.{22 }}hajtás a kontrollhoz képest (4B. ábra). A CXCL9 nem volt kimutatható az RMC sejtekben.
4. ábra: A só fokozta a CXCL10 és CXCL11 expresszióját egy mezangiális sejtvonalban, ahol a melatonkezelés csökkentette az expresszióját. Az RMC-t (patkányok mezangiális sejtvonala) 80 mM sóval kezeltük 0,5 mM melatoninnal és anélkül. A CXCL10 (A) és a CXCL11 (B) szinteket a sókezelés és azmelatonincsökkenteni ezt a felszabályozást. A grafikonok 6 független kísérletet mutatnak be. *-p Kisebb vagy egyenlő, mint 0.001 versus kontroll #-p Kisebb vagy egyenlő, mint 0.005 versus só 80 mM és melatonin 0,5 mM. $-p Kisebb vagy egyenlő, mint 0,05, szemben a 80 mM sóval és 0,5 mM melatoninnal.
4. Megbeszélés
Jótékony hatása amelatoninA HTN-ről korábbi tanulmányok kimutatták, és javasolták a kezelésre rezisztens HTN lehetséges hatásmechanizmusát [18]. Első vizsgálatunkban az oxidatív stresszre összpontosítottunk, és feltártuk, hogy a melatonin csökkenti a HSD által kiváltott oxidatív stresszt. Jelen tanulmányunkban az adaptív immunhatásra összpontosítottunk, és kimutattuk, hogy a melatonin javítja a HSD-vel táplált patkányok túlélését. Ez a hatás a vesébe beszivárgó T-sejtek számának csökkenésével és a vese szabályozásának csökkenésével járvesekemokin expresszió.
Történelmi adatok azt mutatják, hogy a HSD-t fogyasztó DSS-patkányokban súlyos HTN alakul ki, és magasabb mortalitási arányt mutatnak [19]. Dahl maga számolt be a modell létrehozásakor, hogy amikor a DSS-patkányokat elválasztáskor (21-23 napos korukban) HSD-re (8 százalék NaCl) helyezték, gyorsan kifejlődött bennük a HTN, és a sótáplálás 16. hetére valamennyien elpusztultak [20]. Később, a törzs néhány módosítása után Rapp et al. beszámoltak arról, hogy a HSD (8 százalékos NaCl) nyolc héten belül minden patkány elpusztult [21]. A vizsgálatunkban részt vevő patkányok elhullási aránya magas volt, de nem érte el a 100 százalékot, valószínűleg az alacsonyabb (4 százalékos) sótartalom miatt az étrendjükben. Ennek ellenére nyilvánvaló, hogymelatonina kiegészítés jelentősen megakadályozta a mortalitást.
A súlygyarapodás a patkányok jólétének markere 4-13 hetes korban. A DSS patkány a Sprague Dawley-től származik, amely egy jól jellemzett törzs. A kísérleteinkben használt patkányok korában a patkányoknak következetesen hízniuk kell [22]. Számos állatkísérletben a súlycsökkentést tekintik a kísérletek egyik „végpontjának” [23]. Számos tanulmányból világos, hogy a HSD DSS patkányokban alacsonyabb súlygyarapodást eredményez a kontrollokhoz képest [24,25]. Ezekkel a vizsgálatokkal összhangban súlykülönbségeket is megfigyeltünk a csoportok között. Itt a patkányok nem híztak négy hét HSD után. A melatonin a HSD ezen hatását is megállította, mivel a melatoninnal kezelt patkányok súlya tovább hízott, bár kisebb mértékben, mint a kontrollok.
Az a képesség,melatoninA 20. század hetvenes évek végén fedezték fel a vérnyomás csökkentését állatmodellekben [26–28]. Azóta több más modellben is beszámoltak róla, például arról, hogy a magas fruktóztartalmú étrend metabolikus szindrómát vált ki spontán hipertóniás patkányokban [29,30]. Ezen a területen végzett vizsgálataink az elsők, amelyek kimutatták, hogy a melatonin szerepet játszik a só által kiváltott HTN-ben azáltal, hogy megakadályozza a szervkárosodást és csökkenti a mortalitást.
Ebben a tanulmányban kimutattuk, hogy a HSD T-limfocita infiltrációt indukál aveseEz a folyamat, amelyet főként Mattson csoportja ír le DSS-patkányokban [31–33]. Ennek a beszűrődési folyamatnak a DSS-modellben betöltött döntő szerepét egy újabb tanulmány bizonyítja, amely azt figyelte meg, hogy a T-sejt-hiányos DSS-patkányok védettek a A HSD és a lépsejtek transzfer által indukált HTN súlyosbítja a sóérzékeny HTN-t [34].
A melatonin számos szempontból befolyásolhatja a T-sejteket (lásd [35]). Ez a tanulmány először mutatta meg eztmelatonincsökkenti mind a CD4 plus, mind a CD8 plus Tsejtek vonzását avesea HSD-ben. A melatoninnak ez a hatása lehet az a mechanizmus, amely aláhúzza jótékony hatását ebben a modellben.
A melatonin T-sejt-infiltrációt csökkentő képességét a kísérleti autoimmun encephalomyelitis (EAE) egérmodellben írták le. Az EAE-ben kimutatták, hogy a melatonin csökkenti a CD4 plusz T sejtek és a Th17 sejtek beszűrődését a központi idegrendszerbe [36,37].
A T-sejtek egy adott szövethez való vonzódását főként a helyi magas koncentráció szabályozzakemokinekamelyek kemotaktikus citokinek, amelyek szabályozzák az immunsejtek migrációs mintázatát és elhelyezkedését. A T-sejt-infiltrációt kiváltó két nagy kemokincsalád a CXC motívum ligandum (CXCL) és a CC motívum ligandum (CCL) kemokincsalád [38].

Cistanche a veseműködési zavarok javítására
Vizsgálatunkban nem találtunk állandó mintát a CCL család válaszában a HSD-re és amelatonin. A kilencbőlkemokinekebben a családban csak a CCL7 és a CLL21 esetében figyelték meg, hogy növelték expressziójukat a HSD miatt, és a melatonin kiegészítés csökkentette ezt. A HSD növelte a CCL3 expresszióját, de nem észleltek csökkenést a melatoninnal kezelt patkányokban. Egy közelmúltban, ugyanebben a modellben végzett tanulmány kimutatta, hogy a HSD felszabályozza a CCL2-tveseRNA-Seq módszerrel [39]. Ez a tanulmány azonban a diéta kezdete utáni 3. és 21. napon tesztelte a szinteket. Tanulmányunkban nyolc hét után teszteltük a szinteket. Lehetséges, hogy a kemokin expressziója megváltozik a HSD periódus alatt.
Ezzel szemben a CXCL család legtöbbjének, beleértve a CXCL 1-et, 9-et, 10-et, 11-et és 16-ot, szintje megemelkedett a HSD-vel kezelt patkányokban, ésmelatonina kiegészítés megszüntette ezt a növekedést.Csak a CXCL12 nem mutatott növekedést a HSD-re adott válaszreakcióban.
A CXCL9, CXCL10 és CXCL11, amelyeket „interferonnal indukálható CXC kemokin receptor 3 liganduknak” neveznek, IFN-indukálja, és a CXC kemokin receptor 3 (CXCR3) ligandumai. In vivo vizsgálatok kimutatták fontosságukat a T-limfociták aktiválásában és a célszervhez való toborzásában [40–42]. Youn et al. humán hipertóniás betegeknél mind a T-sejtek veseinfiltrációját, mind a három CXCR3 emelkedett keringési szintjét mutatta.kemokinek, ami arra utal, hogy a CXCR3 és ligandumai relevánsak a humán HTN-ben részt vevő T-sejtek számára [43]. Egy másik tanulmány kimutatta, hogy a CXCL10 szintje emelkedett hipertóniás betegekben, és szintje korrelál a vérnyomásértékükkel [44].
Ezeknek a vizsgálatoknak köszönhetően a CXCL9, CXCL10 és CXCL11-re összpontosítottunk. A mezangiális patkány sejtvonalat tenyésztettük, és 80 mM NaCl-dal és 0,5 mM melatoninnal kezeltük. Megállapítottuk, hogy a CXCL 10 és 11 a sejtekben szabályozottabb, és a melatonin megszünteti ezt az emelkedést. Eredményeink azt mutatják, hogy a só hatása a CXCL 10 és 11 emelésére, és ezzel ellentétes hatásamelatonin, mindkettő közvetlenül kimutatható volt a mezangiális sejtekben. Ezzel szemben a CXCL9-et nem mutatták ki ezekben a sejtekben.
Tanulmányunknak korlátai vannak. FACS-eredményeink szerint sok CD3 plusz kettős negatív volt mind CD4, mind CD8 esetében. Ugyanezek az eredmények voltak Mattson 2010-es tanulmányában [31]. Azonban Mattson csoportjának újabb tanulmányaiban a CD3 plusz CD4-CD8-sejt nagyon kevés volt [32,33,45,46]. A kettős negatív CD3 sejtek számának jelentős csökkenése a CD45 marker hozzáadásának és csak a CD45-pozitív sejtek elemzésének eredménye lehet, amit Mattson későbbi tanulmányaiban is elvégeztek. Lehetséges, hogy a CD3 plusz CD4-CD8- nagy tömege műtermék. Azonban nem ismert műtermék a CD3 plusz CD4 plus és a CD3 plusz CD8 plus sejtpopulációról.
5. Következtetések
Összefoglalva, a magas sótartalmú étrend összefügg a T-sejtek beszivárgásával aveseDSS patkányok. A só szintén növelte a specifikus T-sejt-kemoattraktánsok expresszióját a vesében. Kezelés amelatonin(30 mg/ttkg/nap) megszüntette ezeket a hatásokat (melatonincsökkenti a T-sejtek HSD-indukálta infiltrációját a vesékbe, valamint csökkenti a CXCL3 ligandum kemokin expresszióját).
In vitro vizsgálatunk kimutatta, hogy a só és a melatonin szabályozhatja a kemoattraktánsok expresszióját azáltal, hogy közvetlenül befolyásoljavesesejteket.
A szerző közreműködése: Conceptualization, AL; formális elemzés, AB és RK; vizsgálat, RK;módszertan, AB és AL; írás – eredeti tervezet, AB és AL; írás – áttekintés és szerkesztés, YSand EG Minden szerző elolvasta és beleegyezett a kézirat közzétett változatába.
Finanszírozás: Ez a kutatás nem kapott külső támogatást.
Az intézményi felülvizsgálati bizottság nyilatkozata: A vizsgálati protokollt a Sheba egészségügyi központ intézményi állatetikai bizottsága hagyta jóvá, a 1219/19/ANIM protokoll és az Egészségügyi Minisztérium 16418. számú jegyzőkönyve.
Tájékozott hozzájárulási nyilatkozat: Nem alkalmazható.
Adatelérhetőségi nyilatkozat: A jelen tanulmányban bemutatott adatok a megfelelő szerzőtől kérésre rendelkezésre állnak.
Köszönetnyilvánítás: A szerzők köszönetet mondanak Zehava Shabtai-nak kiváló technikai támogatásáért és Michael Kanovsky-nak szerkesztői szolgáltatásaiért.
Összeférhetetlenség: A szerzők nem nyilatkoznak összeférhetetlenségről.

Hivatkozások
1. Olsen, MH; Angell, SY; Asma, S.; Boutouyrie, P.; Burger, D.; Chirinos, JA; Damasceno, A.; Delles, C.; Gimenez-Roqueplo, AP; Hering, D.; et al. Felhívás cselekvésre és életútra vonatkozó stratégia a megemelkedett vérnyomás jelenlegi és jövő nemzedékekre nehezedő globális terheinek kezelésére: A Lancet Bizottság a hipertóniával kapcsolatban. Lancet 2016, 388, 2665–2712. [CrossRef]
2. O'Brien, E. The Lancet Commission on hypertonia: A megemelkedett vérnyomás globális terheinek kezelése a jelenlegi és a jövő generációira. J. Clin. Hypertens 2017, 19, 564–568. [CrossRef]
3. O'Donnell, M.; Mente, A.; Yusuf, S. Nátriumbevitel és a szív- és érrendszer egészsége. Circ. Res. 2015, 116, 1046–1057. [CrossRef]
4. Schiffrin, EL A kis artériák átépülésének mechanizmusai, vérnyomáscsökkentő terápia és az immunrendszer hipertóniában.Clin. Investig. Med. 2015, 38, E394–E402. [CrossRef]
5. Guzik, TJ; Hoch, NE; Brown, KA; McCann, LA; Rahman, A.; Dikalov, S.; Goronzy, J.; Weyand, C.; Harrison, DG A T-sejt szerepe az angiotenzin II által kiváltott magas vérnyomás és érrendszeri diszfunkció genezisében. J. Exp. Med. 2007, 204, 2449–2460. [CrossRef][PubMed]
6. Kleinewietfeld, M.; Manzel, A.; Titze, J.; Kvakan, H.; Yosef, N.; Linker, RA; Muller, DN; Hafler, DA A nátrium-klorid patogén TH17 sejtek indukálásával autoimmun betegséget vált ki. Természet 2013, 496, 518–522. [CrossRef]
7. Mattson, DL; Lund, H.; Guo, C.; Rudemiller, N.; Geurts, AM; Jacob, H. Az 1. rekombinációt aktiváló gén genetikai mutációja Dahl-sóra érzékeny patkányokban csökkenti a magas vérnyomást és a vesekárosodást. Am. J. Physiol. Regul. Egész szám. Összeg. Physiol. 2013, 304, 407–414.[CrossRef]
8. Mattson, DL Infiltráló immunsejtek avesesóérzékeny magas vérnyomásban és vesekárosodásban. Am. J. Physiol. Ren. Physiol. 2014, 307. [CrossRef] [PubMed]
9. Lu, X.; Crowley, SD Gyulladás sóérzékeny hipertóniában és vesekárosodásban. Curr. Hypertens Rep. 2018, 20. [CrossRef][PubMed]
10. Baker, J.; Kempinski, K. Role ofmelatonina vérnyomás szabályozásában: Kiegészítő vérnyomáscsökkentő szer. Clin. Exp. Pharm.Physiol. 2018, 45, 755–766. [CrossRef] [PubMed]
11. Grossman, E.; Laudon, M.; Zisapel, N. A melatonin hatása az éjszakai vérnyomásra: Randomizált kontrollált vizsgálatok metaanalízise. Vasc. Egészségügyi kockázatkezelés. 2011, 7, 577–584. [CrossRef] [PubMed]
12. Pozo, D.; Delgado, M.; Fernandez-Santos, JM; Calvo, JR; Gomariz, RP; Martin-Lacave, I.; Ortiz, GG; Guerrero, JM. A Mel1a-melatonin receptor mRNS expressziója patkány csecsemőmirigyből és lépből származó limfociták T és B alcsoportjaiban. Faseb J. Off. Publ. Fed.Am. Soc. Exp. Biol. 1997, 11, 466–473. [CrossRef]
13. Guerrero, JM; Pozo, D.; García-Mauriño, S.; Osuna, C.; Molinero, P.; Calvo, JR. A nukleáris receptorok részvétele a melatonin általi fokozott IL-2-termelésben Jurkat sejtekben. Ann. NY Acad. Sci. 2000, 917, 397–403. [CrossRef] [PubMed]
14. Farez, MF; Mascanfroni, ID; Méndez-Huergo, SP; Yeste, A.; Murugaiyan, G.; Garo, LP; Balbuena Aguirre, ME; Patel, B.; Ysrraelit, MC; Zhu, C.; et al.MelatoninHozzájárul a sclerosis multiplex relapszusok szezonalitásához. Cell 2015, 162, 1338–1352.[CrossRef] [PubMed]
15. Kirabo, A.; Fontana, V.; de Faria, APC; Loperena, R.; Galindo, CL; Wu, J.; Bikinejeva, AT; Dikalov, S.; Xiao, L.; Chen, W. et al. A DC izoketálisan módosított fehérjék aktiválják a T-sejteket és elősegítik a magas vérnyomást. J. Clin. Investig. 2014, 124, 4642–4656. [CrossRef][PubMed]
16. Leibowitz, A.; Volkov, A.; Volosin, K.; Shemesh, C.; Barshack, I.; Grossman, E. A melatonin megakadályozzavesesérülést a magas sótartalmú étrend által kiváltott magas vérnyomás modellben az oxidatív stressz csökkentésével. J. Pineal Res. 2016, 60, 48–54. [CrossRef] [PubMed]
17. Hawkins, P.; Morton, DB; Burman, O.; Dennison, N.; Honess, P.; Jennings, M.; Lane, S.; Middleton, V.; Roughan, JV; Wells, S. et al. Útmutató a laboratóriumi állatok jóléti értékelésére vonatkozó protokollok meghatározásához és végrehajtásához: A BVAAWF/FRAME/RSPCA/UFAW Közös Munkacsoport tizenegyedik jelentése a finomításról. Labor. Anim. 2011, 45, 1–13. [CrossRef]
18. Simko, F.; Reiter, RJ; Paulis, L.Melatoninmint racionális alternatíva a rezisztens hipertónia konzervatív kezelésében.Hypertens Res. 2019, 42, 1828–1831. [CrossRef] [PubMed]
19. Rapp, JP Dahl sóérzékeny és sórezisztens patkányok. Hypertension 1982, 4, 753–763. [CrossRef]
20. Dahl, LK; Knudsen, KD; Heine, MA; Leitl, GJ A krónikus túlzott sófogyasztás hatásai. Kísérleti hipertónia módosítása patkányokban az étrend változtatásával. Circ. Res. 1968, 22, 11–18. [CrossRef] [PubMed]
21. Rapp, JP; Dene, H. Dahl sóérzékeny és sórezisztens patkányok beltenyésztett törzseinek fejlődése és jellemzői. Hypertens 1985,7, 340–349. [CrossRef]
22. Brower, M.; Grace, M.; Kotz, CM; Koya, V. Sprague Dawley patkányok növekedési jellemzőinek összehasonlító elemzése különböző forrásokból. Labor. Anim Res. 2015, 31, 166–173. [CrossRef]
23. Talbot, SR; Biernat, S.; Bleich, A.; van Dijk, RM; Ernst, L.; Häger, C.; Hilgers, SOA; Koegel, B.; Koska, I.; Kuhla, A.; et al.A testsúlycsökkentés humánus végpontként való meghatározása: Kritikus értékelés. Labor. Anim 2020, 54, 99–110. [CrossRef] [PubMed]
24. Geschka, S.; Kretschmer, A.; Sharkovska, Y.; Evgenov, OV; Lawrenz, B.; Hucke, A.; Hocher, B.; Stasch, J.-P. Az oldható guanilátcikláz stimuláció megakadályozza a fibrotikus szövetek átépülését és javítja a túlélést sóérzékeny Dahl patkányokban. PLoS ONE 2011, 6, e21853. [CrossRef] [PubMed]
25. Wang, Y.; Mu, JJ; Liu, FQ; Ren, KY; Xiao, HY; Yang, Z.; Yuan, ZY A só által kiváltott hám-mezenchimális átmenet Dahlsóra érzékeny patkányokban az emelkedett vérnyomástól függ. Braz. J. Med. Biol. Res. Rev. Bras. Pesquisa Med. E Biol. 2014, 47, 223–230.[CrossRef]
26. Holmes, SW; Sugden, D. Proceedings: The effect of melatonin on pinealectomia induced hypertension in the patkány. Br. J. Pharm. 1976, 56, 360P–361P.
27. Zanoboni, A.; Zanoboni-Muciaccia, W. Experimental hypertonia pinealectomized patkányokban. Life Sci. 1967, 6, 2327–2331. [CrossRef]
28. Zanoboni, A.; Forni, A.; Zanoboni-Muciaccia, W.; Zanussi, C. Pinealectomia hatása az artériás vérnyomásra és a táplálék- és vízbevitelre patkányban. J. Endocrinol. Investig. 1978, 1, 125–130. [CrossRef] [PubMed]
29. Pechánová, O.; Zicha, J.; Paulis, L.; Zenebe, W.; Dobesová, Z.; Kojsová, S.; Jendeková, L.; Sládková, M.; Dovinová, I.; Simko, F. et al. Az N-acetilcisztein és a melatonin hatása spontán hipertóniás felnőtt patkányokban megállapított magas vérnyomásban. Eur. J. Pharmcol. 2007, 561, 129–136. [CrossRef] [PubMed]
30. Leibowitz, A.; Peleg, E.; Sharabi, Y.; Shabtai, Z.; Shamiss, A.; Grossman, E. A szerepemelatoninmetabolikus szindrómában szenvedő patkányok magas vérnyomásának patogenezisében. Am. J. Hypertens 2008, 21. [CrossRef] [PubMed]
31. De Miguel, C.; Das, S.; Lund, H.; Mattson, DL A T limfociták közvetítik a magas vérnyomást ésveseDahl-sóra érzékenyek károsodása. Am. J. Physiol. Regul. Egész szám. Összeg. Physiol. 2010, 298, R1136–R1142. [CrossRef] [PubMed]
32. Evans, LC; Petrova, G.; Kurth, T.; Yang, C.; Bukowy, JD; Mattson, DL; Cowley, AW A megnövekedett perfúziós nyomás előidézi a vese T-sejt-infiltrációját a Dahl-sóra érzékeny patkányban. Hypertonia 2017, 70, 543–551. [CrossRef]
33. Abais-Battad, JM; Alsheikh, AJ; Pan, X.; Fehrenbach, DJ; Dasinger, JH; Lund, H.; Roberts, ML; Kriegel, AJ; Cowley, AWJ;Kidambi, S.; et al. Az étrend hatása a Dahl-sóra érzékeny magas vérnyomásra, a vesekárosodásra és a T-limfocita-transzkriptomra. Hypertens 2019, 74, 854–863. [CrossRef] [PubMed]
34. Fehrenbach, DJ; Dasinger, JH; Lund, H.; Zmaj, J.; Mattson, DL A lépsejtek átvitele súlyosbítja a sóérzékeny hipertóniás betegeket. Exp. Physiol. 2020, 105, 864–875. [CrossRef] [PubMed]
35. Ren, W.; Liu, G.; Chen, S.; Yin, J.; Wang, J.; Tan, B.; Wu, G.; Bazer, FW; Peng, Y.; Li, T.; et al. Melatonin jelátvitel T-sejtekben: Funkciók és alkalmazások. J. Pineal Res. 2017, 62. [CrossRef]
36. Álvarez-Sánchez, N.; Cruz-Chamorro, I.; López-González, A.; Utrilla, JC; Fernández-Santos, JM; Martínez-López, A.; Lardone, PJ; Guerrero, JM; Carrillo-Vico, A. A melatonin a T effektor/regulációs egyensúly megváltoztatásával kontrollálja a kísérleti autoimmun encephalomyelitist. Brain Behav. Immun. 2015, 50, 101–114. [CrossRef]
37. Chen, S.-J.; Huang, S.-H.; Chen, J.-W.; Wang, K.-C.; Yang, Y.-R.; Liu, P.-F.; Lin, G.-J.; Sytwu, H.-K.Melatoninfokozza az interleukin 10 expresszióját és elnyomja a kemotaxist, hogy gátolja a gyulladást in situ és csökkentse a kísérleti autoimmunencephalomyelitis súlyosságát. Int. Immunopharmacol. 2016, 31, 169–177. [CrossRef] [PubMed]
38. Griffith, JW; Sokol, CL; Luster, Kr. uKemokinekés kemokin receptorok: a sejtek pozicionálása a gazdaszervezet védelméhez és immunitásához.Annu. Rev. Immunol. 2014, 32, 659–702. [CrossRef] [PubMed]
39. Alsheikh, AJ; Dasinger, JH; Abais-Battad, JM; Fehrenbach, DJ; Yang, C.; Cowley, AWJ; Mattson, DL A CCL2 közvetíti a korai vese leukocita infiltrációt sóérzékeny hipertónia során. Am. J. Physiol. Ren. Physiol. 2020, 318, F982–F993. [CrossRef][PubMed]
40. Liu, L.; Callahan, MK; Huang, D.; Ransohoff, RM kemokin receptor CXCR3: Váratlan rejtély. Curr. Top. Dev. Biol.2005, 68, 149–181. [CrossRef] [PubMed]
41. Vőlegény, JR; Luster, AD CXCR3 ligandumok: redundáns, kollaboratív és antagonista funkciók. Immunol. Cell Biol. 2011, 89,207–215. [CrossRef] [PubMed]
42. Van Raemdonck, K.; Van den Steen, PE; Liekens, S.; Van Damme, J.; Struyf, S. CXCR3 ligandumok betegségben és terápiában. CytokinGrowth Factor Rev. 2015, 26, 311–327. [CrossRef] [PubMed]
43. Youn, J.-C.; Yu, HT; Lim, BJ; Koh, MJ; Lee, J.; Chang, D.-Y.; Choi, YS; Lee, S.-H.; Kang, S.-M.; Jang, Y.; et al. Immunoeszcens CD8 plusz T-sejtek és 3-as típusú CXC kemokin receptorkemokineknőnek humán hipertóniában. Hypertens 2013, 62, 126–133.[CrossRef] [PubMed]
44. Stumpf, C.; Auer, C.; Yilmaz, A.; Lewczuk, P.; Klinghammer, L.; Schneider, M.; Daniel, WG; Schmieder, RE; Fokhagyma, CD A Th1 kemoattraktáns interferon-gamma-indukálható protein (IP) 10 szérumszintje megemelkedett esszenciális hipertóniában szenvedő betegeknél. Hypertens Res. 2011, 34, 484–488. [CrossRef] [PubMed]
45. Rudemiller, NP; Lund, H.; Priestley, JRC; Endres, BT; Prokop, JW; Jacob, HJ; Geurts, AM; Cohen, EP; Mattson, DL Az SH2B3 mutációja (LNK), egy genomszintű asszociációs vizsgálat jelöltje a hipertóniára, gyengíti a Dahl-sóra érzékeny magas vérnyomást a gyulladásos moduláció révén. Hypertens 2015, 65, 1111–1117. [CrossRef] [PubMed]
46. Wade, B.; Petrova, G.; Mattson, DL Immunfaktorok szerepe angiotenzin II által kiváltott magas vérnyomásban és vesekárosodásban Dahlsalt-érzékeny patkányokban. Am. J. Physiol. Regul. Egész szám. Összeg. Physiol. 2018, 314, R323–R333. [CrossRef] [PubMed]
