2. rész: A hippocampális CREB-pCREB-miRNS MEF2 tengely aktiválása, amely modulálja a térbeli tanulási és memóriaképesség egyéni változásait
Mar 18, 2022
Kapcsolatba lépni:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791

A Cistanche javíthatja a memóriát
A fenti eredmények alapján megvizsgáltuk, hogy a hippokampusz miR-466f-3p expressziója nem szabályozott-e egerekben a térbeli tanulás során ésmemóriaképződése az idegsejtek morfológiáját is befolyásolta in vivo. Szignifikánsan azt találtuk, hogy a GLN egerek hippocampalis neuronjainak átlagos gerincsűrűsége magasabb volt, mint a PLN egereké, amint azt a piramis Golgi-impregnálása kimutatta.
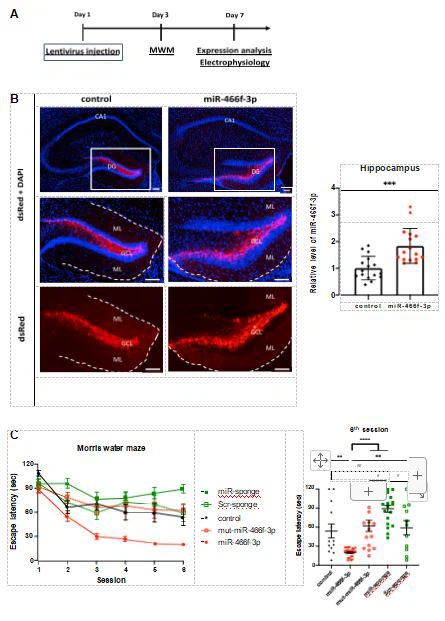
3. ábra: A hippokampusz miR-466f-3p expressziós szintjének változásának hatása az egér MWM teljesítményére
(A) Az MWM feladat kísérleti idővonala, az expressziós elemzés vagy az egér agyának elektrofiziológiai mérése lentivírus injekció után.
(B) Bal oldali panelek: a dsRed expressziója egér hippocampusban. Reprezentatív kis és nagy nagyítású IF-képek rekombináns lentivírusokkal fertőzött egerek hippokampuszáról, amelyek kontrollként csak a dsRed-t (a kép bal oldali oszlopa) vagy a miR-466f-3p plusz dsRed-et (jobbra) fejezik ki. képek oszlopa). A felső két kép bekeretezett területei kinagyítva és lent láthatók. Mérlegrudak, 100 mm. A szaggatott vonalak a DG határait jelzik. A sejtmagokat DAPI-val festették meg. GCL, szemcse sejtréteg; ML, molekuláris réteg. Jobb oldali hisztogram, a miR-466f-3p relatív expressziós szintjei kontrollal vagy miR-466f-3p-t expresszáló lentivírussal fertőzött egér hippocampusban, RT-qPCR-rel meghatározva ( n=16 csoportonként).
(C) Különböző rekombináns lentivírusokkal fertőzött egerek MWM teljesítménye, öt különböző, dsRed-only, miR{1}}f-3p, mut-miR-466f{ plazmiddal csomagolva. {5}}p, illetve miR/SCR-szivacsok a hippokampuszukba (n=13, 26, 16, 19 és 11 csoportonként). Bal oldali panel: menekülési késleltetés a képzés során. Jobb oldali panel: egyéni menekülési késleltetés a 6. munkamenetben.
A (B)-ben látható adatok átlag ± SD, a (C)-ben mutatott adatok pedig átlag ± SEM. A statisztikai szignifikanciát páratlan t-teszttel (B), kétirányú ANOVA-val Bonferroni post hoc összehasonlítással (C, bal oldali panel), vagy egy-ANOVA-val Tukey post hoc teszttel (C, jobb oldali panel) értékeltük. Statisztikai különbségek: #p < 0.05,="" **/##p="">< 0,01="" és="" ****p="">< 0,0001;="" *mir-466f-3p="" másokkal="" szemben;="" #mir-szivacs="" kontra="">
neuronok a GLN és PLN egér hippokampuszában (S3 ábra). Ezek az eredmények azt mutatják, hogy a hippokampusz miR-466f-3p felszabályozása elősegíti a neuritok kinövését és a dendritgerinc képződését, ami hasonló a GLN egerek hippokampuszában megfigyelt gerincsűrűség indukciójához a PLN egerekhez képest.
A miR-466f-3p pozitívan modulálja az egér térbeli tanulását ésmemóriateljesítmény, valamint szinaptikus plaszticitás
Annak megvizsgálása, hogy a miR{0}}f-3p pozitívan szabályozza-e az egér térbeli tanulását ésmemóriarekombináns lentivírus fertőzési megközelítést alkalmaztunk a miRNS túlzott expressziójára az egér hippokampuszában. Az egereket 7 nappal a lentivírus-injekció után elemeztük (3A. ábra). A miR-466f-3p csípő-expressziós szintjének reprezentatív képei valóban magasabbak voltak a miR-466f-3p túlzott expressziós csoportban a kontrollcsoporthoz képest (jobb hisztogram a 3B. ábrán). Azt találtuk, hogy az MWM-feladatnak alávetett, hippocampális miR-466f- 3p-túlexpressziójú egerek menekülési késleltetése 88 ± 5 s az 1. munkamenetben és 19 ± 1 s a 6. munkamenetben (piros pontvonal, 3C. ábra), amelyek jobbak voltak, mint a vektor kontroll egerek (fekete vonal) vagy mutáns kontroll egerek (piros körvonal), és hasonlóak az 1A. ábrán leírt GLN egerek menekülési látenciáihoz. Ezzel párhuzamosan megvizsgáltuk a miR-466f-3p funkcióvesztés hatását a térbeli tanulásra ésmemóriaa miR-466f-3p gátlásával miR-szivaccsal. Nevezetesen, azon egerek MWM-teljesítménye, amelyekben a hippokampusz miR-466f-3p-t befogta a miR-szivacs, hasonló volt a PLN-egerekéhez, azaz még azáltal sem tanulták meg, hogy megtalálják a platformot. az utolsó munkamenet (folytonos zöld négyzet vonal,


3C. ábra). Továbbá úgy tűnt, hogy a lentivírussal injekciózott egerek nem zavarták meg a homeosztatikus plaszticitást, mivel az egyes csoportok néhány egere megtanulta, vagy legalábbis tanulási folyamatban volt az utolsó ülés során (3C. ábra, jobb oldali hisztogram).
Tekintettel arra, hogy a miR{0}}f-3p túlzott expressziója az egér hippocampusában javította a tanulást ésmemóriaA miR-466f-3p különböző szintjét kifejező tenyésztett hippocampalis neuronok összehasonlító elektrofiziológiáját elemeztük. A miR-466f-3p-t vagy a mut-miR-466f-3p-t, a miR-szivacsot vagy a kontrollt túlzottan kifejező DIV14 hippocampalis neuronokból származó miniatűr gerjesztő posztszinaptikus áram (mEPSC) teljes sejtes patch bilincsekkel rögzítettük. Míg a négy mintakészlet között nem volt szignifikáns különbség a mEPSC amplitúdójában, a Tau emelkedésében vagy a bomlási Tauban, a miR-466f-3p-t túlexpresszáló neuronok mEPSC gyakorisága szignifikánsan magasabb volt a más csoportok (4A. ábra), ami azt jelzi, hogy a posztszinaptikus glutaminerg receptorok erősebben aktiválódtak a miR-466f- 3p túlzott expressziójára.

Ezután mértük a hosszú távú potencírozást (LTP), hogy közvetlenül meghatározzuk a miR-466f-3p szerepét a szinaptikus plaszticitásban in vivo. Az egerek hippokampuszába rekombináns lentivírussal injektáltuk a 3. ábrán leírtak szerint, majd a Schaffer kollaterális útvonal tetanikus stimulációjával (három sorozatú nagyfrekvenciás stimuláció [3xHFS]) LTP-hippokampuszszeleteket indukáltunk. Azt találtuk, hogy protokollunk minden csoportban LTP-t indukált, amint azt a mezei gerjesztő posztszinaptikus potenciálok (fEPSP) tartós növekedése bizonyítja a cornu ammonis 1 (CA1) régióban (4B. ábra, bal oldali panel). Az LTP erősebb volt a miR-466f-3p-t túlexpresszáló szeletekben (az alapvonal 188%-a ± 2%-a 40-50 perccel a stimuláció után, átlag ± SEM) a mutánshoz képest (169% ± 1%). a kiindulási értéktől), az SCR-szivacs (az alapvonal 173 százaléka ± 3 százaléka) és a kontrollvírussal fertőzött szeletek (az alapvonal 159 százaléka ± 2 százaléka), mint miR-466f-3p gátlás A miR-szivacs csökkentette az LTP-t (az alapvonal 128%-a ± 1%-a) a kontrollokhoz képest (4B. ábra, jobb oldali panel). A GLN és a PLN csoport LTP-jét is megmértük edzés után. A vonatkozó adatok azt is feltárták, hogy a GLN és PLN csoportok között jelentős különbségek vannak a fEPSP meredekségében a CA1 régióban (4C. ábra). Így a miR-466f-3p magasabb szintje fokozza az LTP-t és a szinaptikus plaszticitást, ami viszont elősegítheti a tanulást és amemóriaaz egerek képessége. A 2., 3. és 4. ábrán bemutatott adatok együttesen azt mutatják, hogy a miR-466f-3p kritikus pozitív szerepet játszik a térbeli tanulásban ésmemóriaképződés, valószínűleg a gerincképződés, az LTP és a szinaptikus plaszticitás erősítése révén.
A Mef2a mRNS a miR-466f-3p szabályozó célpontja
Bioinformatikai elemzést végeztünk, hogy azonosítsuk azokat a potenciális cél-mRNS-eket, amelyeket a miR-466f-3p 30 UTR-jükhöz való kötődése szabályoz. Az általunk azonosított jelöltek között volt a MEF2A-t kódoló Mef2a mRNS. Érdekes módon korábban azt találták, hogy a MEF2A expressziója csökkent az MWM edzés után, és ennek a faktornak a túlzott expressziója negatív hatással volt az egerek teljesítményére (Cole és mtsai, 2012). Ezért luciferáz riporter vizsgálatot használtunk annak megvizsgálására, hogy a miR-466f-3p szabályozza-e a Mef2a mRNS transzlációját a 30 UTR-hez való kötődés révén. Vad típusú vagy mutáns Mef2a 30 UTR szekvenciákat inszertáltunk egy SV40-promoter által vezérelt luciferáz cDNS-től (Luc) lefelé, ami a psiCHECK2-MEF2A 30 UTR vagy psiCHECK{19}} riporterplazmidot eredményezte. mut-MEF2A 30 UTR (5A. ábra). Amint az 5B. ábra bal oldali hisztogramján látható, a miR-466f-3p együttes expressziója gyengítette a Mef2a 30 UTR által irányított luciferáz expresszióját. Ez a hatás a miR-466f-3p és a Mef2a 30 UTR közötti kölcsönhatástól függ, mivel a miR-466f-3p előre jelzett kötőhelyének mutációja a Mef2a 30 UTR (50-UGU-GUAU-30) vagy a miR-466f-3p (50-AUACACA-30) magterülete a Mef2a 30 UTR felismerése megszüntette a miR-466f-3p luciferáz aktivitásra gyakorolt gátló hatását (5B. ábra, középső hisztogram). Ezenkívül a miR-szivacs koexpressziója, de nem a CR-szivacs, szintén megszüntette a miR-466f-3p luciferázaktivitásra gyakorolt elnyomó hatását (5B. ábra, jobb oldali hisztogram). Nevezetesen, sem a miR-466f-3p túlzott expressziója, sem a miR-szivacs nem volt hatással a Mef2a mRNS szintjére az elsődleges hippocampális neuronokban (5C. ábra), de csökkentették vagy növelték a MEF2A fehérje szintje (5D. ábra). Azt is megállapítottuk, hogy a miR-466f-3p, illetve a miR-szivacs túlzott expressziója csökkentette vagy felfelé szabályozta az aktivitással szabályozott citoszkeletális asszociált fehérje (Arc) mRNS szintjét az elsődleges hippocampális neuronokban (5C. ábra). , amely egy ismert downstream célpont volt, amelyet a MEF2A pozitívan szabályoz (Flavell et al., 2006)

Fluoreszcencia in situ hibridizációt (FISH) is végeztünk a miR-466f-3p kimutatására, és kombináltuk a MEF2A IF jelölésével a DIV14 elsődleges hippocampalis neuronokban forskolin kezelés nélkül vagy azzal együtt. A forskolinról ismert, hogy kémiai LTP-t indukál és aktiválja az adenilil-ciklázt, ezáltal megemeli az intracelluláris cAMP-szintet. Megfigyeltük a MEF2A nukleáris kolokalizációját miR-466f- 3p-vel, amint azt az 5E. ábra reprezentatív képei mutatják. A forskolin stimuláció után azonban a miR-466f-3p jel mind a szómában, mind a dendritekben megnőtt, míg a MEF2A jel a


A sejtmag csökkent, amint azt az egyes idegsejtek MEF2A és Fast Red jeleinek intenzitásának kölcsönös változásai mutatják (5E. ábra). Összefoglalva, az 5A–5E. ábrák adatai azt jelzik, hogy a miR-466f-3p negatívan szabályozza a MEF2A fehérje expresszióját azáltal, hogy kötődik a Mef2a mRNS 30 UTR-éhez, és ennek következtében elnyomja annak transzlációját.
A fent leírt eredményekkel összhangban azt találtuk, hogy a MEF2A fehérje hippocampális szintje lecsökkent GLN egerekben az MWM edzés után, de nem a PLN egerekben (5F ábra). Ezenkívül a MEF2A relatív szintje az egyes GLN egerekben (pontok) és PLN egerekben (négyzetek) fordítottan korrelált a miR-466f-3p (R=0.60, 5G ábra). Így a térbeli tanulás heterogén mintái ésmemóriaA képességet a hippocampalis miR- 466f-3p sztochasztikus növekedése modulálja az egyes egerekben, és ennek következtében a MEF2A csökkenése a neuronális aktivitás stimulálásakor.
A hippocampalis CREB sztochasztikus aktiválása és a miR{0}} klaszter ebből következő transzkripciós upregulációja az MWM edzés során
Megvizsgáltuk azokat a mechanizmusokat, amelyek által az egér hippokampuszában lévő R-466f-3p sztochasztikusan felszabályozható az MWM feladat által. Három miRNS-prekurzor kódolja a miR-466f-3p-t, amelyek mindegyike a rágcsáló-specifikus miR-466-669 klaszterhez tartozik, amely gazdagénjének, az mSfmbt2-nek a 10. intronjában található (Inoue et al. ., 2017) (6A. ábra). Érdekes módon a miR-466f-3p-vel ellentétben nem volt szignifikáns különbség az mSfmbt2 expressziós szintjei között a GLN és PLN csoportok között (6B ábra), ami arra utal, hogy a miR-466-669 klaszter egy külön átiratot kódolhat. ahelyett, hogy része lenne az mSfmbt2 elsődleges átiratának. Ennek megfelelően több primer-készletet terveztünk a miR-466-669 klaszter feltételezett elsődleges transzkriptumának azonosítására RT-qPCR segítségével. Ahogy a 6A. ábrán látható, egy hosszú PCR-fragmens (plusz 282-2381), valamint egy sor átfedő qPCR-sáv, nevezetesen A (plusz 282-115), B (131-406), C (388-686), D ( 662 - 1 028), E ( 1 004 - 1 299), F ( 1 242 - 1 629), G ( 1 605 - 2 029) és H ( 2 005 - 2 381) az egér hippokampuszában kimutatható, de nem, 3. rész 06 - 2. ) (az adatok nem láthatók). Ezek az adatok alátámasztják, hogy a miR{51}} klaszter egy hosszú transzkriptumot kódolt, közel körülbelül 2388 bp-ra az első miRNS-prekurzortól (azaz a pre-mir-466m, plusz 1-gyel jelölve a 6A. ábrán). Figyelemre méltó, hogy hasonlóan ahhoz, amit a miR-466f-3p esetében tapasztaltunk, ennek a transzkriptumnak az átlagos szintje a GLN egerek hippokampuszában magasabb volt, mint a PLN egereknél (6C. ábra). Így a fokozott tanulás ésmemóriaA GLN egerek képessége a miR-466-669 klaszter transzkripciós aktiválásának köszönhető.
A nukleáris CREB aktiválása foszforilációval az MWM feladatok során vagy a tanulás más formái során kritikus lépés a rövid távú hosszú távúvá alakításában.memória(Lisman et al., 2018; Rogerson et al., 2014). Ezért megvizsgáltuk, hogy az MWM-feladaton átesett egerek miR-466f-3p változó szintjei összefüggésben állnak-e a CREB aktiválási állapotával. Ennek az ötletnek a feltárásához először megvizsgáltuk a hippocampalis CREB foszforilációs szintjét egyes egerekben. Amint a 6D. ábrán látható, a CREB aktiválása (az S{6}} aminosavnál végzett foszforiláció révén) fokozódott GLN egerekben a PLN és HC egerekhez képest. Azt is megerősítettük, hogy a miR-466f-3p valóban együtt expresszálódott a pCREB-vel neuronokban, miRNS ISH-val kombinálva a pCREB és a MAP2 IF-festésével az elsődleges hippocampális neuronokban (S2A ábra). Ezenkívül a miR- 466-669 klaszter elsődleges transzkriptumszintjei pozitívan korreláltak a pCREB-vel GLN egerekben (R=0.52), míg a PLN egerekben negatívan korrelált a pCREB-vel (R=0). .71) (6E. ábra). Ellenőriztük, hogy van-e összefüggés egy másik aktív faktor, a foszfo-extracelluláris szignál által szabályozott kináz (pERK) szintjei és a miR-466-669 klaszter elsődleges transzkriptumszintjei között. Azt találtuk, hogy mindkét típusú MWM-vel edzett egerek pozitív korrelációt mutattak a miR-466-669 klaszter jel és a pERK között (R=0.59 és 0.48; S4A ábra), és nem volt különbség a pERK/ értékben. tERK kifejezés a két csoport között (S4B ábra). A CREB aktiválásának a miR-466-669klaszter transzkripciós felszabályozására gyakorolt hatásának további tisztázása érdekében, következésképpen


miR-466f-3p, specifikus CREBinhibitorként használtunk,666- 15 (Xie et al., 2015), a DIV14 elsődleges hippocampális neuronok forskolin kezelésével kombinálva. A forskolinról ismert, hogy aktiválja a CREB foszforilációt (Malhotra et al., 2015). Azt találtuk, hogy az elsődleges hippocampális neuronok 666-15-el történő előkezelése blokkolta a forskolin által kiváltott CREB aktivációt (6F ábra), és csökkentette a miR-466f-3p és miR-466-669 klaszter szintjét. átirat (6G és 6H ábra). Ezzel párhuzamosan az ismert pCREB-célgének, a nurr1 és homer1a (Bridi és mtsai, 2017; Jensen és mtsai, 2017) mRNS szintje is csökkent a 666-15 kezelés hatására (6H. ábra). Összességében a 6. ábra azt mutatja, hogy a CREB sztochasztikus aktiválása az MWM-feladaton átesett beltenyésztett egerek egy alpopulációjában a miR-466-669 klaszter transzkripcióját, következésképpen a miR-466f{{{23 indukcióját idézi elő. }}p, ezáltal fokozva a térbeli tanulásukat ésmemóriaképessége, hogy jobban teljesítsen a feladatban.

VITA
Feltártuk a miRNS-ek lehetséges szerepét a térbeli tanulás változó képességének modulálásában ésmemóriabeltenyésztett C57BL/6J egerek között. Azt javasoljuk, hogy a CREB sztochasztikus aktiválása és ennek következtében a hippocampalis miR-466f-3p felszabályozása hozzájárul a nagyobb térbeli tanuláshoz ésmemóriatesztegereink egy alcsoportjának képessége, valószínűleg a miR-466f-3p-nek köszönhető, amely közvetíti a Mef2a mRNS-t kódoló transzlációs gátlását.memórianegatív szabályozó MEF2A. Eredményeink egy olyan forgatókönyvet kínálnak, amely bemutatja egy specifikus miRNS funkcionális és evolúciós szerepét a megismerés szabályozásában a CREB-pCREB-miR-466f-3p-MEF2A tengely környezeti ingerek általi sztochasztikus indukcióján keresztül.
Az MWM feladatot széles körben alkalmazták a térbeli tanulás változó képességének vizsgálatára ésmemóriarágcsálóknak. Normál körülmények között a rágcsálók disztális jelzéseket használnak a tájékozódáshoz, lehetővé téve számukra, hogy megtanulják és megjegyezzék a rejtett platform helyét a feladatban. Vizsgálati beltenyésztett C57BL/6J egereink többsége (62 százalék) a szökési késleltetés normális mintázatát mutatta, és 30 másodpercen belül megtalálta a platformot a 3.-6. munkamenetben (1A. ábra, GLN). Ezzel szemben az egerek egy csoportja (38 százalék) még a 6. munkamenetig (PLN) sem tanulta meg a feladatot. Nevezetesen, az egereket két másik felismerési tesztnek is alávettük. Az első az újszerű objektumfelismerési (NOR) teszt volt, amely egyetlen kísérlet, amely a veleszületett feltáráson alapul, megerősítés vagy stressz nélkül, hogy motiválja a viselkedést (Leger et al., 2013). A NOR és az MWM feladatok közötti korreláció az egérteljesítmény tekintetében gyenge (R {{1{{2{22}}}}}.13), ami hasonló a NOR teljesítmények és a hippokampusz expressziós szintjei közötti korrelációhoz. miR-466f-3p (R=0.01; az adatok nem láthatók). A NOR teszt szintén nem mutatott ki különbséget a megkülönböztetési indexben az MWM GLN és a PLN csoportok között (0,36 ± 0,25 versus 0,29 ± 0,18; S1B ábra). A másik térbeli tanulás ésmemóriaAz általunk alkalmazott -függő feladat a Barnes labirintus (BM), amely hasonló az MWM-hez. Ez azon a feltételezésen alapul, hogy az averzív környezetbe helyezett rágcsálóknak meg kell tanulniuk és emlékezniük kell a platform felszíne alatt található menekülődoboz helyére. Amint az S1C ábrán látható, azt találtuk, hogy az egerek teljesítménye a BM próbakísérletekben szintén pozitív korrelációt mutat a miR-466f-3p hippocampális expressziós szintjével. Így a CREB-pCREB-miR-466f-3p-MEF2A tengely indukciója a hippocampusban a tanulás során, ill.memóriakialakulása térbeli kontextusfüggő.
