3. rész: Természetes fenolok testreszabott funkcionalizálása a biológiai aktivitás javítása érdekében
Mar 28, 2022
További információért. kapcsolatba lépnitina.xiang@wecistanche.com
5. Lipid fenolok
Lipidfenolok(vagy fenolos lipidek, más néven fenolipidek) lipofil láncokkal helyettesített fenolok, amelyek amfifil tulajdonságokat adnak a molekulának. Fontos fenolos lipid a -tokoferol[330]; ez a vegyület azonban önmagában is megérdemli a felülvizsgálatot, ezért nem került bele.
A természetes lipid fenolok jelentőségét sokáig alábecsülték [331]. Azonban a kiválóantioxidáns, az antigenotoxikus és citosztatikus tulajdonságokat mára megállapították [332], valamint bioaktivitásukkal, amelyek befolyásolják az érintett biológiai utakat.Alzheimer kórpatogenezis 333]. A kesudióból (Anacardium occidentale) extrahált lipid fenolok gyulladásgátló és ízületi gyulladás elleni hatásáról is beszámoltak [334].
Egy ilyen vegyületosztály fontossága miatt az elmúlt évtizedekben számos szintetikus lipid fenolt javasoltak biológiai alkalmazásuk további kiterjesztésére.

További termékekért kattintson ide
5.1. Lipid fenolok biokatalizált szintézise
A lipázok a választott enzimek a módosított vagy szintetikus lipidek előállítására szolgáló átészterezési reakciók végrehajtására, funkcionális vagy gyógyszerészeti alkalmazásokkal [335, 336]. A katekolból és zsírsavakból nagyszámú észtert állítottak elő a katekol zsírsav etil-észterrel készült szuszpenziójának keverésére [337].
A félszintetikus lipid fenolokat fenolsavak lenmagolajjal [338,339], oleinnel [340], halmájolajjal [341] és krillolajjal [342] való átészterezésével állítottuk elő. A szerves oldószerekben vagy oldószermentes rendszerben végrehajtott reakciókat [343,344] a Candida Antarctica által izolált Novozym 435 katalizálta (33. ábra).

Újabban a hozamok javultak szuperkritikus szén-dioxiddal reakcióközegként [345]. Az elkészített lipid fenol keverékek antioxidáns aktivitását teszteltük. A kapott gyökfogó aktivitás a közepestől a jóig terjedt, de mindig alacsonyabb volt, mint a -tokoferolé. Ráadásul, mivel keverékekből nyertük, az eredményeket nem lehetett egyetlen vegyületnek tulajdonítani.
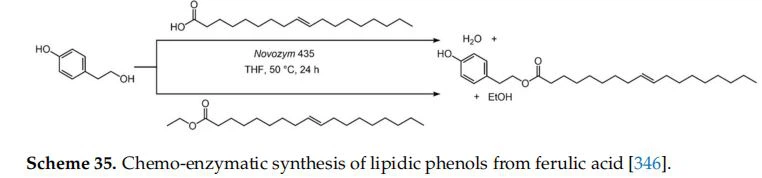
Ezzel szemben a változó lánchosszúságú zsírsavak tiszta fenolos lipidjeit ferulinsavval állítottuk elő [346]. A szintézis egy biokatalizált lépést tartalmazott (a Nosozyme által) (34. séma).
Azantioxidáns aktivitásA vizsgálat vegyes eredményeket hozott, mivel a gyökfogó vizsgálat nem mutatott javulást a ferulinsavhoz képest, míg a linolsav micelláris rendszerben történő autooxidációja némi javulást mutatott, ami a megnövekedett oldhatóságnak tulajdonítható.

Fenolsavat és zsírsavakat tartalmazó foszfatidilkolinok kemoenzimatikus szintéziséről számoltak be [347], az egyik aktív származékkal, a 1-(4-hidroxi-3, 5-dimetoxi) cinnamoil-2-acil-sn-glicerin-3-foszfokolin, amely kiváló antioxidáns aktivitást mutat.
Egy másik megközelítés volt a lipid fenolok fenolból és szabad zsírsavakból vagy a megfelelő észterekből történő előállítása, biokatalizátorként a Candida Antarctica immobilizált lipázzal [348]. A tirozol antioxidáns aktivitása megnövekedett acilezéskor, de nem találtunk összefüggést a zsíracilcsoportban található kettős kötések számával (35. ábra).
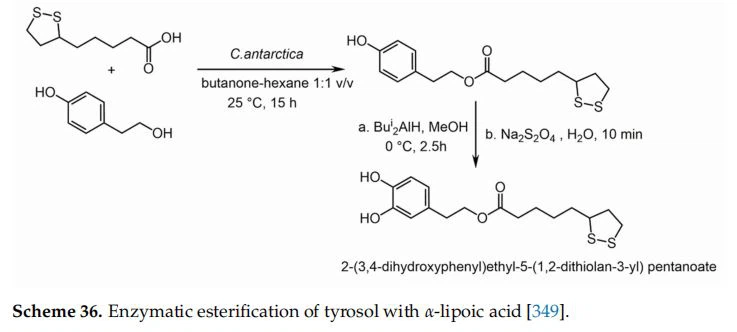
Egyes észtereket természetes fenolokból és -liponsavból szintetizáltak a Novozym 435 (a Candida Antarctica immobilizált lipáz B-je) által katalizált reakcióban butanon-hexán keverékben [349]. Az antioxidáns aktivitást nemcsak gyökfogó vizsgálattal határoztuk meg, hanem tonhal-halolaj emulzióban az oxidáció gátlásának mérésével is. A tirozolból és -liponsavból nyert 2-(3,4-dihidroxi-fenil)-etil-5-(1,2-ditiolán-3-il)-pentanoát észter. aromás hidroxilezéssel (36. séma) mindkét tesztben kiváló antioxidáns aktivitást mutatott, és a szerzők szerint prodrugként is használható, mert hidrolízise során nem mérgező, sőt egészséges vegyületek szabadulnak fel belőle.
Később kiderült, hogy az 2-S-lipoil-kávésav-metil-észter gátolja a humán melanomasejtek tirozinázát [350].
A célt, hogy egyetlen lipid fenolt állítsanak elő, elkerülve egy bonyolult keverék problémás szétválasztását, többlépéses stratégiával érték el, amely kémiai és enzimatikus katalízist is magában foglal. A Candida Antarctica (CAL-B) immobilizált lipázát szerves tápközegben alkalmaztuk [351] (37. séma).
![Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol](/Content/uploads/2022842169/20220328111325cc1b5fb0d7394a028caf7ce4b3cdd52d.png)
A jellemzést követően az előállított 1-[11-(feruliloxi)undekanoil)glicerint antimikrobiális, antioxidáns és citotoxikus vizsgálatoknak vetették alá. Az antimikrobiális aktivitás mérsékelt, az antioxidáns aktivitás kiváló, és bizonyos rákos sejtvonalak elleni aktivitás ígéretes volt, így a szerzők előre jelezték a lehetséges kozmetikai és orvosbiológiai alkalmazásokat.
Átészterezési reakciót végeztek Candida Antarctica lipáz B-vel, a 4-hidroxi-fenil-ecetsavat trioleinnel és halolajjal kezelve olyan szintetikus anyagokat kaptak, amelyek antioxidáns és antibakteriális hatással is rendelkeznek [352].
5.2. Lipid fenolok kémiai szintézise
A lipid fenolokat észterként állítottuk elő, vagy hosszú szénláncú karbonsavakkal képzett fenolokból vagy fenolsavakból. A szintetikus lipid fenolok válogatott példáit az 1. táblázat tartalmazza.

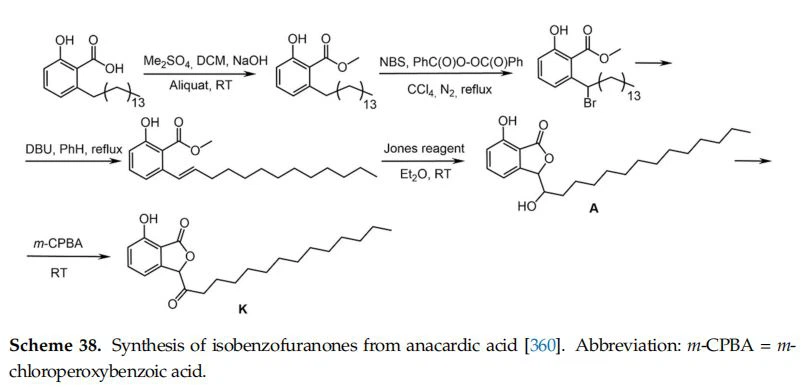
Az Anacardium occidentale friss és száraz kesudiójából származó anakardsavat izobenzofuranonokká alakították át, amint azt a 38. séma szemlélteti, alkohol(A) vagy keto(K) funkciós csoporttal a hosszú láncban [360].
Mind az A, mind a K izobenzofuranonok, valamint az aciklikus prekurzor mérsékelten vagy szignifikánsan aktívak voltak a különböző humán rákos sejtvonalakkal végzett citotoxicitási szűrésben.
Jó antioxidáns képességet figyeltek meg az olívaolaj stabilizálására a fenolos zsírsav-észterek családjával, amelyeket 3,4-dihidroxi-benzoil-alkoholból (protokatekuin-alkohol) vagy hidroxi-tiroszolból és zsírsavakból állítottak elő. A reakciót vízmentes THF-ben hajtottuk végre karbodiimid és DMAP [361] jelenlétében. Mind a húsz vegyületet potenciális antioxidánsként vizsgálták a finomított olívaolajban. Úgy tűnik, hogy a fenilgyűrűhöz kapcsolódó alkillánc hossza befolyásolja az aktivitást.
Miután kiderült, hogy a Merulius incarnates gombateremből izolált 5-alkil- és 5-alkil-rezorcinolok gátolják a meticillinrezisztens Staphylococcus aureust [362], jó szintetikus módszerre volt szükség, mert nem könnyen alkalmazhatók. rendelkezésre állnak, de fontosak az analitikai, metabolikus és bioaktivitási vizsgálatokhoz. A Wittig-reakción alapuló általános módszert dolgoztak ki [363] az aromás gyűrűbe történő alkillánc-bevezetés problémájának megoldására. A problémát úgy oldották meg, hogy a hosszú szénláncú alkanolokat, ha elérhetőek voltak, félig stabilizált benzil-foszfónium-ilidekkel vagy 3,5-dimetoxi-benzol-karbaldehiddel alkil-foszfónium-ilidekkel reagáltatták. Az eljárás során 5-alkil-rezorcinolokat szállítottak legfeljebb 25 szénatomos alkilláncokkal. A reakciót vízben vagy víz-DMSO elegyben, MW besugárzással, nyomás alatt vagy nyitott edényben hajtjuk végre. Minden útvonalra egy példa látható a 39. sémán.

Közepestől jóig terjedő in vitro antioxidáns aktivitást mutatott az 1,2-dibutanoil-oxi-2-(4-hidroxi-3-metoxifenil)etil-butanoát, a ferulinsavból nyert lipid fenol [354] .
2-Metil-5-[(2Z)-non-2-en-1-il]benzol-13-diol és 5-[(2Z)-non{ Az {10}}en-1-il]benzol-1,2,3-triol a természetes 5-[(2Z)-non{{18} szintetikus származékaiként készült }en-1-il]benzol-1,3-diol (klimakostol), a Climacostomum virens protozoonok védekező vegyi anyaga[355]. Az aromás gyűrű szerkezeti módosulásai (egy metil- és egy hidroxilcsoport) növelték a toxicitást.
Long-chain alkyl hydroxycinnamates were prepared from the corresponding monoesters of malonic acid and benzaldehyde derivatives by Knoevenagel condensation [364]. The observed antioxidant activity followed the order caffeic esters > sinapic esters >ferulsav-észterek.
A 12-hidroxi-9-oktadekánsavat (ricinoleinsavat) (Z)-metil-12-aminooktadeka-9-enoáttá alakították, majd fenolsavakkal reagáltatták, így a megfelelő amidok keletkeznek [356 ]. A vizsgált antioxidáns aktivitás azt mutatta, hogy a fenolos savak lipofil részekkel történő módosítása javítja antioxidáns és rákellenes tulajdonságaikat.
Érdemes jelezni a lipid fenolok fogalmilag eltérő típusát, nevezetesen a kávé és más fenolsavak fenil-szulfonil-furoxán származékait [357]. Az in vivo jó antioxidáns aktivitás mellett ezek a vegyületek antikoaguláns és értágító hatást is mutattak, ami az NO-felszabadító képességnek tulajdonítható.
Kávésavat vagy 3,4-dimetil-kávésavat almasavdal reagáltattak, majd 8-18 szénatomos lánchosszúságú zsírsav-monogliceridekkel kapcsolták össze [359]. A fenol- és zsírsavak kombinációja hat amfifil vegyületből álló sorozatot eredményezett, amelyek aktivitását tesztelték. A szerzők szerint nem mérgezőnek bizonyultak, és stabil olaj-a-vízben emulziókat adnak, amelyek alkalmasak élelmiszer-, gyógyszer- és kozmetikai iparra.

6. Polifenolok
Természetespolifenolokaz ehető növényekben található bioaktív molekulák számos és nagymértékben elterjedt csoportját alkotják, amelyek bioaktivitása a szív- és érrendszer védelmétől a rák megelőzéséig terjed [365-368].
A polifenolokat pirén vagy pirídium típusú benzo-kondenzált heteroaromás gyűrű jelenléte jellemzi. Általában félszisztematikus nómenklatúrával nevezik el őket, amely a szülő heterocikluson alapul. Így a fenil-szubsztituenst tartalmazó benzopirén-származékokat flavonoknak, míg a fenollal szubsztituált benzofenonokat flavonoknak nevezzük. Az alapvegyületek és fenil-származékaik szerkezetét a 9. ábra gyűjtötte össze.
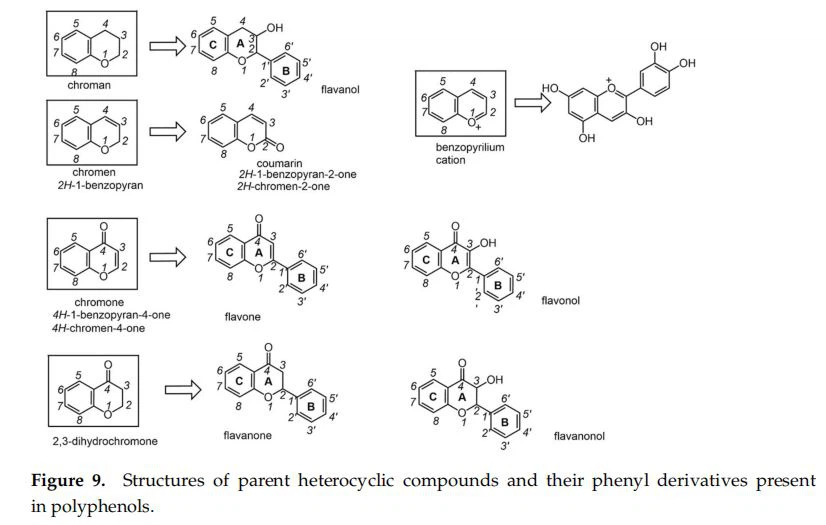
Természetes és félszintetikus erősen oxidált bioaktív anyagok szintézisepolifenolok2008-ban felülvizsgálták az előrelépéseket és a kihívásokat [369]. Alternatív megoldásként a hatékonyabb és fenntarthatóbb termelés származhat mikrobasejt-gyárakból, amint azt 2018-ban felülvizsgálták [370].
A természetes fenolok kémiai átalakulása hatékonyabb fajokhoz vezethet, ha megértjük a biológiai aktivitás alapjául szolgáló szerkezeti jellemzőket. Így a reprezentatív polifenolok kémiai módosításainak eredményeit a következőkben közöljük.
6.1. Fenolok a Chromanból
A katekin a flavanolok családjába tartozó polifenol, amely megtalálható a zöld teában. A 10. ábrán bemutatott származékokat racém katechinből (tetra-metoxi, pentaacetoxi és ciklikus) állítottuk elő[371]. A katechint és származékait vizsgáltuk a gyökértelepítő gombák elleni antimikrobiális aktivitásra, amely a kevésbé poláris vegyületekben, bár kisebb hatékonysággal, megmaradt.
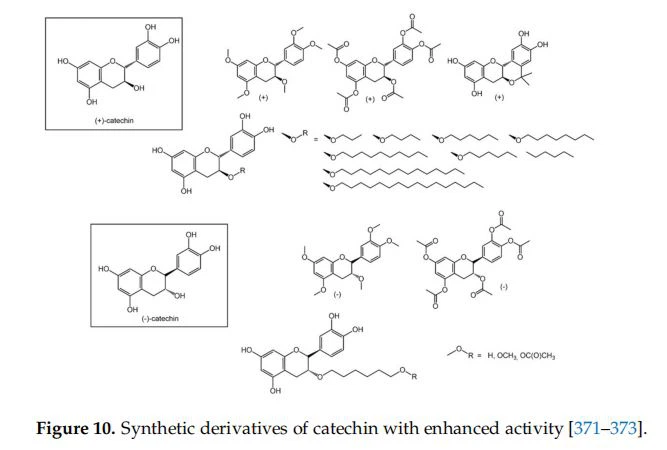
A galvinoxilgyökkel szemben vizsgált (plusz)-katekin antioxidatív gyökfogó képessége fokozódik a ninhidrinnel való reakció során [374].
A mikroorganizmusok növekvő rezisztenciájának problémájának megoldása érdekében a vizsgálatok a katechin szintetikus származékainak előállítására és tesztelésére irányultak. A 3-hidroxilcsoportok szisztematikus éterezése különböző hosszúságú lineáris alkilláncokkal vagy szubsztituált benzilcsoportokkal a katechin 3-O-alkil-analógjainak [372] könyvtárát eredményezte, amelyeket a gombaellenes hatás tesztelésére használtak. a szerkezet függvényében. A hosszabb láncú (C14-C16) vegyületek gyengébb aktivitást mutattak, mint a C8-C12 láncú vegyületek.
Ezen túlmenően a 3-ban az -OH funkcionalitás változtatásával tizenkét (-)-katekin származékot állítottak elő [373]. Csak három vegyület mutatott nagyobb antibakteriális és gombaellenes aktivitást, mint a standard gyógyszerek (neomicin és mikonazol). A molekuláris dokkolási vizsgálatok megegyeztek a kísérleti eredményekkel.
A brazilin és az oxidált brazilein analóg (11. ábra) a növényekben (Caesalpinia sappan L.) megtalálható kromán származékok, amelyek gyulladásgátló tulajdonságaikról ismertek. Új szintetikus származékokat készítettek daganatellenes hatásuk feltárására. A brazilok [375] szintézise 1,3-dihidroxi-benzolból (rezorcin) és 3-klór-propánsavból indult ki, a kulcsfontosságú köztitermék 7-hidroxi-4-kromanon képződésével. . A szintetizált brazilok (1l. ábra) gyulladáscsökkentő hatását tesztelték számos humán rákos sejtvonallal szemben, de csak néhány szintetikus származék mutatott némi javulást a helyettesítetlen brazileinhez képest.
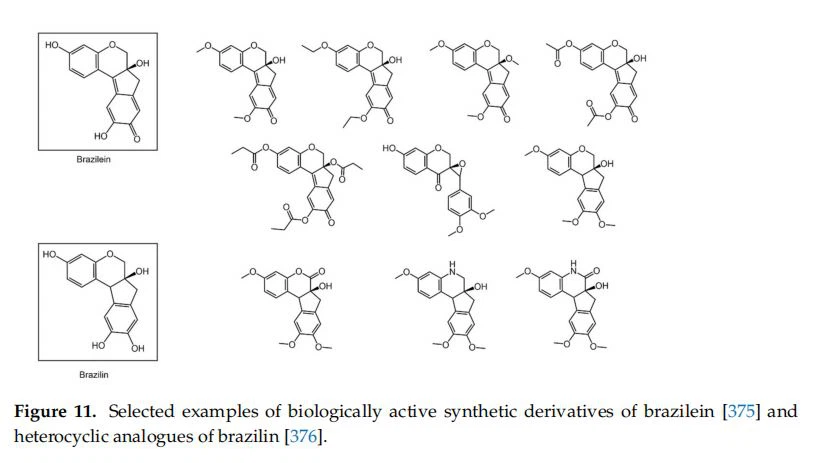
6.2. Fenolok a Chromentól
A kumarin (2H-chromen-2-one), a króm leggyakoribb származéka, és a helyettesített kumarinok a zöld növényekben találhatók, ahol eltérő hatást fejtenek ki [377].
Figyelembe véve a kumarin heterociklusos rendszerhez vezető reakciók sokoldalúságát [378], számos szubsztituált kumarint szintetizáltak, és ígéretes aktivitást találtak a kumarinnal fuzionált 14A-tiazepinekkel, amelyeket 4-hidroxi-kumarinokból (40. séma)[379] szintetizáltak.
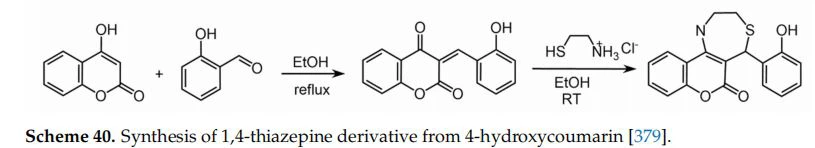
A 7-vagy 8- pozícióban hidroxilcsoporttal szubsztituált kumarinokat és benzokumarinokat állítottak elő, és számos biológiai aktivitásra in vitro tesztelték [380]. Általában hatékony szuperoxid-anion-megkötőket szállítottak, és gátolták az in vitro lipidperoxidációt; másrészt nem mutattak jelentős lipoxigenáz gátló aktivitást.
6.3. Fenolok a Chromonból
A kvercetin (3,3'4',5,7-pentahidroxiflavon) egy flavonol, amely nagymértékben jelen van növényekben, ételekben és italokban, gyakran a fiszetinnel (3,3'4',7-tetrahidroxiflavon) együtt. .
A kvercetin iránti érdeklődést rákellenes, gyulladáscsökkentő és antioxidáns szerepe váltotta ki. Különös jelentőséggel bír a vérnyomáscsökkentő hatás [381]. Számos szintetikus származékot készítettek azzal a céllal, hogy rákellenes jelölteket állítsanak elő, amelyek leküzdhetik a kvercetin problémákat: (i) alacsony vízoldhatóság, (ii) alacsony biológiai hozzáférhetőség és (ii) gyors lebomlás. A biológiai aktivitásra vonatkozó vizsgálatok nem voltak elegendőek e származékok tényleges hatékonyságának felmérésére, bár néhányuk ígéretesnek tűnt [382]. Másrészt a Cu(I)-vel való egyszerű komplexálás olyan Cu(kvercetin)(bipy) komplexet eredményezett, amely fokozott antioxidáns tulajdonságokkal rendelkezik a szabad kvercetinhez képest [383].
A kvercetin és származékai terápiás tulajdonságai iránti érdeklődés nem korlátozódik a citotoxicitásra, amint azt a 2010 és 2015 között bejelentett szabadalmak száma is mutatja [384]. A kiválasztott értelmes példákat a 2. táblázat gyűjti össze.

A legtöbb ilyen származék az összes hidroxilcsoportban átalakult, a C-3-hidroxilcsoport módosítása pedig a rákellenes aktivitás fokozódását eredményezte. Ezenkívül a bioaktivitást jelentősen növelte a nanotechnológia.
A vízben való szűkös oldhatóság problémájaflavonoidokA polifenolokkal foglalkoztak a hidrofil szubsztituenseket tartalmazó származékok, például a szulfát tekintetében [385].
Egy másik megközelítés a cukrok konjugátumainak elkészítése volt, flavonoidokkal az aglikonnal. Többek között glükózt, galaktózt és ramnózt használtak.
Az enzimatikus szintézis sikeres volt a természetes vegyületek módosításában, ami nemcsak jobban oldódó, hanem hatékonyabb fajokat is eredményezett gyógyászati [386] vagy kozmetikai [387] alkalmazásokban.
Érdekes, hogy a rutin (2-(3,4-dihidroxifenil)-5,7-dihidroxi-3-[ -L-ramnopiranozil-(1→6){ A {11}}D-glükopiranoziloxi]-4H-kromén-4-on) enzimes átészterezési reakcióval tovább alakult mono- és diacetát származékokká (41. séma), amelyek megőrizték antioxidáns tulajdonságait és így tovább hatékonyan képesek áthatolni az egér makrofágok sejtmembránján [388]. Ezenkívül az acetoxi-szubsztituált rutinek nem voltak toxikusak az emlőssejtekre, és az enzim újra felhasználható volt.

A cukorszubsztituált flavonoidok fontosságát a miricitrin (miricetin-3-O- -L-ramnopiranozid) szemlélteti, amelynek antioxidáns hatása védő hatást fejtett ki a DNS-károsodás ellen [389].
Új flavonoid állványt készítettek a szalicilát és trimetoxibenzol csoportok flavonoidokba való bejuttatására [390]. Valamennyi vegyület antiproliferatív aktivitását értékeltük három, közepestől jóig terjedő aktivitást mutató humán tumorsejttel szemben.
6.4. Fenolok 2,3-dihidrokromonból
A flavanonok, a növények széles spektrumú biológiai aktivitású másodlagos metabolitjai közül a csíkozás (5-hidroxi-7-metoxi-flavanon) keltett érdeklődést, mivel ez az ujjgyökér (Kaempferia pandurata) rizómájának fő összetevője. a délkelet-ázsiai konyhában használatos, számos farmakológiai hatásról ismert, amelyek közül az antimikrobiális ígéretes.
A pinostrobin allilálását és prenilezését MW besugárzással végeztük (Mitsunobu és metatézis reakciók, Claisen és Cope átrendeződések) (42. séma), így olyan vegyületeket kaptunk, amelyeket számos rákos sejtvonal ellen teszteltek [391]. A származékok reaktívabbak voltak, mint a pinostrobin, amit a szerzők a biológiai célpontokkal való jobb kölcsönhatásnak tulajdonítottak, az alkenil-szubsztituensek által biztosított megnövekedett lipofilitás miatt.

A pinostribint egyszerű SN2 körülmények között prenilezték (43. séma), így olyan termékek keverékét kapták, amelyek többsége elvesztette a flavanon szerkezetét. Elválasztották őket és tesztelték az antimikrobiális aktivitást [392], közepes hatást mutatva. Érdekes módon számos prenilált kumarint és kvercetint izoláltak a Broussonefia papyrifera gyökérkérgéből metabolitokként, amelyek bizonyos esetekben citotoxikus aktivitást mutattak [393].

Az asztilbin, a flavanol taxifolin cukorszármazéka, a hagyományos kínai orvoslásban általánosan használt gyógynövényekből nyerik ki. Lehetséges gyógyszerészeti felhasználásukhoz azonban az extrakcióból származó asztilbin nem elegendő. Az asztilbin taxifolinból történő előállításának hatékony eljárása a mikrobiális fermentáción alapult genetikailag módosított Escherichia coliban (44. séma) [394].

A naringenin (5,7-dihidroxi-flavanon) 4'-O-glükozid származékainak (5,7-dihidroxi-flavanon) előállítására kaszkádos biokatalitikus rendszert fejlesztettek ki, amely számos bioaktív hatású flavonoid szőlőben és narancsban található [395]. A módszer az uridin-difoszfát szacharózból történő regenerálásán és újrafelhasználásán alapul, valamint preparatív léptékű előállítást végez. Ugyanezzel a módszerrel kaptuk a kvercetin 7-OaL-ramnozidot.
Érdekes módon a myricitrin (miricetin-3-O- -L-ramnopiranozid)[389] és a naringenin, amely a Cynara cardunculus, egy erőteljes természetes gyomirtó kivonatában jelen van, fitotoxikus hatást fejtett ki a Trifolium incarnatum levelein, megnyitva a utat a természetes gyomirtókhoz, amely terület egyre fontosabb a gyomok általánosan használt szerekkel szembeni ellenálló képessége miatt[396].

7. Kurkumin és kurkuminoidok
kurkumin, [1,7-bisz(4-hidroxi-3-metoxifenil)-1,6-heptadién-3,5-dionel, a A kurkumából izolált sárga pigment (Curcuma longa Linn) egy többfunkciós vegyület, amely legalábbis az elmúlt húsz év irodalmát olvasva egyfajta csodaszernek tűnik a modern társadalom összes betegségére, beleértve a rákot és az Alzheimer-kórt is. A fenolos-OH csoportok biztosítják az antioxidáns tulajdonságokat, míg a ketoenol egyensúly miatti kiterjedt konjugáció (45. ábra) a fotodinamikus aktivitás alapja.

Számos közelmúltbeli áttekintés tárgyalja a kurkuminok és származékai biológiai aktivitásának [397-400] és lehetséges orvosi felhasználásának [70,292,401-404] szempontjait. A hatásmechanizmussal együtt olyan fontos szempontokat is megvitattak, mint az új bejuttatási módszerek és más vegyületekkel való szinergikus hatások [405]. Egyre nagyobb érdeklődés övezi a kurkumin alapú gyógyszereket a neurodegeneratív betegségek [406], különösen az Alzheimer-kór[407] és a rák [408] ellen.
Az új kurkumin származékok keresését (i) az anyag hozzáférhetőségének növelésének szükségessége, és (i) a vizes oldatban való oldhatóság javításának szükségessége motiválja.
Figyelemre méltó, hogy a kurkumint Cu(II)-vel kezelve egy Cu(kurkumin)(bipy) komplexet izoláltak, amely a szabad kurkuminhoz képest jobb antioxidáns és DNS-kötődés volt, miközben gombaellenes tulajdonságai alapján kevésbé toxikus [383]. . Azt is közölték, hogy a szonokémiai módszerrel előállított ezüst-kurkumin nanokonjugátumokat bőrsejtvonalakon és Escherichia coli elleni antibakteriális aktivitásra tesztelték. Az eredmények azt mutatták, hogy az ezüst nanorészecskéket a kurkumin biokompatibilissé tette, míg a kurkumint fotostabilabbá és antibakteriális hatásúbbá teszik [409].
A kurkumin származékokat a szerkezeti változásoknak megfelelően tárgyaljuk.
7.1. Kisebb szerkezeti változások
Kisebb szerkezeti változtatások megváltoztathatják a hatékonyságotkurkuminbioaktivitás. Például egy metilcsoport 2-es pozícióba vagy két metilcsoport, mint a 2-es, 7-dimetil-kurkumin bevitele, fokozott angiogenezis-ellenes aktivitást és a tumornövekedés elnyomását [410], valamint megnövekedett gyulladásgátló aktivitást [411] figyeltek meg. ] és az enzimatikus redukcióval szembeni stabilitás [412], a kurkumin tekintetében.
Az alapvegyület acetilezésével könnyen előállítható diacetilkurkumin kiváló antibakteriális aktivitást mutatott [413], és hatékony volt egerekben az ízületi gyulladás elleni aktivitásban (3. táblázat) [414].
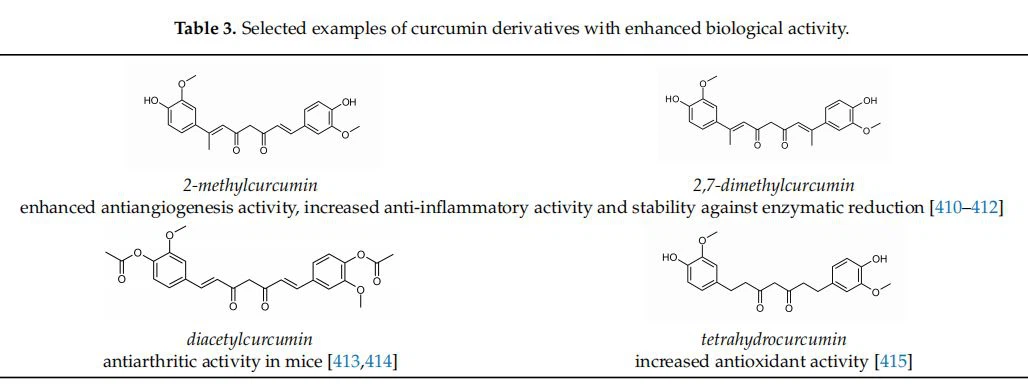


A kurkumin antioxidáns hatását a dimetoxi metabolitok és a hidrogénezett származékok antioxidáns hatásával hasonlították össze [415]. Az eredmények azt mutatták, hogy a telített származékok (tetrahidro-, hexahidro- és oktaéder-kumarinok) fokozott antioxidáns aktivitással rendelkeznek a kumarinhoz képest (3. táblázat).
A prenil szubsztituensek mindkét aromás gyűrűbe történő bevezetésével kapott származékot oxidatív stressz ellen tesztelték[416] (3. táblázat), amely azonos vagy jobb antioxidáns tulajdonságokat mutatott a kurkumin tekintetében.
Egy drasztikusabb szubsztitúciót hajtottak végre, elektronvonzó szubsztituenseket vittek be a benzolgyűrűkbe, vagy akár heterociklusokat is kondenzáltak (3. táblázat)[417].
7.2. Helyettesítők az UI-telített láncban
A legtöbb szintetikus származék a 4-es pozícióba bevitt szubsztituensekből származik, így befolyásolva a kurkumin tautomer egyensúlyát. A keto-enol egyensúlyhoz kapcsolódó fontos bioaktivitás az Alzheimer-kórban jelenlévő amiloid (A) aggregációval való kölcsönhatás. A szubsztituált kurkuminok keto-enol tautomer egyensúlyának kiterjedt vizsgálatát végezték el [432-434]. Nemrég arról számoltak be, hogy a 4,4-diszubsztituált kurkumin (12. ábra), ahol a ketoforma az egyetlen lehetséges, megköti a nem fibrillárisan oldódó A oligomereket, és a szerzők szerint" első generációssá válik. A oligomereket célzó vegyület"[435].
A fluorozott kurkumin-származékok jelentős gátlást mutattak a tioredoxinnal kölcsönhatásba lépő fehérje (TXNIP) működésében, amely számos betegséggel kapcsolatos [418].
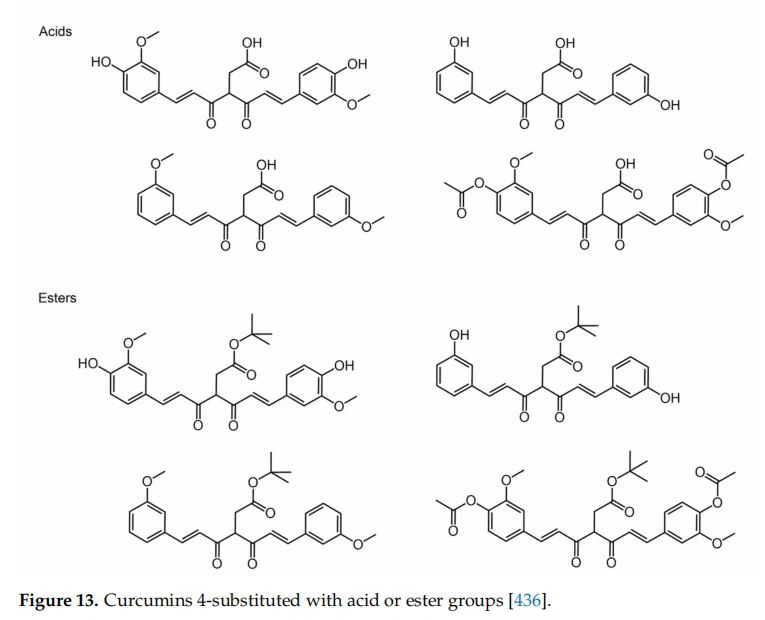
Számos kurkumin-származékot állítottak elő, amelyek a 4-es pozícióban sav- vagy észtercsoportokkal voltak szubsztituálva [436] (13. ábra). Meghatároztuk a savasságot, a lipofilitást és a kinetikai stabilitást, valamint a szabad gyökfogó aktivitást, hogy értékeljük a szerkezet és az aktivitás közötti kapcsolatot. Az észterszármazékok szelektivitást mutattak a vastagbél karcinóma sejtekkel szemben, valószínűleg a kurkuminnak köszönhetően magasabb lipofilitásuknak köszönhetően.
![The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers](/Content/uploads/2022842169/20220328112546d633ce9f0cd54ad68e1c33ed5c4758d7.png)
Egy másik megközelítés volt egy telítetlen csoport bejuttatása a 4-es pozícióba (3. táblázat), a Knovenagel reakciójával benzol-karbaldehiddel, 4-hidroxi-benzaldehiddel és 4-hidroxi-3-metoxi-benzaldehiddel (vanillin)419. ]. A kapott származékokat tesztelték P. falciparum elleni maláriaellenes aktivitásra, és a vanillin-származék meglehetősen erős volt.{8}}A 2-hidroxi-benzol-karbaldehidből [420] és 4-benzilidén-kurkuminokból előállított benzilidén-kurkuminokat antioxidánsként vizsgálták, és mindkettő hatásos volt a szürkehályog csillapításában tenyésztett patkánylencsékben.
7.3. A -dikarbonil-csoport módosítása
Tizennyolc új származék, amelyek továbbra is a kurkumin hepta-1,6-dien-3,5-dion szerkezetét mutatják, de az egyik karbonilcsoport beépült a cikloheptanon részbe. sokoldalú szintetikus stratégiával szintetizálták [421]. A szubsztituált tropinon egyik példáját a 3. táblázatban közöljük. A szerzők biztosak abban, hogy a tropángyűrűt tartalmazó dikarbonil-kurkuminok családja fontos aktivitással fog rendelkezni, mivel az egyszerű monokarbonil-tropanonok citotoxikusak voltak az emlőráksejtekkel szemben.
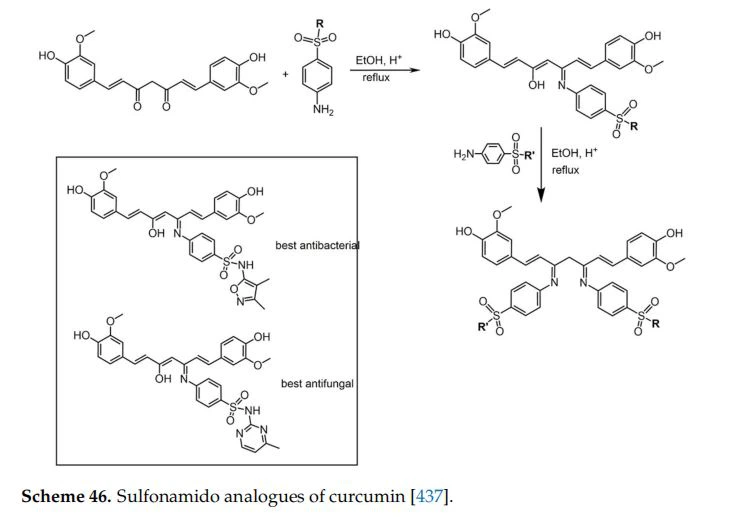
A kurkumin-származékok könyvtárát egy vagy két ekvivalens szulfonamiddal (a szulfa-gyógyszerek közül kiválasztott) reagáltatva kaptuk meg (46. séma)[437]. Az antibakteriális és gombaellenes hatásokat Gram-pozitív és Gram-negatív mikroorganizmusokkal szemben értékelték, jó eredménnyel.
3,4-A kurkumin dihidropirimidin-2(1H)-on és tionanalógjait (3. táblázat) jó hozammal állítottuk elő egyedényes, többkomponensű ciklokondenzációval MW besugárzás mellett [425]. Az antibakteriális és antioxidáns vizsgálatokat in vitro végezték, az eredményeket a szerzők az előbbi esetben "közepesnek", az utóbbi esetben "kiválónak" ítélték.
A kurkumin pirazolszármazékát készítették elő, hogy megpróbálják ugyanabba a molekulába beépíteni a kurkumin és az aszteroidaszerű vegyület (ciklohexil-biszfenol A) szerkezeti jellemzőit[422]. A vegyületről azt találták, hogy neuroprotektív a sejttenyésztési vizsgálatokban, intracelluláris és extracelluláris amiloid ellen is. Ezenkívül egy patkány tárgyfelismerési tesztben azt találták, hogy memóriajavító tulajdonságokkal rendelkezik [423].

7.4. A -dikarbonil-csoport részleges helyettesítése
A kurkumin -dikarbonil-csoportjának részleges helyettesítését hasznosnak ítélték a nem kielégítő stabilitás problémájának megoldására. A kurkumin monokarbonil-analógjainak sorozata, amelyet az alkalmasan szubsztituált benzaldehidből és egy cikloalkánból [438-440] szintetizáltak. A szubsztituált ciklopentanonok és ciklohexanonok stabilitása in vitro javult. A citotoxikus aktivitás a ciklohexanonok esetében is nagyobb volt, a szubsztituensek elektronhatásainak kiemelkedő jelentősége mellett (47. ábra).

Az aminokarbonil-kurkumin analógokat gyulladást elősegítő citokinekkel szemben tesztelték, amelyek erősebb gátló képességet mutatnak, mint a kurkumin.
Szimmetrikus bisz(arilidén)ketonokat állítottunk elő cikloalkanonok és szubsztituált benzaldehidek reagáltatásával, savkatalizált aldolos kondenzációban. A szintetizált vegyületek többsége gátolta a petefészekrák sejtek növekedését, még a ciszplatinra rezisztens sejteknél is [441].
Számos szintetikus aminokarbonil-kurkumin analógot teszteltek Trichomonas vaginalis (ez a "leggyakoribb nem vírusos szexuális úton terjedő fertőzés" a világon) ellen[442]; 15-difenilpenta-1,4-dién{ {5}}egy,15-bisz(2-klórfenil)penta-1.4-dién-3-egy és 2,6-bis({ A {13}}klór-benzilidén)ciklohexanon jelentős parazitaellenes hatást fejtett ki a kurkuminnál alacsonyabb hatékony koncentrációban.
A közelmúltban az első, de nagyon ígéretes eredményt a (2E,6E)-2,6-bisz(2(trifluormetil)benzilidén)ciklohexanonnal sikerült elérni, amelyről azt találták, hogy gyógyítja a cukorbetegség okozta sebeket egerek [426] (3. táblázat).
Egy tucat kurkumin-aminokarbonil-analógot szintetizáltak, hogy olyan vegyületeket találjanak, amelyek megnövekedett kémiai stabilitással és végül jobb rákellenes hatással rendelkeznek egyes emberi rákos sejtekkel szemben [427]. Ezek közül kettő (3. táblázat) megfelelt a követelményeknek, és egymást követően tesztelték őket melanomasejtek ellen, ami szelektíven toxikus hatást eredményezett428].
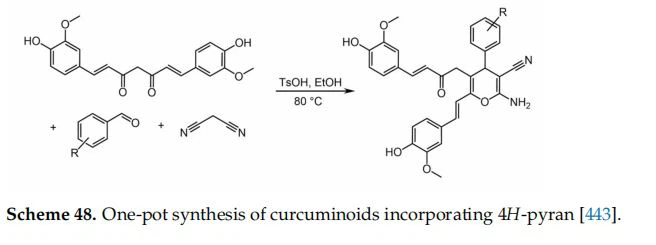
4H-pirán heterociklusokat tartalmazó új kurkuminoidokat állítottak elő kurkumin propanodinitrillel és szubsztituált benzolkarbaldehiddel való egyedényes kondenzációjával (48. ábra)[443]. A -dikarbonil rész ebből következő módosítása javította a -glükozidáz gátlását, amely egyike a szénhidrátok hidrolíziséért és így az étkezés utáni hiperglikémiáért felelős enzimek egyikének. Ez a tulajdonság az antioxidáns aktivitással együtt lehetséges jótékony következményekkel járhat a diabetes mellitus ellen, különösen azért, mert nem észleltek toxikus hatást a közönséges emberi bél mikroflórára.
7.5. A telítetlen lánc hosszának csökkentése
Kurkumin analóg, 5-(3,4-dihidroxifenil)-3-hidroxi-1-(2-hidroxifenil)penta-2,4- A dién-1-egyik gyulladásgátló hatást mutatott egerekben (3. táblázat)[429]. Hasonló, azonos vázzal rendelkező vegyületeket használtak a reaktív oxigénfajták fokozásának fontosságának megállapítására a tumorigenezis elnyomásában [444]. A szerzők szerint ezek a vegyületek ígéretesek egy kevés mellékhatással rendelkező rákellenes gyógyszer kifejlesztéséhez.
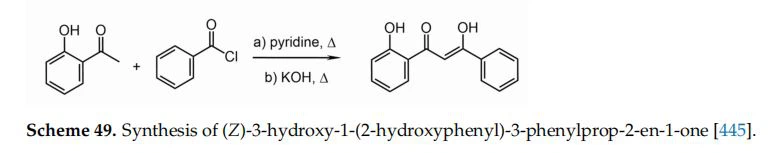
Hasonló, de rövidebb vegyületet, a (Z)-3-hidroxi-1-(2-hidroxifenil)-3-fenilprop-2-én-1-ont állítottak elő. hogy 2-hidroxifenil-metil-ketonból és benzoilből induljunk ki
klorid (49. reakcióvázlat). Az eredményül kapott molekula szelektív citotoxicitást mutatott az emlőrák MCF{1}} sejteken [445], a humán vastagbélrák sejtvonalakon [446] és a humán osteosarcoma sejteken [447].
7.6. Derioatioes a kurkumin szerkezetének csak "félével".
A szerzők által retro-kurkuminoidoknak nevezett vegyületcsaládot úgy készítették elő, hogy a kurkumin szerkezetének csak a felét tartsa fenn (50. séma), mivel a -dikarbonil-csoportot tekintették felelősnek a kurkumin szűkös stabilitásáért [448]. A kapott vegyületek releváns citotoxikus aktivitást mutattak humán rákos sejtvonalakkal szemben, de nem károsították az egészséges sejteket.

Egy szintetikus amid analóg antioxidáns és gyulladásgátló tulajdonságokat mutatott. Jó eredménnyel tesztelték májzsugorodásban indukált elhízással küzdő egereken [430] (3. táblázat).
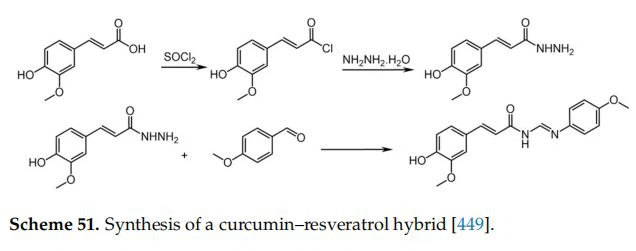
A szubsztituált fahéjsav hidrazid-származékából és egy sor szubsztituált benzaldehidből kiindulva kurkumin-rezveratrol hibridek könyvtárát szintetizálták [449]. Az 51. reakcióvázlaton bemutatott példa a legígéretesebb hibridre utal, mint tumorellenes többcélú szer.
7.7. Fényérzékenyítők
A kurkumin jó biokompatibilitása miatt kiváló fényérzékenyítő lehet, de a gyakorlati felhasználást erősen korlátozza alacsony stabilitása és csekély vízoldhatósága. Megoldást kerestem kationos szubsztituenseket tartalmazó kurkumin származékok előállítására [450] (14. ábra).

Valamennyi származék nagy stabilitást mutatott pH és hőmérséklet mellett. Ami a fotodinamikai tulajdonságokat illeti, az E. coli fotodinamikus inaktivációját tudták elősegíteni, ahol a Hexa-kationos fajok a leghatékonyabbak, valószínűleg a magas hidrofilitás miatt.
Összehasonlító vizsgálatot végeztünk különböző, ad hoc szintetizált kurkumin származékokon, azzal a céllal, hogy növeljük a szöveti penetrációt, növelve a felszívódási maximumot. így 1,11-difenil-1,3,8,10-undekatetraén-57-dion és 1,7-bisz(4'-dimetilaminofenil){{11 A }},6-heptadienil-3,5-dion ígéretes tulajdonságokat mutatott a reaktív oxigénfajták létrehozása és ezáltal a fotodinamikus terápia hatékonysága szempontjából [431]. 8. Következtetések
A természetes fenolok és biológiai aktivitású származékaik gyorsan növekvő kutatási témát jelentenek, tekintettel számos jelenükre és jövőbeli alkalmazásukra. Szerkezeti sokféleségük számos lehetőséget kínál a kémiai átalakításokra, amelyek célja a természetes fenolok hátrányainak leküzdése. Mindazonáltal, eltekintve a rengeteg publikációból kirajzolódó irányelvektől, mint például a bioaktív vegyületek stabilitásának és biológiai hozzáférhetőségének javítása, a szerkezeti követelményekről alkotott kép még nem teljes, tekintettel az in vivo és a helyszíni alkalmazások optimalizálására. .
