D-vitamin, sejtek öregedése és krónikus vesebetegségek: mi hiányzik az egyenletből? Ⅱ
Sep 20, 2023
3. CKD és celluláris öregedés
A legújabb preklinikai kutatások kimutatták a sejtes és molekuláris öregedéssel kapcsolatos mechanizmusok fontos szerepét a természetes öregedésben,AKI, valamint az AKI-CKD átmenetben [2,38–41]. A C57BL/6 egerekben a természetes öregedést csökkent Klotho génexpresszió és aDDRa vesékben amint 12 hónap. Ezenkívül a gyulladásos sejtek beszűrődésével és további Klotho-szabályozással összefüggő elhúzódó DDR-t és állandó sejtciklus-leállást figyeltek meg 18-hónapos egerek veséjében. Ezek az eredmények korai öregedéssel összefüggő változásokat mutatnak a vesében, megelőzve a veseműködési zavart, amelyet 18-hónapos egereknél figyeltek meg [39]. A redox-egyensúly szabályozását kulcsfontosságú mechanizmusként javasolták, amely részt vesz a vesekárosodás során a sejtes öregedés korai aktiválásában. A ROS-termelést és a vesegyulladásos sejtek infiltrációját nefrotoxikus gyógyszer vagy ischaemia-reperfúziós károsodás (IRI) okozta akut tubuláris károsodás váltja ki. Mivel a sérült tubuláris epiteliális sejtek egyes részei nem mennek át hatékony DNS-javításon vagy apoptózison, korai életkorukban (3 hónapos korukban) elöregednek, hasonlóan a természetesen öregedő egereknél megfigyeltekhez [40,41]. Ha azonban idős egereket AKI-nek vetnek alá, mindezek a folyamatok és mechanizmusok felerősödnek [41]. Ezenkívül a természetesen öregedő egerekben a 12 hónapos korai öregedési aktiváció a redox egyensúly felborulásával, a nukleáris faktor (eritroid eredetű 2)-szerű 2 (Nrf2) deregulációjával, fokozott lipid-peroxidációval és vesegyulladással társult [39]. Az Nrf2 az indukálható antioxidáns válaszok fő szabályozója, amely mérsékelheti az oxidatív stressz okozta sejtkárosodást [42]. A különböző AKI-modellekben végzett preklinikai vizsgálatok korai sejtöregedés-aktivációt írtak le, beleértve a p21 expressziójának fokozását. Ezenkívül az IRI-ben a p53-inhibitorral végzett kezelés bebizonyította a G1 sejtciklus leállításának fontosságát az AKI-ről CKD-re való átmenetben és a fibrózis progressziójában [38–41]. További vizsgálatokra van szükség a vesekárosodásban és -javításban szerepet játszó sejtes és molekuláris mechanizmusok feltárására, beleértve a helyreállítási folyamat kudarcát is.

KATTINTSON IDE, HOGY KIVÁLÓ MINŐSÉGŰ 25%-OS ECHINACOSIDE CISTANCÉT SZEREZZA VESEMŰKÖDÉS MEGŐRZÉSE
Érdekes módon az öregedő sejtek ellenőrzött eltávolítása ("szenoterápia") meghosszabbítja az egészséges élettartamot, ésmegőrzött veseműködés[43]. A vesekárosodásban szerepet játszó másik lehetséges mechanizmus a sérült tubuláris sejtek SASP indukciója által okozott másodlagos öregedésnek köszönhető. A SASP összetevőit célzó legújabb vizsgálatok vesevédő hatást mutattak ki. Ebben az értelemben a CCN{1}}deletált egereken végzett IRI-vizsgálatok kimutatták, hogy a CCN2 a SASP-szekréció része, amely önmagában is kiválthatja az öregedést. Tenyésztett rágcsáló tubuláris epiteliális sejtekben a CCN2-vel végzett stimuláció öregedő sejtfenotípust indukált [38]. Ezenkívül a humán vesetranszplantátumok megnövekedett CCA-val kapcsolatos fehérjéket mutattak a CCN2 fehérje fokozódásával összefüggésben, ami megerősíti az egérkísérletek klinikai jelentőségét [38]. Azonban további preklinikai vizsgálatokra van szükség annak értékelésére, hogy a CKD-ben vagy vesegraftokban az öregedés megcélzása milyen mértékben csökkenti a fibrózist és javítja a veseműködést és a graft túlélését.
4. D-vitamin, öregedés és CKD
A D-vitamin-útvonal hibái lehetnekzavarják a vese képességéthogy aktiválja ezt a hormont [44]. Ezenkívül alacsony D-vitaminszintet figyeltek meg olyan állapotokban, mint például a korai öregedés és a CKD, ami hatással lehet a betegség progressziójára és a betegek kimenetelére. E bizonyítékok ellenére ezen a területen számos megválaszolatlan kérdés még további vizsgálatot igényel, hogy teljes mértékben megértsük a D-vitamin-hiány és a D-vitamin-útvonal hibáinak emberi egészségre gyakorolt hatását. Itt röviden áttekintjük a D-vitamin fő hatásmechanizmusait, valamint kapcsolatát az öregedéssel, az immunrendszer szabályozásával és a vesekárosodással.
4.1. A D-vitamin szintézise és hatásmechanizmusai
A D-vitamin fő keringési formája, a 25-dihidroxi-D3-vitamin (25(OH)VD3) a májban szintetizálódik a D3-vitaminból (VD3), amely a 7-dehidrokoleszterin átalakulásának eredménye. a bőrben. A VD3 az étrendből is beszerezhető. A 25-dihidroxi-D3-1 --hidroxiláz enzim katalizálja átalakulását 1,25(OH)2VD3-má, amelyet kalcitriolnak vagy 1,25D-nek is neveznek, amely a legaktívabb natív D-vitamin metabolit és egy erős szteroid hormon [45] ]. Ezt az enzimet a mitokondriumok nagy mennyiségben expresszáljákvese proximális tubuláris sejtjei, de különböző szövetekben is megtalálható, így az immunrendszerben is. Ezért sok sejttípus képes lokálisan 1,25D-t termelni, és képes autokrin vagy parakrin funkciókat megjeleníteni, ami megmagyarázza pleiotróp tulajdonságait [46]. Másrészt az 1,25D főként avese és béla D-vitamin 24-hidroxiláz enzim [47]. A D-vitamin hiánya az elégtelen napozáshoz kapcsolódik, és gyakori télen és időseknél, valamint számos betegségben [14–20]. Érdekes módon meg kell fontolni a D-vitamin pótlását, ha D-vitamin-elégtelenség vagy hiány áll fenn, azaz amikor a szérum 25-OH-D-vitamin szintje 30 ng/ml alatt van [48].

A D-vitamin funkcióit a D-vitamin receptoron (VDR) keresztül fejti ki [44]. A VDR a nukleáris receptor szupercsalád tagja, és 1,25D kötődés hatására specifikus, elsődleges és másodlagos célgénekként osztályozott gének transzkripciós faktoraként viselkedik [49,50]. Az elsődleges célgének főként az 1,25(OH)2VD3-aktivált VDR által közvetlenül szabályozott transzkripciós faktorokból állnak. Szabályozzák a másodlagos célgének expresszióját, amelyek túlnyomórészt leszabályozottak: a D-vitamin bizonyos gyulladásgátló hatásait így modulálják [51]. Ezért a VDR-hez való 1,25D kötődés szabályozza az ásványi homeosztázist és a csontrendszer egészségét szabályozó gének transzkripcióját, de olyan gének transzkripcióját is, amelyek szabályozzák az immunrendszert, a vese- ésszív- és érrendszeri funkciók[43]. A VDR számos sejttípusban expresszálódik, ezért a VDR mindenütt jelenlévő expressziója magyarázatot adhat a D-vitaminnak a klasszikus kalcium-anyagcserére gyakorolt hatásai mellett [52] a vérképző őssejt-termelésre, az immunrendszer szabályozására, a sejtciklusra és a különböző metabolikusokra. függvények [53–55].
A D-vitamin más membránreceptorokat is aktiválhat, például az 1,25D(3)-MARRS szteroidkötő fehérjét, amelyet ERp57/GRp58-nak is neveznek [56,57]. Ez a receptor nemgenomikus hatásokat közvetít, amelyek a gyors membrán által kezdeményezett jelátvitelhez kapcsolódnak [57]. A bélsejtekben az 1,25D3-MARRS közvetítette a kalcium [58,59] és a foszfát [60] felszívódását azáltal, hogy gyorsan stimulálta ezek szállítását. Az 1,25D3-MARRS szerepét a rákban tanulmányozták a legszélesebb körben [61–63], amely az extracelluláris és intracelluláris redox aktivitásokhoz, valamint a STAT3 megkötéséhez kapcsolódik [64]. A vesére vonatkozóan kevés az adat. Megnövekedett ERp57 vizeletszintet figyeltek meg humán CKD-s betegek korai stádiumában, és ez korrelált a vesefibrózis súlyosságával [65], amint azt a kísérleti vesefibrózisban [65] megfigyelték. A tenyésztett tubuláris hámsejteken végzett in vitro vizsgálatok azonban azt mutatták, hogy a VDR agonista parikalcitol gyulladásgátló hatásait, beleértve az NF-κB2 aktivációt, nem a MARRS/ERp57 közvetíti [66]. Ezek az eredmények arra utalnak, hogy további vizsgálatokra van szükség az 1,25D3-MARRS szerepének meghatározásához a D-vitamin veseműködésében.
4.2. D-vitamin, mint öregedésgátló faktor
A D-vitamin egyes nem klasszikus hatásai ellensúlyozhatják az öregedés jellemzőit [6,7] (1. ábra). In vitro kísérletek kimutatták, hogy az 1,25D csökkenti a progerin káros hatását a genom stabilitására. A progerin az LMNA gén mutáns formája, amely progéria szindrómában expresszálódik, és gátolja a RAD51-et, ami a cGAS/STING/IFN kaszkád aktiválásához és a DNS instabilitásához vezet. A D-vitamin megakadályozza a RAD51 elvesztését, így korlátozza a progerin káros következményeit [67]. Ezenkívül az alacsonyabb D-vitamin-szinthez kapcsolódó rövidebb élettartam összefüggésbe hozható a telomerek hosszával. Klinikai vizsgálatok azt mutatják, hogy a D-vitamin szintje vagy bevitele hosszabb leukocita telomerhosszal vagy telomeráz aktivitással jár [68]. Ebben az összefüggésben a DNS-metilációt specifikus CpG-dinukleotidoknál a biológiai öregedés biomarkereként javasolták [69]. Két humán tanulmány kimutatta, hogy a D-vitamin szintje vagy a D-vitamin-kiegészítés alacsonyabb epigenetikai életkorral és alacsonyabb halálozási kockázattal jár [70,71].
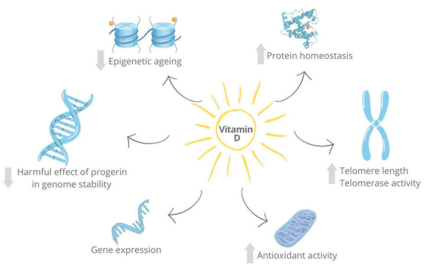
1. ábra. A D-vitamin pleiotróp hatásai a sejt öregedésével kapcsolatban. Az 1,25D ellensúlyozza a progerin hatását a DNS stabilitására, segít szabályozni az epigenetikus életkort, fenntartja a fehérje homeosztázist, megőrzi a telomerek hosszát, szabályozza a géntranszkripciót és csökkenti az oxidatív stresszt a pro-oxidáns és antioxidáns gének szabályozásával
A proteosztázis elvesztése az öregedés másik jellemzője [7]. A D-vitamin-kiegészítés elősegíti a fehérje homeosztázist és meghosszabbítja a C. elegans élettartamát azáltal, hogy indukálja a Nrf2-, mint a xenobiotikus és az oxidatív stressz-válasz faktor (SKN-1) célgének génexpresszióját (72Ez az út szabályozása emlősökben is megerősítették: 10(OH)áz-/- egerekben az 1,25 duplán szabályozott Nrf2, csökkent ROS, csökkent DNS-károsodás, p16 /Rb és p53/p21 jelátviteli celluláris öregedés és SASP, valamint megnövekedett sejtproliferáció és élettartam (73). .
Ezenkívül a D-vitamin-útvonal génjeinek genetikai hibái korai öregedéssel járnak. A VDR knockout (KO) egerek például öreg fenotípust mutatnak [74]. A magas kalcium-, foszfát- és laktóztartalmú étrenddel kezelt VDR KO egerek várható élettartama csökkent, méretük kisebb, alopecia és megváltozott a bőr szerkezete [74]. A VDR KO egerek megváltozott inzulinszekréciót [75], szívelégtelenséget [76], rendellenes motoros viselkedést [77] és más, idő előtti öregedést idéző jellemzőket is mutathatnak. Az 1 (OH)áz KO egerek élettartama lecsökkent, amit exogén 1,25D-vel megfordíthat [73]. Érdekes módon a D-vitamin génhibái fokozott oxidatív stresszel járnak. Az 1 (OH)áz KO egerekben a ROS szintek számos szövetben szignifikánsan megemelkedtek, a bőrben és a májban pedig csökkent a szuperoxid-diszmutáz 2 és a peroxiredoxin I expressziója [73.
4.3. D-vitamin és az immunrendszer
A D-vitamin nem klasszikus hatásai közül a gyulladáscsökkentő hatások fontosak lehetnek az öregedés modulálásában, mivel a szisztémás gyulladás az idősek halálozásának előrejelzője [78,79]. Az 1,25D szabályozhatja az immunrendszert, csökkenti a gyulladást és serkenti a toleranciát, amint azt a közelmúltban áttekintették [10,11] A monociták és a makrofágok 1,25D-t termelhetnek, ami a cathelicidin LL stimulálásával fokozza antimikrobiális aktivitásukat-37 [80– 83]. Másrészt, a D-vitamin adása gátolta az LPS által kiváltott citokintermelést monocitákban és makrofágokban a MAPK foszfatáz-1 felszabályozásán, valamint az ezt követő p38 és JNK inaktivációján keresztül [84]. Ezenkívül az 1,25D gátolta az NF-κB jelátvitelt a VDR célgének, például a THBD [85] és a LILRB4 [86] felpörgetése révén. Figyelemre méltó, hogy a lokálisan aktivált 1,25D különböző immunsejttípusokban is befolyásolhatja a fenotípus változásait. Az 1,25D gátolja a limfocita T proliferációt, modulálja a citokintermelést [87,88] és a VDR/PLC- 1/TGF- 1 útvonal modulálásával indukálja a szabályozó T-sejteket [89] (2. ábra). A VDR analógok elnyomták a Th17 differenciálódását in vitro a STAT3 és RORgt szabályozásával, amely két kulcsfontosságú transzkripciós faktor szabályozza ezt a folyamatot [90]. Ezenkívül a D-vitamin modulálja a dendrites sejtek érését és működését [91]. Az 1,25D emellett stimulálja a gyulladáscsökkentő citokin interleukin-10 termelését gyenge, korai és fitt betegekben [92].

2. ábra D-vitamin és T-sejtek. Az 1,25(OH)2VD3 a PLC- 1 és a TGF- 1 expressziójának növekedéséhez vezet, ami végső soron a FOXP3 expresszió indukcióját és a naiv T-sejtek szabályozó T-sejtekké történő differenciálódását eredményezi (Treg).
4.4. A D-vitamin egyéb öregedéssel kapcsolatos célpontjai
A Klotho egy öregedésgátló fehérje, főleg a vesetubulusokban termelődik [93]. A preklinikai adatok azt mutatták, hogy az 1,25D fokozta a Klotho gén transzkripcióját a vesében [94]. Monocitákban a Klotho megakadályozta a Golgi apparátus aktiválódását és az endoplazmatikus retikulum stresszválaszát a CREB34L, TFE3, ATF6 és IRE1 felszabályozásával, gátolva a SASP komponensek génexpresszióját [95]. Ebben a tekintetben a Klotho gyulladáscsökkentő hatással is rendelkezik a pro- és gyulladásgátló faktorok szabályozásán keresztül, amelyek közül néhány a SASP összetevője, sejttenyészetekben és in vivo [96,97]. Kimutatták, hogy a Klotho csökkenti az oxidatív stresszt a kardiovaszkuláris rendszerben és az érrendszeri öregedést [98,99], valamint modulálja a gyulladásos jelátviteli útvonalat a hasnyálmirigy béta sejtjeiben és a diabéteszes kardiomiopátiában [100–103]. Mindezek az adatok alátámasztják, hogy a Klotho-szabályozás egy másik lehetséges mechanizmus lehet a D-vitamin öregedésgátló hatásában.
A sirtuinok (SIRT) az enzimek egy csoportja, amelyekről kimutatták, hogy modulálják az öregedési folyamatot [104,105]. Ezek a fehérjék a nikotinamid-adenin-dinukleotidra (NAD+) támaszkodnak, amely poszttranszlációsan módosíthatja a fehérjéket [106]. A Sirtuin-1 (SIRT1) elsősorban a sejtmagban található, szabályozza a génexpressziót és dezacetilezi az intracelluláris jelátviteli fehérjéket, köztük a hisztonokat [107]. Ez a fehérje hosszú élettartammal jár, és negatív szabályozó hatással van az NF-κB jelátvitelre [108,109]. Ezenkívül a SIRT1 aktiválása megakadályozta az endothel öregedését a PGC-1 dezacetilezésével, a PPAR aktiválásával, valamint a NADPH oxidáz által közvetített ROS termelés és a NO inaktiváció leszabályozásával [110]. Ezenkívül a SIRT1 lelassította a vaszkuláris meszesedést az endothel NO biohasznosulásának és öregedésének modulálásával, ami a D-vitamin-kezeléssel helyreállított folyamatokat [111].Az öregedő vesékben, a SIRT1 expressziója csökkent, és más célmolekulák, köztük a PGC-1 /ösztrogénnel rokon receptor-1 (ERR-1), PPAR, Klotho és HIF{{ expressziójában bekövetkezett változásokhoz kapcsolódott 5}} [112,113]. Azonban jövőbeli tanulmányokra van szükség annak bizonyítására, hogy a sirtuinok célba juttatása milyen jótékony hatással van az emberi öregedésre.
4.5. D-vitamin és CKD
Az endokrin 1,25(OH)2VD3 főként a proximális tubuláris sejtek mitokondriumaiban termelődik. CKD-ben a proximális tubuláris sejtek károsodása korlátozza az 1,25D biohasznosulását, mivel fokozatosan csökkena vese képességét1 -hidroxilázt termelnek, a fent említettek szerint, hozzájárulva ezzel a betegség klinikai megnyilvánulásaihoz (3. ábra). Az 1,25D termelés elvesztése kulcsfontosságú szerepet játszik a CKD ásványi és csontrendszeri rendellenességben (CKD MBD), amely a másodlagos hiperparatireózist okozza. A D-vitamin feltöltését, a kalcitriolt és a VDR aktivátorokat, például a parikalcitot régóta használják a másodlagos hyperparathyreosis megelőzésére vagy kezelésére. Ezenkívül az újabb adatok felfedték a VDR aktiválásának funkciójátvese- és szív- és érrendszeri egészség[44,45]. A szérum 25-hidroxi-D-vitamin [25(OH) D] szintje 20 és 30 ng/ml között nem tekinthető elegendőnek, és<20 ng/mL deficient [114]. Recent guidelines recommend measuring and treating vitamin D insufficiency in patients with CKD categories G3–G5 [115]. However, the active molecule and the dose to be used are still debated.

3. ábra D-vitamin és a vese. Sérülésre válaszul a tubuláris hámsejtek mitokondriális diszfunkciója csökkenti a 1 25D-t az alacsonyabb aktiváció miatt. Ezenkívül a D-vitamin hiánya hozzájárul a vesekárosodás progressziójához.
4.5.1. D-vitamin-receptor aktiválása és kísérleti vese
Károsodás A preklinikai vizsgálatokban a D-vitamin receptor agonistákkal (VDRA-kkal) végzett kezelés vesevédő hatást mutatott, beleértve a gyulladáscsökkentő hatást (116,117). Az egyik legtöbbet tanulmányozott VDRA a szintetikus D-vitamin analóg paricalcitol (19-nor-1,25-hydroxyvitaminD(2)). Ciklosporin A által kiváltott nefropátiában a parikalcitol javította a veseműködési zavarokat és csökkentette a monocita/makrofág infiltrációt, a gyulladásos citokinek vesén belüli túlzott expresszióját a mitogén által aktivált protein kináz jelátviteli útvonalak gátlásán keresztül (118,119). csökkentette a gyulladásos sejtek infiltrációját és a citokintermelést a COX-2 és a PGE2 (120) fokozása révén. Ebben a modellben a Toll-like receptor 4 (TLR4) aktiváció gátlása is szerepet játszik a parikalcitol gyulladásgátló hatásában [121] Az unilaterális ureterelzáródás (UUO) modellben egerekben a parikalcitol csökkentette a T-sejtek és makrofágok infiltrációját, valamint a RANTES és a TNF-alfa expresszióját az elzáródott vesékben [122]. patkányoknál a kalcitriollal vagy parikalcittal végzett kezelés csökkentette az IL-6, a monocita kemoattraktáns fehérje (MCP)-1 és az IL-18 teljes vese mRNS-expresszióját a vesefunkció vagy az albuminuria jelentős csökkenése nélkül [123] . Az adriamicinnel indukált fokális szegmentális glomerulosclerosis egérmodellben a VDRA-k csökkentették a podocita sérülést és a proteinuriát a Wnt/-catenin jelátvitel blokkolása révén [124]. Az 22-oxa-kalcitriol csökkentette a podocita károsodást, korlátozta a lábnyúlványok kiürülését és növelte a nephrin, CD2AP és podocin expresszióját [125]. A kalcitriol csökkentette a podocita tranziens receptor potenciál kationcsatorna C6 (TRPC6) expresszióját [126]. Ezenkívül a VDRA-k és a renin-angiotenzin rendszer blokkolása kombinációja csökkentette az albuminuriát és a podocita károsodást [127]. Egerekben a streptozotocin által kiváltott diabéteszes nephropathiában a doxercalciferol vitaminanalóg és az AT1 antagonista lozartán egyidejű alkalmazása volt a leghatékonyabb beavatkozás az albuminuria csökkentésére, a glomeruláris filtrációs gát szerkezetének megőrzésére és a glomerulosclerosis csökkentésére [128]. Hasonló eredményeket figyeltek meg a lozartánnal és parikalcittal kezelt diabéteszes Lprdb/db egereknél [129]. Mindezek a preklinikai adatok egyértelműen bizonyítják a VDRA-k gyulladásgátló hatását a vesekárosodásban.

Az NF-κB útvonal az egyik legfontosabb jelátviteli útvonal, amely részt vesz a gyulladások és az immunfunkciók szabályozásában [130]. Egyes tanulmányok szerint a parikalcitol blokkolhatja az NF-κB aktivációt (4. ábra) [123]. Érdekes módon az UUO modellben a parikalcitol gátolja a vesegyulladásos infiltrációt és a RANTES expresszióját azáltal, hogy elősegíti az NF-κB jelátvitel VDR-közvetített megkötését [122]. A kanonikus NF-κB1 útvonal aktivációját a gyulladást elősegítő génszabályozással hozták összefüggésbe [122]. Konkrétan a p65 foszforilációja a Ser536-on, az aktív p65–NF-κB komplex ezt követő transzlokációja a sejtmagba, majd a specifikus promóterekhez való kötődés bizonyítottan szabályozza a gyulladást elősegítő gének, köztük az MCP-1 és a RANTES géntranszkripcióját. [121]. A nem kanonikus NF-κB2 útvonal aktiválódását a közelmúltban a vesekárosodással is összefüggésbe hozták [66]. Ezt az utat a TNF receptor-asszociált faktorok (TRAF) és az NF-κB-indukáló kináz (NIK) szabályozzák. CKD-s betegekben a parikalcitol-kezelés helyreállította a keringő TRAF3 szintet, gátolva a nem kanonikus NF-κB2 útvonalat és csökkentve a vesegyulladást [66]. Az IRI által kiváltott AKI-ban a parikalcitol csökkentette a gyulladásos választ azáltal, hogy elnyomta a TLR4- NF-κB jelátviteli útvonalat, és csökkentette a gyulladást elősegítő citokinek, például az IL-6 és az MCP-1 expresszióját [ 131]. Amint azt korábban megjegyeztük, a CKD-ben a Klotho leszabályozott. A CKD D-vitamin-hiányos kombinált patkánymodelljében a parikalcitol-kezelés nem változtatta meg a szérum-Klotho-t, de enyhítette a vese- és érkárosodást [132]. Kísérleti CKD modellekben a D-vitamin-hiányos étrend TGF-/Smad2/3-közvetítette EMT-vel összefüggő vesefibrózist indukál [133]. VDR-génhiányos egereken végeztek vizsgálatokat a VDR VDRA-hatásokban betöltött szerepének felmérésére [66,134–136]. UUO-ban a VDR-hiányos egerekben a veseléziók súlyosbodnak [137]. Ebben a modellben a parikalcitol elnyomta a vese fibrotikus markereket, például a TGF-béta1-et [138]. Ezenkívül az alfa{51}}savas glikoprotein (AGP), a kalcitriol egy downstream molekulájának beadása az UUO modellben gyengítette a fibrózist és a gyulladást [139]. A Nrf2 egy fontos transzkripciós faktor, amely az antioxidáns védelemben vesz részt az antioxidáns enzimek, például a hem oxigenáz -1 (HO-1) downstream génexpressziójának szabályozása révén. A ciszplatin által kiváltott AKI modelljében a parikalcitol renoprotektív hatást fejt ki azáltal, hogy a Nrf2/HO-1 jelátvitel révén csökkenti a vese oxidatív károsodását és gyulladását [140]. Ebben az értelemben a SIRT1-ről kimutatták, hogy az antioxidáns útvonalak, például a Nrf2/HO-1 jelátvitel aktiválásával gyengíti az IR által kiváltott vesekárosodást [141]. A SIRT1 a HIF-1 dezacetilációja révén védőhatást is nyújthat a tubulointersticiális károsodás ellen [113]. Ezenkívül a podocita SIRT1 csökkenése felgyorsítja a vesekárosodást [142]. Érdekes módon kevés tanulmány értékeli, hogy a VDRA-k módosíthatják-e az öregedéssel kapcsolatos vesekárosodást. Ebben az értelemben patkányokban a kontrasztanyag által kiváltott AKI modelljében a parikalcitol enyhítette a vesekárosodást az apoptotikus sejthalál, a mitofág és a p16 és -galaktozidáz öregedési markerek downregulációja révén [143]. A VDR hiánya a podocitákban fokozza a p53 expresszióját, ami az Agt és az AT1R fokozott transzkripciójához vezet, ami a SIRT1 leszabályozásával aktiválja a RAS útvonalat [144]. Amint azt korábban megjegyeztük, a SASP számos komponensét az NF-κB transzkripciós faktor szabályozza [33–35]. Ezért az NF-κB útvonal aktiválását gátló hatások, amelyeket néhány tanulmányban a parikalcitolra adott válaszként leírtak, arra utalnak, hogy a parikalcitol gátolja a másodlagos öregedést, bár jövőbeli vizsgálatokra van szükség.

4. ábra: D-vitamin és celluláris öregedés a vesében. A sérülésekre válaszul javasolt mechanizmusok; A tubuláris epiteliális sejtekben a mitokondriális diszfunkció csökken a 1 25D az alacsonyabb aktiváció miatt. Ezenkívül a D-vitamin hiánya hozzájárul a vesekárosodás progressziójához.
4.5.2. A D-vitamin-receptor aktiválása és az emberi vesebetegségek
Számos megfigyeléses tanulmány hangsúlyozza a 25(OH) D-szint és a szív- és érrendszeri betegségek, az érelmeszesedés, a magas vérnyomás és a szívbetegség közötti összefüggést CKD-betegeknél és időseknél (145). A D-vitamin-hiány független előrejelzője volt a szívelégtelenségben szenvedő vagy anélküli betegek halálozásának ([146-149]. Felmerült, hogy a halálozás szezonális ingadozása (azaz a szív- és érrendszeri betegségek okozta halálozások számának csökkenése nyáron, illetve a téli halálozások számának növekedése) összefüggésbe hozható a vér alacsonyabb D-vitamin-szintjével télen [ Megfigyeléses és klinikai vizsgálatokban a VDRA-k a PTH-szinttől függetlenül alacsonyabb kardiovaszkuláris és egyéb halálozási rátákkal jártak együtt (20 151 152).
A D-vitamin-pótlás klinikai hatása a vese- vagy szív- és érrendszeri betegségekre a CKD-MBD-n túlmenően vitatéma volt a kutatók között. Chun Hu és munkatársai (153) egy áttekintésben azt találták, hogy a bizonyítékok nem elegendőek annak alátámasztására, hogy a D-vitamin javítja az érrendszeri működést és csökkenti a gyulladást az ilyen betegeknél. Másrészt Ding Dou és munkatársai [154] úgy vélték, hogy a D-vitamin-kiegészítők előnyei a dózistól és a betegség progressziójától függően változhatnak. Mindeközben és munkatársai (155) pozitív eredményekről számoltak be a rövid távú D-vitamin-beavatkozásokból az endothel funkció javítása tekintetében. Két áttekintés azonban ( 156 157] egyetértettek abban, hogy a D-vitamin pótlása nem befolyásolja pozitívan a szívműködést és szerkezetet. Egy közelmúltban végzett metaanalízis azt is feltárta, hogy a parikalcitol csökkenti a kardiovaszkuláris események kockázatát, de nem védi a vesefunkciót (157.
A betegek különböző jellemzői, beleértve az olyan változókat, mint a D-vitamin-hiány korábbi fennállása, az étkezési sóbevitel vagy más jellemzők, megmagyarázhatják egyes adatok következetlenségét [158-160]. A vese- vagy szív- és érrendszeri betegségekre gyakorolt hatáson túlmenően a D-vitamin-pótlás javíthat bizonyos, a krónikus vesebetegséggel összefüggő patológiákat. Például egy 2019-es szisztematikus áttekintés kimutatta, hogy a 25(OH)D normál vagy magas szintje és a táplálékkiegészítők használata az összetett fertőzések alacsonyabb kockázatával jár együtt a hosszú távú dialízis alatt álló betegeknél [161]. Egy másik, ugyanebben az évben publikált tanulmány kimutatta, hogy a D-vitamin-kezelés javította az éhomi glükóz-, a HOMA-IR-, a triglicerid- és a koleszterinszintet a krónikus vesebetegségben szenvedő betegeknél [162]. Ezek az eredmények befolyásolhatják a D-vitamin-szint és a krónikus vesebetegségben szenvedő betegek mortalitása közötti lehetséges összefüggést. Ebben a tekintetben bizonyíték van arra, hogy a magas D-vitamin szint a krónikus vesebetegségben szenvedő betegek minden okból eredő halálozásának alacsonyabb kockázatával jár [163], bár más szerzők azt állítják, hogy a bizonyítékok nem elegendőek ennek alátámasztására [164].
A Wecistanche támogató szolgáltatása – Kína legnagyobb ciszterna exportőre:
E-mail:wallence.suen@wecistanche.com
Whatsapp/Tel.:+86 15292862950
Üzlet:
https://www.xjcistanche.com/cistanche-shop






