A klinikailag releváns nonszensz mutáció által okozott ataxia telangiectasia új, ataxiás egérmodellje (1. rész)
Jun 10, 2022
További információért kérem vegye fel a kapcsolatotdavid.wan@wecistanche.com
Absztrakt
Az ataxia telangiectasia (AT) és az 1-es típusú okuláris apraxiával (AOA1) járó ataxia pusztító neurológiai rendellenesség, amelyet a genom stabilitási gének nullmutációi okoznak, az AT mutált (ATM) és az Aprataxin (APTX) génekben. E rendellenességek kezelésére szolgáló mechanikai ismereteink és terápiás repertoárunk súlyosan hiányzik, nagyrészt azért, mert a korábbi, hasonló nullmutációkkal rendelkező állatmodellek nem tudták összefoglalni a motoros koordináció jellegzetes elvesztését (azaz ataxiát) és a kapcsolódó kisagyi hibákat. NövelésévelgenotoxikusUgyanabban az állatban az Atm (nonszensz) és az Aptx (knockout) gének nullmutációinak beiktatása révén egy új egérmodellt hoztunk létre, amely először fejleszt ki fokozatosan súlyos ataxiás fenotípust, amely a kisagyi molekula sorvadásához kapcsolódik. réteg. Azt találtuk, hogy a cerebelláris Purkinje neuronok biofizikai tulajdonságai jelentősen megzavarodtak (pl. csökkent membránkapacitás, alacsonyabb akciós potenciál küszöbértékek stb.), míg a szinaptikus bemenetek tulajdonságai nagyrészt változatlanok maradnak. Ezekzavarokjelentősen megváltoztatják a Purkinie neuron idegi aktivitását, beleértve a spontán akciós potenciál tüzelésének fokozatos csökkenését
az a gyakoriság, amely az állat első életévében korrelál mind a cerebelláris atrófiával, mind az ataxiával. A kettős mutáns egerek szintén nagy hajlamot mutatnak a rák (timomák) és az immunrendszeri rendellenességek (a timociták korai fejlődésének és a T-sejtek érési zavarának) kialakulására, amelyek az AT-re jellemző tünetek. Végül egy klinikailag releváns nonszensz típusú nullmutáció beiktatásával az Atm-be bemutatjuk, hogy a Small Molecule Read-Through (SMRT) vegyületek visszaállíthatják az ATM-termelést, jelezve, hogy potenciálisan a jövőbeni AT-terápia.


Kattintson ide, ha többet szeretne megtudni Cistanche-ról
1.{1}} Bevezetés
Az ataxia telangiectasia (AT) egy ritka (1:100,000) (Swift és mtsai, 1986), egy autoszomális recesszív genetikai rendellenesség, amelyet rákra való hajlam, immunhiány és erősen behatoló, progresszív és súlyos ataxia jellemez. kisagyi atrófiához (Rothblum-Oviatt et al. 2016; Boder és Sedgwick 1958; Levy és Lang 2018). Az AT-betegek jellemzően életük második vagy harmadik évtizedében halnak meg (Crawford et al. 2006) nyirokrák, légúti fertőzések vagy ataxia szövődményei következtében – sajnos a túlélés nem változott drámai módon az 1950-es évek óta (Micol et al. 2011; Rothblum- Oviatt et al.2016). Míg a betegség progressziója és a halálozás okai nagyon eltérőek a betegek között, a jelentések szerint a mozgáskoordináció erősen behatoló, progresszív hanyatlása van a legnagyobb negatív hatással a páciens életminőségére (Jackson et al. 2016). Az ellátás általában palliatív jellegű, a rákos megbetegedések vagy fertőzések csökkentésére, korlátozására vagy megszüntetésére irányul. Nem állnak rendelkezésre hosszú távú terápiák az ataxia és a kapcsolódó kisagyi diszfunkció és atrófia kezelésére. Az AT-t az ATM hiánya vagy működési zavara okozza (AT mutált) fehérje (Savitsky et al. 1995). A nonszensz mutációkat okozó korai terminációs kodon (PTC) az ismert esetek felét teszi ki, amihez a missense és a deléciós mutációk is hozzájárulnak (Concannon és Gatti 1997; Sandoval et al. 1999). Az ATM egy szerin/treonin PIKK családba tartozó kináz, amely kulcsszerepet játszik a DNS-károsodási válaszban (DDR), megvédve a sejteket a naponta előforduló több tízezer DNS-sérüléstől (Lindahl és Barnes 2000; Kastan és Bartek 2004; Shiloh és Ziv 2013). Az aktív monomer formában az ATM több kulcsfontosságú fehérjét foszforilál, leállítva az új DNS termelődését (sejtciklus leállás) (Ando et al. 2012), majd a károsodás súlyosságától függően DNS-javítást vagy programozott sejtet indít el. halál (azaz apoptózis) (Ando et al. 2012; Rashi-Elkeles et al. 2006). Az ATM számos downstream DDR-útvonalbeli célpontját azonosították, köztük a p53-at, a CHK2-t, a BRCA1-et, az SMC1-et és az NBS1-et (Matsuoka és mtsai, 2007). Az ATM DNS-javításban betöltött szerepe az immunrendszer normál fejlődésében is szerepet játszik, ahol azt javasolják, hogy hozzájáruljon. a természetes DNS-splicing rekombinációjához, amely a T- és B-limfocita érésének génátrendeződése során következik be (Chao, Yang és Xu 2000; Matei, Guidos és Danska 2006; Vacchio et al. 2007; Schubert, Reichenbach és Zielen 2002 ). Bár szerepei még csak kialakulóban vannak, az ATM szerepet játszik az oxidatív stressz homeosztázisában (Guo és mtsai, 2010) és a mitofagiában (Valentin-Vega és Kastan 2012; Pizzamiglio, Focchi és Antonucci, 2020). Nem világos, hogy az ATM-hiány miért okoz ataxiát, de messze nem ez az egyetlen DDR-fehérje, amely az ataxiához kapcsolódik, mivel az Aprataxin (APTX) (Aicardi és mtsai 1988), Meiotikus rekombináció 11 homológ 1 (MRE11) (Sedghi et al. 2018), Nibrin (NBS1) (van der Burgt et al. 1996), Senataxin (SETX) (Moreira et al. 2004) és a tirozil-DNS foszfodiészteráz 1 (TDP1) (Takashima et al. 2002), ha hiányzik vagy nem működik, kisagyi eredetű ataxiát okozhat. Ez arra utal, hogy a genom-instabilitási szindrómák neurológiai jellemzőinek közös oka van, bár ezt még mechanikusan bizonyítani kell (McKinnon 2009; Rass, Ahel és West 2007). Az egyik fő tényező, amely korlátozza azon képességünket, hogy meghatározzuk, hogy a DDR-fehérjék, például az ATM elvesztése miért hat szelektíven a kisagyra és okoz progresszív ataxiát, az, hogy nincs olyan állatmodell, amely összefoglalná ezeket a neurológiai tüneteket (Lavin 2013). Az elmúlt évek során számos AT rágcsálómodellt hoztak létre olyan génmutációk beiktatásával, amelyek fehérje diszfunkciót (kinázaktivitás hiányát) vagy teljes hiányt okoznak (Herzog és mtsai 1998; Xu és Baltimore 1996; Elson és mtsai 1996; Spring et al.). 2001; Campbell és mtsai. 2015; Quek és mtsai. 2016; Tal és mtsai. 2018; Lavin 2013); egy törpesertésről is nemrégiben számoltak be (Beraldi et al. 2017). Mindazonáltal egyiknél sem alakul ki nyilvánvaló, progresszív ataxia kisagyi diszfunkcióval és sorvadással, amely az emberi betegséget ismétli, annak ellenére, hogy a rendellenesség egyéb aspektusai, mint például a pajzsmirigyrák, a meddőség és az immunrendszeri rendellenességek kialakulnak. Továbbra sem világos, hogy ezek a korábbi állatmodellek miért nem mutatják a progresszív ataxiás fenotípust (Lavin 2013). Lehetséges, hogy az egerekben a fajspecifikus molekuláris kompenzációk redundanciákat vagy alternatív útvonalakat biztosítanak, amelyek minimalizálják az ATM-hiány hatásait az agyban (El-Brolosy és Stainier 2017). Az is lehetséges, hogy a korábbi modellek lerövidített élettartama (Barlow et al. 1996) túl rövid ahhoz, hogy a kisagyi diszfunkciót és sorvadást kiváltó sztochasztikus mechanizmusok felhalmozódjanak és befolyásolják a motoros viselkedést. Az egyéb kihívások közé tartoznak a potenciálisan szivárgó genetikai manipulációk, amelyek alacsony szintű ATM fehérjét vagy maradék kinázaktivitású aktív fragmenseket eredményeznek, így korlátozva a neuropatológiát (Li et al. 2011). Egy ilyen döntő állatmodell hiányának hatása van
jelentősek voltak, és súlyosan korlátozták a kísérleti tanulmányokat a sejtes és molekuláris mechanizmusok azonosításában, és hátráltatták a preklinikai fejlesztést és a nagyon szükséges terápiák tesztelését. Itt azt teszteljük, hogy a növekvő genotoxikus stressz azáltal, hogy nem csak az Atm génben, hanem a kapcsolódó Aptx génben is nullmutációkat helyez el, reprezentatívabb egérmodellhez vezet-e, amely kisagyi diszfunkciót, sorvadást és progresszív ataxia kialakulását mutatja. Az Aptx kiiktatása mellett döntöttünk, mert hiánya AT-szerű rendellenességet okoz az emberekben, az úgynevezett ataxia 1-es típusú szem apraxiával.AOA1), which does not feature A-T's other system defects that could increase the potential for prenatal lethality or early death (e.g., immunodeficiency and cancer predisposition)(Coutinho P 2002).Moreover, APTX is a phosphodiesterase involved in DNA reassembly after double-and single-stranded repair, and has a function downstream of—but not directly regulated by or related to—ATM (Gueven et al.2004; Schellenberg, Tumbale, and Williams 2015; Ahel et al.2006).We hypothesized that the functional expression of both proteins would have an additive effect and induce neurological dysfunction. Our results indeed demonstrate that mice deficient in ATM and APTX develop cerebellar dysfunction, atrophy, and progressive and profound ataxia, while mice deficient in either protein alone do not Additionally, double mutants displayed other characteristic symptoms of A-T, including defects in immune maturation and a high incidence of cancer (thymomas), making it the most representative model, from a phenotypic standpoint to date. Finally, we designed this new mouse model to test our recently developed Small Molecule Read-Through Compounds(SMRT)that enable translation through premature termination codons(Du et al.2013). Thus, we inserted a premature termination-causing nonsense mutation (103C>T) az észak-afrikai AT-betegek nagy családjában közös Atm génben (Gilad, Bar-Shira és mtsai, 1996). Ez a mutáció korai terminációs kodont (PTC) eredményez, amely normális esetben a 35. aminosav lenne, és az ATM transzláció elvesztését eredményezi. Itt beszámolunk az elvi bizonyítási kísérletekről, amelyek bemutatják, hogy az AT egérmodellbe beépített klinikailag releváns genetikai mutációk alkalmasak az átolvasási vegyületekre, és így alkalmasak az SMRT vegyületek preklinikai tesztelésére.

2.0 Eredmények
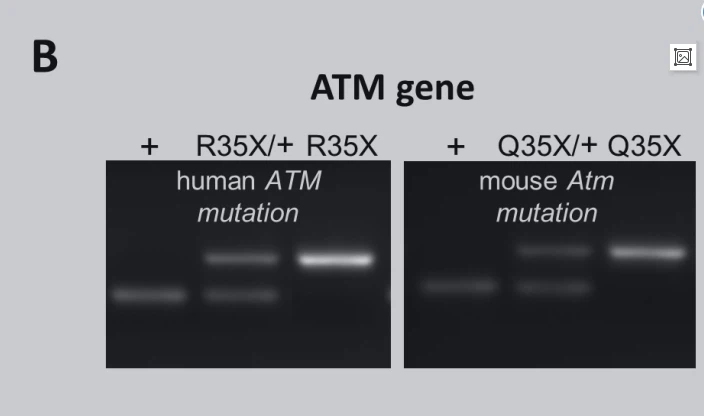
2.1 Creation of a new A-T mutant mouse model expressing a clinically relevant nonsense mutation To create a more clinically relevant mouse model of A-T we used a gateway recombination cloning and site-directed mutagenesis method to recapitulate a c.103C>T(p.R35X) mutation in the ATM gene found in a large population of North African A-T patients(Fig.1A and Methods)(Gilad, Khosravi, et al. 1996). The insertion of thymine in place of cytosine at this site in exon 3 results in a premature termination codon(PTC)-causing nonsense mutation in the ATM gene. Since the c.103C>A T mutáció eltérő PTC-ket eredményez a humán génben, mint az egér Atmgén – TGA vs. TAG, respectively—we created two different mice by exchanging the mouse Atm exon 3 with either a human or mouse exon 3 variant with the c.103C>T mutation(Fig.1B). In the human variant, a 103C>T mutation of the mouse codon, where the arginine(R) encoding codon(CGA) becomes a TGA stop codon, results in a mouse we denote as AtmR35×(officially Atm'm103cAc)rGAMag). In the mouse variant, the c.103C>A T mutáció a glutamint (Q) kódoló CAG kodont TAG stopkodonná alakítja, és Atm235×-nek (hivatalosan Atmm1.103c) time-nak jelöljük. A PTC jelenléte az ATM-expresszió elvesztését eredményezi, vagy körülbelül felére csökken a heterozigótában, amely egy normál egérmásolatot expresszál.
vagy Atm Q35v35×) (ábra vagy Atm 835×), vagy teljesen homozigótában (Atm?35×R35×Atm gén ()Atm35× plusz 1C).
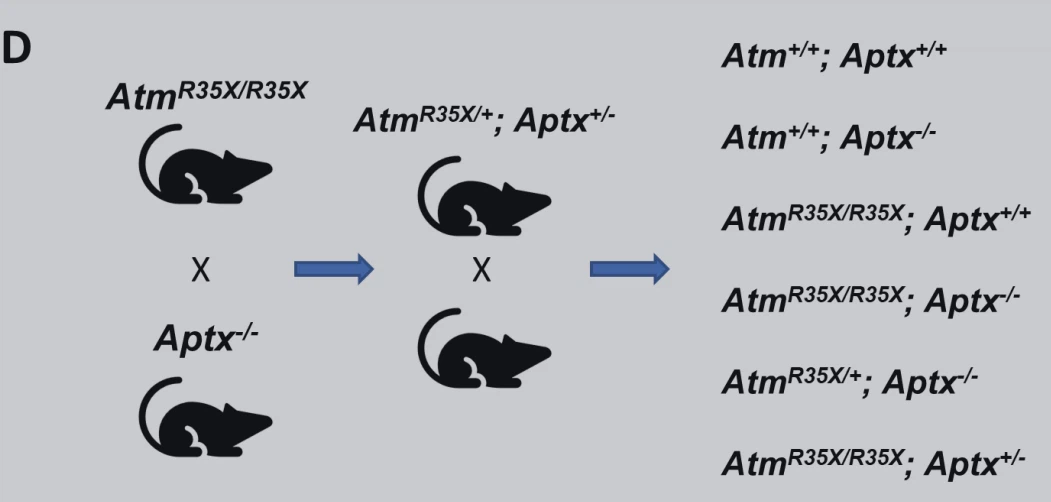
Atm35x7R35×; Aptx^ (kettős mutáns) egereket úgy hoztunk létre, hogy először egy mutáns AtmF3xR3x (kongenikus a C57BL/6J háttéren) és Aptx' (kevert C57BL/6J és 129 háttér) egereket Aptx* egerekkel kereszteztünk. F1-5 alomtárs Atm"; Aptx* egereket ezt követően keresztezték, hogy az almon belül heterozigóta Atm-et generáljanak, hogy elegendő számú kísérleti és kontroll genotípust hozzanak létre annak meghatározásához, hogy a különböző mennyiségű ATM és APTX elvesztése hogyan befolyásolja az állat fenotípusát ( 1D ábra).
A korábbi ATM-hiányos AT egérmodellekhez hasonlóan az ATM vagy APTX hiány önmagában nem eredményezett ataxiás egereket (1. és 2. videó). Azonban mindkét fehérje hiánya (Atm35k35x; Aptx') súlyos és fokozatosan ataxiás fenotípus kialakulásához vezet (1E. ábra, 3. és 4. videó).
2.2 Az ATM-hiányos egerek túlélési aránya csökkent, és magas a timomák előfordulása
Felmértük az ATM és az APTX különböző szintjét expresszáló kontroll és kísérleti egerek általános egészségi állapotát és fejlettségét (2. ábra). Azt találtuk, hogy az Atm735xR35×; Az Aptx^'egerek körülbelül 55 százalékkal lassabban nőttek, és elérték a becsült platósúlyt, amely körülbelül 35 százalékkal volt kisebb, mint a kontroll genotípusoké (log-rank, n=21 - 40,p<0.0001; fig.="" 2a).="" these="" differences="" in="" weight="" were="" a="" postnatal="" phenomenon,="" as="" no="" significant="" weight="" differences="" were="" detected="" just="" after="" birth="" (p8)="" across="" all="" genotypes(1-way="" anova,n="5" to="" 23,="" p~0.23).="" adolescent="" double="" mutant="" mice="" at="" postnatal="" day="" 45(p45)weighed="" on="" average="" 30%="" less="" than="" male="" mice="" [double="" mutant:14.4±1.0g="" (n="13)vs." wildtype:20.2±0.5="" g(n="16),"><0.0001] and="" 25%less="" in="" females="" [double="" mutant:12.7±0.6g="" (n="17)" vs.wildtype:17.0±0.2g(n="15)," test,=""><0.0001; fig.="" 1a].differences="" across="" the="" control="" genotypes="" were="" observed,="" but="" they="" were="" small="" and="" not="" consistent="" across="" time="" points="" or="" sex="" and="" therefore="" judged="" to="" not="" be="" physiologically="" relevant="" (fig.="" 2a).="" survivability="" of="" the="" atm735xr35×;="" aptx*="" mice="" was="" significantly="" reduced="" compared="" to="" atm*;="" aptx*="" mice,="" with="" 53%="" of="" mice="" still="" alive="" at="" 400="" days="" of="" age,="" compared="" to="" 97%="" of="" atm*;="" aptx*="" mice="" at="" the="" same="" time="" point="" (fig.2b).atm="" deficiency="" alone="" was="" sufficient="" to="" reduce="" survivability;="" as="" compared="" to="" atm*;="" aptx*="" mice,="" both="" atm35xr35×;="" aptx*="" and="" atm735x/r35x;="" aptx*="" mice="" had="" significantly="" reduced="" survivability="" [42%,log-rank,xu5="13.49,p=0.0002" and="" 52%,log-rank,xu,53)=""><0.0001,respectively]. no="" significant="" difference="" in="" survivability="" between="" atm-deficient="" mice="" with="" partial="" or="" complete="" aptx="" deficiency="" was="" detected="" [log-rank,="" x(2.85)="1.01,p=0.6]." conversely,="" mice="" harboring="">
least one functional copy of the Atm gene had normal survivability, regardless of whether they expressed APTX or not [log-rank, X(3 131)=3.08, p=0.4]. No significant difference between male and female mice was observed, and thus data were pooled [log-rank, p>0.4 minden páronkénti összehasonlításhoz; Fig.{2}}Fig.S1B]. Általában az ATM-hiányban szenvedő egerek harmada pusztult el a mellüregben talált, nagyméretű csecsemőmirigyrákhoz (timomához) kapcsolódó szövődmények miatt (2C. ábra). Az APTX jelenléte vagy hiánya nem befolyásolta a rák prevalenciáját, és a legalább egy Atm-átirattal rendelkező egerek rákmentesek voltak legalább P400-ig. Összességében az ATM-hiány, de nem az APTX-hiány súlyos hatással volt az egerek egészségére és túlélésére.


2.3 Mind az ATM, mind az APTX hiánya szükséges a progresszív motoros diszfunkció kialakulásához
A súlyos ataxia progresszív kialakulása az AT jellegzetessége, amely az Atm? 35/R35x; Aptx' egerek, de az általunk tesztelt többi kontroll genotípus egyike sem. Összességében azt találtuk, hogy a mozgáskoordinációs zavarok a születés után 210 és 400 nappal jelentkeznek az Atm735Xk3x-ben; Az Aptxegereket, és nem találtak bizonyítékot ataxiára az Atm vagy Aptx gén legalább egy másolatával rendelkező egerekben (3A, B ábra). A függőleges pólus teszthez Atm735xR3x×; Az Aptx' egereknek kétszer annyi időbe telt leereszkedni P400-nál, mint az Atm*;Aptx*,Atm*; Aptx',Atm735xR35×; Aptx* vagy Atm35×*; Aptx' egerek [Hím: 29,1±0,9s(n=3) vs.7,5±0,4s(n=12),12,5±2,5s(n=9),9,2±0,9s (n=10),8,6±0,9s(n=11),1-utas ANOVA,F4.40=19.9,p<0.001;female:19.0±4.0s(n=4)was.7.5±0.4s(n=12),7.8±0.4s(n=10),10.5±1.2s(n=6), 8.2±0.5="" s(n="8),1-way" anova,="" f4,="" 35="13.9,"><0.0001]. an="" examination="" of="" gait="" indicated="" thatatm?35×r35×;="" aptx^="" mice="" at="" p400,="" but="" not="" p210="" need="" additional="" stabilization="" during="" ambulation,="" as="" they="" spend="" twice="" as="" much="" time="" with="" 3="" paws,="" rather="" than="" the="" normal="" 2,="" in="" contact="" with="" the="" ground="" as="" they="" walk="" across="" the="" gait="" analysis="" platform="" [male:="" 56.2="" vs.="" 26.4="" to="" 32.2="" %,1-way="" anova,="" f4.54)="14.3,"><0.0001; female:="" 58.4="" vs.18.9="" to="" 28.8="" %,1-way="" anova,="" f3.178)="95.5,"><0.0001; fig.3b].="" atm35xr35×;="" aptx'="" also="" display="" a="" slower="" cadence="" and="" average="" speed="" across="" the="" platform="" compared="" to="" all="" other="" genotypes="" at="" p400="" [cadence,="" male:9.5="" vs.="" 13.3="" to="" 15.9="" steps/s,="" 1-way="" anova,="" f3.204)=""><0.0001;female: 9.1="" vs.14.2="" to="" 15.9="" steps/s,1-way="" anova,f,204)="39.7,"><0.0001;speed, male:8.8="" vs.22="" to="" 26="" cm/s,1-way="" anova,="" f4.50)=""><0.0001;female: 58.4vs.18.9="" to="" 28.8="" cm/s,1-way="" anova,="" f3.178)="39.7,"><0.0001;fig.3b; fig.3-fig.="" s1].="" this="" difference="" in="" speed="" and="" cadence="" is="" unlikely="" to="" be="" caused="" by="" the="" animal="" size,="" as="" there="" are="" no="" significant="" differences="" in="" these="" parameters="" at="" earlier="" time="" points="" when="" the="" difference="" in="" size="" is="" significant(fig.2a).="" these="" observations="" across="" the="" two="" behavioral="" tests="" were="" found="" in="" both="" male="" and="" female="" mice="" at="" each="" of="" their="" respective="" time="" points,="" consistent="" with="" the="" lack="" of="" sex="" differences="" observed="" in="" a-t="" patients.="" we="" further="" examined="" behavioral="" differences="" between="" the="" atm735xr35x;="" aptx'="" and="" atm*;="" aptx*="" mice="" using="" a="" standardized="" set="" of="" experimental="" procedures="" used="" to="" phenotype="" genetically="" modified="" mice="" (i.e.,="" sherpa;="" fig.3c;="" fig.3-fig.s1)(rogers="" et="" al.1997).="" we="" first="" detected="" differences="" in="" motor="" function="" at="" p8,="" where="" atm35xr35×;aptx'="" mice="" took="" 3-4="" times="" longer="" on="" average="" to="" right="" themselves="" compared="" to="" atm*;aptx*mice="" [male:="" 6.4±1.1="" s(n="24)vs.1.5±0.1" s(n=""><0.0002;female: 11.1±1.9s(n="21)was.2.4±0.3s" (n=""><0.0002;fig.3c bottom].at="" 30="" days="" of="" age,="" we="" detected="" x;="" aptx*="" and="" atm*+;="" aptx**="" mice="" in="" behavioral="" tests="" that="" significant="" differences="" between="" atm735×r35×;="" qualitatively="" measured="" body="" position="" and="" spontaneous="" activity(fig.3c).="" striking="" differences="" in="" atm35×r35×;="" aptx^'="" compared="" to="" atm*;="" aptx*"="" mice="" were="" observed="" at="" p400,="" especially="" for="" behaviors="" related="" to="" movement,="" including="" locomotor="" activity,="" body="" position,="" and="" gait(fig.3c).="" the="" results="" from="" this="" battery="" of="" tests="" demonstrate="" that="" atm35×r35x;="" aptx*mice="" develop="" a="" severe="" change="" in="" behavior="" by="" p400,="" consistent="" with="" purely="" visual="" observations="" of="" significant="" motor="" coordination="" deficits="" in="" the="" mice="" up="" to="" this="" time="" point.="" importantly,="" we="" do="" not="" find="" any="" significant="" differences="" between="" the="" other="" control="" genotypes,="" including="" atm35×;="" aptx*="" mice="" that="" express="" at="" least="" some="" atm="" but="" no="" aptx="" protein="" (fig.="">

2.4 Az ATM- és APTX-hiányos Purkinje neuronok membrán- és szinaptikus tulajdonságai megzavartak
A Purkinje neuronok (PN) a kisagykéregben található kulcsfontosságú neuronális altípusok. Jelentős belső ingerlékenységet mutatnak, és spontán módon aktiválják az akciós potenciálokat, lényegesen nagyobb sebességgel, mint a legtöbb más agyi neuron (sok esetben 50-100 Hz-cel nagyobb). Tevékenységük a kisagyi sejtmagok idegsejtjeinek tónusos gátlásán keresztül alakítja a kisagyi teljesítményt, amelyek az előagyban, az agytörzsben és a gerincvelőben található motoros koordinációs központokba nyúlnak be. A cerebelláris PN diszfunkció az ataxia számos formájával jár együtt, és az AT-ben is szerepet játszik (Hoxha et al.2018: Cook. Fields. and Watt 2021: Shiloh Aptx*-X/R35X.2020). Ezért megvizsgáltuk, hogy az Atm' kisagyban a PN-ek elektrofiziológiai tulajdonságai abnormálisak-e. Mivel a PN kiindulási aktivitását és a bemenetre adott válaszkészséget a passzív és aktív membrántulajdonságok alapvonal-készlete közvetíti (4. ábra), közvetlenül rögzítettük és összehasonlítottuk a PN-ek membrántulajdonságait az Atm35XR35×-ből gyűjtött akut kisagyi metszetekben; Aptx* és Atm*; Aptx* egerek (P350-400). Az Atm35xR35×-ről rögzített PN-ek; Az Aptx egerek szignifikánsan "szorosabb" membránokkal rendelkeztek, és nagyobb membrán bemeneti ellenállást (Rm) mutattak, mint az Atm-ből származók; Aptx* egerek [47,7±5,6 (n=15) vs.
30.2±1,47(n=23)MQ, t-teszt,p-0.008; 4B. ábra], és gyorsabb membránidőállandót() jelenített meg [3,6±0,4(n=15) vs.5,1±0,3(n=23) ms, t-teszt, p=0 0,009;4B ábra]. Ezek az eredmények azt mutatják, hogy az Atm35x/35x;Aptx^PNs teljes membránkapacitása (Cm=t/Rm) jelentősen csökken [98,25±19,23(n=15) vs. 175,6± 12,67 (n) =23)pF,t-teszt,p=0.0025;4B. ábra].Celláris szinten ez arra utal, hogy az ATM- és APTX-hiányos PN-ek kisebb (azaz csökkentett területtel rendelkeznek) vagy vékonyabb membránok
mint a vad típusú PN-é, fejlődési hiányra vagy neurodegeneratív folyamatra utaló eredmény; Aptx/-and (DellOrco et al.2015). Ezt követően felmértük a PN-ek belső ingerlékenységét AtmR35xR3x-ben;
Atm*;Aptx* egerek a PN akciós potenciál (AP) keletkezésének és dinamikájának vizsgálatával. Jelentős hiányosságokat figyeltek meg a PN-ek azon képességében, hogy az áraminjektálás hatására folyamatosan tüzeljenek az Atm35×3x;Aptx^ egerekben (4C. ábra). Ezek a hiányosságok a kiváltott akciós potenciálok amplitúdójában, küszöbértékében és területének jelentős perturbációjával jártak együtt [amplitúdó: 66,2± 0.7 (n=14) vs. 72,1±1,4 (n=13)AmV,t-teszt,p=0.003;küszöb:-55.2±1,5vs.-48. 61±1,9 mV, t-teszt, p=0,0196; terület:17,96±0,6vs.
20,63±1,0 mV*ms, t-teszt, p=0,048; 4C ábra]. Ezek a kísérletek együttesen a PN fiziológiai tulajdonságainak jelentős zavarait mutatják be, amelyek valószínűleg megzavarják az At/mR35×R35× kisagy normális működési képességét; Aptx egerek.
Ezt követően megvizsgáltuk, hogy az AtmR35xR3sx külső és/vagy szinaptikus PN tulajdonságait is befolyásolták-e. Aptx* egerek. Először megvizsgáltuk a spontán gerjesztő posztszinaptikus áramokat (iPSC), amelyeket szemcsesejt-PN szinapszisok (azaz párhuzamos szálbemenetek) generálnak. Az UPSC méretében nem észleltünk különbséget, ami azt jelzi, hogy a szemcsesejt axonterminálisainak (azaz párhuzamos rostok) funkciója viszonylag normális volt az AtmR35KR35X-ben; Aptx'cerebellum[18.92±1.3(n{{10}}) volt. 23,4±3,3(n=11)pA,t-teszt,p=0.477;4D ábra](Yamasaki, Hashimoto és Kano 20{{5{{58} }}}6). Az sEPSC-frekvencia azonban jelentősen megnőtt, ez a jelenség vagy a szinapszisok teljes számának növekedésével, a szinaptikus vezikulák könnyen felszabadítható készletének növekedésével vagy a neurotranszmitterek valószínűségének növekedésével magyarázható. fAtmR35XR35X felszabadulása PN-ekben; Aptx'egerek [18,75±2,8 Hz(n=11) vs. 11,4±1.0Hz(n=11), t-teszt, p=0.{{ 69}}47; 4D ábra]. Ezt követően a kiváltott szinaptikus felszabadulást és a rövid távú plaszticitást vizsgáltuk úgy, hogy egyidejűleg rögzítettük a PN-eket, és elektromosan stimuláltuk a szemcsesejteket (azaz párhuzamos rostok) vagy az inferior olivárium (azaz mászószál) axonokat páros impulzuslökettel (2-). impulzusok, 50 ms távolságra egymástól). A párhuzamos szálak szinaptikus tulajdonságai normálisnak bizonyultak, és nem mutattak szignifikáns különbséget a kiváltott EPSC várható rövid távú facilitációjában (Atluri és Regehr 1996), sem a félszélességben és a csillapítási időállandóban [PPR: 1,3±0. 03 (n=10) vs. 1,4±{{90}}.{{1{{1{{106}}5}}1 }}5(n=13),t-teszt,p=0.162;félszélesség:3.9±0.6 vs.4.9±0.4 ms,t -teszt,p=0.175;időállandó: 3.5±0.5 vs.4.7±0.4 ms,t-teszt,p=0.054;ábra. 4E]. Összehasonlításképpen, a rost-PN szinaptikus válaszreakciókat találtuk, amelyek általában párimpulzus-depressziót mutatnak (Hansel és Linden 2000), t szignifikánsan nagyobb mértékben csökkentik az Atm/3338/R35X; Aptx egerekben [PPR: 0,6±0,03 (n=6) vs.0,7±0,02(n=9),t-teszt,p=0.03;4F. ábra]. Az előhívás teljes szélessége és csillapítási időállandója az áramok is kisebbek voltak [félszélesség: 2,3±0,6(n =6).3,0±0,2(n=9) ms,t-teszt,p=0.004;időállandó(gyors) :1,1±0,14 vs. 2,9±0,4 ms, t-teszt, p=0,001]. Míg ezeket az eredményeket preszinaptikus hiány okozhatja, például a húgyhólyag-raktárak csökkenése a mászószál axonterminálisában, az EPSC kezdeti nagysága nem változott [2,4±0,4(n=6) vs. 1,9 ±0,2 nA (n=9), t-teszt, p=0.3] inkább belső hiányra utal, mint például az endoplazmatikus retikulumból származó Ca2*-beáramlás csökkenése, ami jelentősen befolyásolhatja a hosszú -termi szinaptikus plaszticitás kritikus kisagyi működés szempontjából (Hoxha et al. 2018; Kano és Watanabe 2017). Összességében az itt megfigyelt passzív és aktív PN-tulajdonságok zavarai valószínűleg jelentős cerebelláris diszfunkcióhoz vezetnek az AtmR35X/R35X-ben; Aptx' egerek.
2.5 Az ATM és APTX hiány a PN neurális aktivitásának progresszív perturbációját okozza, ami a dendritekhez kapcsolódikzsugorodó és általános cerebelláris atrófia Decreased rates of spontaneous PN action potential firing, which can be indicative of PN dysfunction, have been observed in several mouse models of ataxia, including spinocerebellar ataxias (SCA)2,3,5,6,13,27, several models of episodic ataxia (e.g., leaner, ducky, and tottering), and autosomal- recessive spastic ataxia of the Charlevoix-Saguenay (Hourez et al.2011; Hansen et al. 2013; Dell'Orco, Pulst, and Shakkottai 2017; Kasumu and Bezprozvanny 2012; Liu et al.2009; Perkins et al.2010; Shakkottai et al. 2011; Jayabal et al.2016; Stoyas et al.2020; Hurlock, McMahon, and Joho 2008; Shakkottai et al.2009; Bosch et al.2015; Walter et al.2006; Alvina and Khodakhah 2010; Ady et al.2018; Lariviere et al.2019; Cook, Fields, and Watt 2021). We, therefore, used this biomarker to characterize the progression of PN perturbation in Atm35XR35; Aptx'mice and assess whether deficits were restricted to ATM- and APTX-deficient mice, consistent with the behavioral results(Fig.2,3). We additionally examined whether decreased PN activity differed across the cerebellum, as anecdotal clinical pathology reports suggest degeneration may occur asymmetrically across the cerebellum, with the anterior and posterior vermis and middle cerebellar hemispheres affected the most, although no systematic analysis has been performed, and the consistency of results across patients is highly variable (Verhagen et al.2012; De Leon, Grover, and Huff 1976; Amromin, Boder, and Teplitz 1979; Monaco et al.1988; Terplan and Krauss 1969; Strich 1966; Solitare 1968; Solitare and Lopez 1967; Aguilar et al. 1968a; Paula-Barbosa et al. 1983). Using extracellular recording methods in the acute slice, we recorded spontaneous action potentials Aptx^ and 3 others from 3,300 PNs(Fig. 4G) across 188 animals, encompassing Atm35×R35×; genotypes at four different time points (P45, 120,210, and 400). We visually selected "healthy cells (see Methods) located deeper in the slice, that consistently fired during the extent of the 60-second recording period. Qualitatively, tissue and cell quality did not visually differ across genotypes under DIC microscopy. Cells were sampled in a distributed fashion across the lateral, intermediate, and medial (vermis)cerebellum of each mouse to assess whether changes in PN firing activity were ubiquitous or anatomically restricted. Regions were segregated based on gross anatomical domains in the mouse defined by natural anatomical boundaries (e.g., foliation) and their general connectivity with different regions of the nervous system (e.g., forebrain, brainstem, etc.)(Voogd and Glickstein 1998). We found that a complete deficiency of both ATM and APTX, consistent with the behavioral results, was necessary to produce a significantly reduced spontaneous PN firing frequency (Fig. 4G, H). Although the trend of slower PN firing rates were observed across most regions of the cerebellum, some subregions appeared to be less or minimally impacted, including several areas of the lateral cerebellum, including the paraflocculus, paramedian, and crus I and Ⅱ (Fig. 4-fig. S2). Significant age-dependent changes in firing frequency were also commonly observed in AtmR35XR35X; Aptx'mice(Fig. 4H), with the most significant decline occurring betweenP120 and 210 [medial: 50.3±2.4Hz(n=61)vs. 36.9±2.2Hz(n=31),t-test,p=0.0006].No significant difference in PN firing frequency was detected between male and female mice within each genotype, thus the data were pooled (2-way ANOVA, p>0.3 minden páronkénti összehasonlításban; ábra 4-ábra S3). Az öröklődő ataxia számos egérmodelljén végzett korábbi tanulmányok, beleértve az epizodikus ataxiát és a spinocerebellaris ataxia számos változatát, azt találták, hogy a PN tüzelés fiziológiai zavara nemcsak gyakoriságát, hanem szabályosságát is megváltoztatja (Kasumu és Bezprozvanny 2012; Jayabal et al. 2016; Stoyas et al. 2020; Cook, Fields és Watt 2021). Összehasonlítottuk a variációs együtthatót (CV) és a szomszédos intervallumok variabilitását (CV2) az AtmR35X/R35X között; Aptx/ és kontroll egerek (4-ábra S4, S5). Nem észleltek különbséget ezekben a paraméterekben a nem, az életkor vagy a genotípus között. A viselkedési eredményekkel összhangban kisagyi diszfunkciót csak az AtmR35XR35X-ben találtak; Aptx'egerek, amelyekben ataxia alakult ki, és nem az ATM vagy APTX részleges vagy teljes expressziójával rendelkező egerekben.


A 2,5 ATM és APTX hiány kisagyi sorvadást vált ki
In A-T patients, ataxia is usually detected between1 two 2-years of age and is associated with little to no cerebellar atrophy (Tavani et al. 2003; Taylor et all. 2015). Significant structural changes and atrophy are usually first detected via neuroimaging between 5 and to 10-years of age (Demaerel, Kendall, and Kingsley 1992; Tavani et al. 2003). Postmortemclinical histopathology in A-T patients points to significant changes in PN morphology and density, however, these reports primarily detail patients at late stages of the disorder, and the relationship between the severity of PN pathology and ataxia is not clear (Verhagen et al. 2012; De Leon, Grover, and Huff 1976; Amromin, Boder, and Teplitz 1979; Monaco et al. 1988; Terplan and Krauss 1969; Strich 1966; Solitare 1968; Solitare and Lopez 1967:Aguilar et al. 1968a; Paula-Barbosa et al. 1983; Gatti and Vinters 1985). In the Atm735X7k3×; Aptx^ mice, we found the gross size of the cerebellum to be normal early in life, but significant atrophy developed as the severity of ataxia increased (Fig.5A). At early stages(P45-P210), the size of the cerebellum in Atm3xR35×; Aptx^ mice did not differ from mice with at least one copy of the Atm gene(2-way ANOVA, Fa.s52)=1.0, p-0.4). However, by P210, the overall size of the cerebellum in Atm735XR35×; Aptx* mice was significantly reduced(1-way ANOVA, F(3,37= 1.4,p=0.3), with the degenerative process continuing to at least the last time point investigated (P460). To rule out the possibility that reduced cerebellar size was related to the smaller stature of Atm735xR35×; Aptx" mice, we examined, animal weight and cerebellar size and found no correlation [Pearson's correlation, p>0.3 mind a 4 genotípusra a P460-nál, n=10-től 20-ig]. Továbbá azt találtuk, hogy a kisagy mérete nem különbözött a hímek és az átlagosan 22 százalékkal kisebb nőstény egerek között a genotípusok között ebben az életkorban [2-way ANOVA, F(2. 153)=1.9, p. =0.2]. Ezért a cerebelláris neurodegeneráció az Atm35XR35×-ben; Az Aptx*egerek, amelyek a P120 után kezdődnek, összefüggésben állnak az ATM és az APTX hiányával. Azt találtuk, hogy a cerebelláris atrófia a molekularéteg szélességének szelektív csökkenésével jár együtt, ahol a PN dendritek találhatók (5B. ábra). A kisagy bruttó méretének, a PN tüzelési gyakoriságának és viselkedésének időbeli változásaival összhangban az ML szélesség Atm35×R35X-ben; Az Aptx* egerek normálisak voltak a fiatalabb egereknél, de a szélességük fokozatosan csökkent, ahogy az ataxia súlyossága 【P400∶120,2±2,1 μm (n=5) vs. 140,2±4,8 μm(n=5 {31}}way ANOVA,Fu42=45.04, p<0.0001;fig.5b, fig.5-figs.s1a】.in="" contrast,="" no="" difference="" in="" the="" width="" of="" the="" granular="" cell="" layer(gcl)across="" age="" was="" observed="" in="" the="" atm35xr3x;="" aptx*mice="" 【p400∶135.5±2.4="" μm(n="6)v.127.5±4.3" μm(n="5),2-way" anova,fu="" 42="3.3,p=0.08;Fig.5B," fig.5-figs.s1a].="" cerebellar="" atrophy,="" however,="" was="" not="" due="" to="" pn="" cell="" death,="" as="" pn="" density="" did="" not="" significantly="" differ="" between="" atm735×r35x;="" aptx'="" and="" atm*;="" aptx*="" mice="" [p400:4.5="" ±0.3(n="9)vs.4.5±0.2(n=7)PNs/4000" μm²,welch's="" t-test,="" p="0.9;Fig.5C," d="" fig.5-figs.s1b】.moreover,="" we="" found="" no="" evidence="" from="" immunohistological="" experiments="" for="" increased="" levels="" of="" aptx"-="" mice="" (fig.5-figs.s2).="" at="" the="" programmed="" cell="" death="" or="" microglial="" activation="" in="" the="" atm?35x/r35x="" anatomical="" level,="" we="" found="" pathological="" changes="" in="" pn="" morphology,="" as="" the="" somatic="" size="" was="" reduced(15.3±0.3(n="5)vs.17.8±0.1(n=5)μm," welch's="" t-test,="" p="0.0004;" fig.5e)and="" the="" primary="" and="" secondary="" dendrites="" were="" abnormally="" large="" in="" caliber="" in="" the="" atm35xxr35x;="" aptx'mice="" (3.1±0.2(n="6)vs.2.8±0.1" (n="6)μm," welch's="" t-test,="" p-0.003;="" fig.5f,="" fig.5-figs.s2c).="" overall,="" we="" found="" a="" good="" correlation="" between="" the="" abnormal="" structural="" and="" electrophysiological="" properties="" of="" the="" cerebellum="" and="" the="" progression="" of="" motor="" deficits.="" 2.6="" differential="" disruption="" of="" thymocyte="" development="" in="" atm-deficient="" vs.="" aptx-deficient="">
Az immunhiányhoz kapcsolódó krónikus szinopulmonális fertőzések az egyik vezető halálok az AT-betegeknél (Morrell, Cromartie és Swift 1986; Bhatt és Bush 2014). Az immunhiány összefüggésben áll a B- és T-limfociták képződésének hiányával, amelyek az antigénreceptor-gén-átrendeződési folyamatok hibáihoz kapcsolódnak a sejtek csontvelőben, illetve csecsemőmirigyben történő termelődése során (Staples et al. 2008). Az érett limfociták számának ebből eredő hibái közé tartozik a CD4t helper T-sejtek és a gyilkos CD8*T-sejtek számának csökkenése (Schubert, Reichenbach és Zielen 2002). Ezért megvizsgáltuk az Atm35xR35× T-sejtek százalékos arányát a perifériás vérben és a különböző szubpopulációkat a csecsemőmirigyben; Aptx*' egerek T-sejt antigénreceptor (TCR) és CD4/CD8 társreceptor expressziót használva. A perifériás vérben a CD3*T-sejtek összfrakciójának szignifikáns csökkenését figyeltük meg csökkent vagy hiányzó ATM-expressziójú egerekben a vad típusú egerekhez képest (6. ábra). Ezt a csökkenést tovább fokozta az APTX egyidejű hiánya. Az ATM és APTX hiányok több mint 65 százalékkal csökkentették a T-sejtek számát a perifériás vérben a vad típusú kontrollokhoz képest. Az APTX-hiány hatása additív volt az ATM-hiányéhoz, ami arra utal, hogy e két fehérje eltérő hatásmechanizmusa van a T-sejt-generációban. A perifériás vérben a T-sejtek százalékos arányának csökkenése leginkább a CD4 plusz segítő T-sejt populáció csökkenésével volt összefüggésben (6B. ábra). Érdekesség, hogy a CD8 plusz T-sejtek aránya csak az AtmR35X/R35×-ben nőtt; Aptx* egerek (6B. ábra). Ismét megfigyeltük az ATM- és APTX-hiányok eltérő hatását, amint azt ezeknek a mutációknak a teljes T-sejt-frakcióra gyakorolt hatásainál láttuk. Tekintettel a T-sejt-populációk csökkenésére a vérben, a következő lépésben a T-sejtek fejlődését értékeltük a csecsemőmirigyben. Ebben a szervben a csontvelőből származó T-sejt progenitorok TCR génátrendeződésen mennek keresztül, amelyet az MHC restrikciós pozitív szelekció és az autoreaktív klónok negatív szelekciója követ. A timociták fejlődésének fázisai követhetők a CD4 és CD8 expresszió timocitákban történő monitorozásával. Ennek a fejlődési programnak a progressziója a kettős negatív (CD4 CD8) timocitáktól a kettős pozitív (CD4*CD8) timocitákig, majd az egyszeresen pozitív (CD4* vagy CD8*) timocitákig terjed. Ezenkívül a kettős negatív stádiumon belül négy különböző alpopuláció azonosítható a CD25 és CD44 expressziója alapján, ezek a DN1 (CD44*CD25), DN2 (CD44*CD25*), DN3 (CD44 CD25*) és DN4 (CD44 fok CD25) (Germain 2002). A timociták fejlődése során a génátrendeződés kétszer fordul elő – egyszer a kettős negatív timocita stádiumban a CD25*CD44 stádiumban (Krangel 2009), majd ismét a kettős pozitív timociták stádiumában, mielőtt külön CD4* és CD8t egyetlen pozitív populációkká fejlődnének (Livak et al. 1999). Az ATM-hiányt az egereknél tapasztalt mindkét átrendeződési roham hibáihoz kapcsolták (Vachio 2007, Hathcock 2013). Ezért összehasonlítottuk a csecsemőmirigyben a különböző fejlődési sejtfelszíni markereket expresszáló sejtek arányát ATM-hiányos és kontroll egereinkben (7. ábra). AtmR35xR35×; Aptx és Atm35×; Aptx^, de nem AtmR35XR35; Az Aptx* egerekben szignifikánsan megemelkedett a CD44*CD25, CD44*CD25t és CD44 CD25* sejtek aránya a vadtípushoz képest (7A. ábra). Úgy tűnik, hogy ezek a megnövekedett arányok részben a CD44 CD25t sejtek CD44 CD25 kettős negatív sejtekké való érésének akadályozásának tudhatók be. az Atm735xR35×-ből származó CD44 CD25 sejtek frakciójaként; Aptx'and Atm35× plus ; Az Aptx'egerek szignifikánsan alacsonyabbak, mint a vad típusú (7A. ábra). Érdekes, hogy az APTX-hiány önmagában volt a legnagyobb hatással a DN4-sejtek elvesztésére, ami arra utal, hogy az APTX-hiány, nem pedig az ATM-hiány felelős ezért a hatásért. Tudomásunk szerint ez a megállapítás először vonja be az APTX-et génátrendeződésben a TCR rekombináció folyamata során. Ezután megvizsgáltuk a CD4*CD8t timociták arányát a CD4tCD8 és CD4CD8 plusz egyszeresen pozitív timocitákhoz viszonyítva ebben a négy különböző törzsben. A vérben és a korábbi vizsgálatokban szerzett eredményeinkkel összhangban azt találtuk, hogy az ATM-hiányos egerek, de nem a kontrollegerek, csökkent CD4*CD8 és CD4CD8* egyedi pozitív timociták expressziót mutattak (7B. ábra). Ezek az eredmények alátámasztják az ATM szerepét a TCR a/δ gén átrendeződésében a timociták fejlődése során (Bredemeyer et al. 2006), amely szerep független az APTX szerepétől a timociták korai érésében.

2.7 Az átolvasási molekulák felülmúlják a PTC-t az ATM-expresszió helyreállítása érdekében
A klinikailag releváns nonszensz mutáció Atm génbe történő beillesztésének elsődleges indoka az volt, hogy létrehozzunk egy egeret, amely alkalmas egy új SMRT-vegyületkészlet kritikus preklinikai tesztelésére. Korábban kimutattuk, hogy az SMRT vegyületek visszaállítják az ATM fehérje termelődését AT betegektől származó limfoblasztoid sejtvonalakban azáltal, hogy legyőzik a nonszensz mutációk által okozott korai terminációs kodonokat (PTC) (Du et al. 2013). Annak bizonyítására, hogy ez az új AT állatmodell alkalmas az SMRT vegyületek tesztelésére, úgy döntöttünk, hogy közvetlenül megvizsgáljuk az ATM-expresszió helyreállítására való képességüket egy olyan explantációs megközelítés segítségével, amely megkerüli az in vivo bejuttatással kapcsolatos kihívásokat (pl. biológiai hozzáférhetőség, szállítási mód stb.). Az ATM expresszióját a lépből, ahol az ATM általában magas szinten expresszálódik, és a kisagyban, a rendellenesség kulcsfontosságú célszövetében mértük. Kitettük ezeket a homozigóta Atm?35×-ből és Atm-ből gyűjtött explantátum szöveteket? 35 egeret SMRT-vegyületjelölttel (GJ103) vagy olyan aminoglikoziddal, amelyről korábban ismert volt, hogy átolvasási tulajdonságokkal rendelkezik (G418), majd immunblottal mértük az ATM-expressziót, hogy értékeljük a helyreállítást. Mindkét típusú ATM-hiányos egerben az ATM-expressziót következetesen helyreállította a lépben és a kisagyban mind a G418, mind a GJ103 (8. ábra). Ezek az eredmények azt mutatják, hogy SMRT-vegyületeink lehetővé teszik a PTC-ket okozó 3 lehetséges nonszensz mutáció közül legalább 2 átolvasását, és megalapozzák az in vivo hatékonysági tesztelést a következő vizsgálatokban.
