A veseátültetés túlélésének előrejelzésére szolgáló kockázati index kidolgozása és érvényesítése: A veseátültetés kockázati indexe
Mar 04, 2022
Bevezetés
Veseátültetésjobb életminőséget és jobb túlélést kínál másokhoz képestvesehelyettesítő terápia módozatai [1]. Az egészségügyi rendszerek azonban világszerte küzdenek azért, hogy áthidalják a növekvő szakadékot a magas kereslet közöttveseátültetésekés a korlátozott kínálat. Az egyik stratégia az irányításvesegraftokat a leghosszabb élettartamú recipiensekre helyezzük, ezáltal csökkentve mind a graft meghibásodását, mind a működő graft miatt elhunyt betegek számát [2]. A graft kudarcát a transzplantációt megelőzően előrejelző kockázat-előrejelző modellek klinikai támogatást nyújtanak a leghosszabb élettartamú recipiensek és az alacsony kudarc kockázatával rendelkező allograftok összeegyeztetésének komplex döntéshozatalában. Több is vanveseaz irodalomban olyan graftkockázat-előrejelzési modellek, amelyek segítették a bizonyítékokon alapuló orvosi döntéshozatalt a klinikai gyakorlatban [3, 4]. AzVeseDonor Risk Index (KDRI), amelyet Rao et al. 2009-ben széles körben elterjedt a klinikai döntéshozatalban [3], és az Egyesült Államokban használjákVeseElosztási rendszer [5]. A Te C-index, amely azt jelzi, hogy egy előrejelzési modell képes megkülönböztetni a hosszabban túlélő graftokat a rövidebb túlélő graftoktól, azonban 0,62, egy érték, amely csak ésszerű megkülönböztetést jelez. A statisztikákon vagy a gépi tanulási módszereken alapuló új megközelítések pontosabb előrejelzéseket adhatnak [6].
A gépi tanulás gyorsan fejlődött az elmúlt évtizedekben, és már alkalmazzák az orvosi diagnosztika egyes területein [7]. Csoportunk nemrégiben végzett szisztematikus áttekintése rávilágított a gépi tanuláson alapuló kockázat-előrejelző modellek szerepére az orvosi döntéshozatalban, ami pontosabbá teszi.veseátültetéskimenetel előrejelzései [8]. Áttekintésünk azonban megállapította, hogy az Egyesült Államokban kifejlesztett modellektől eltérő modelleket általában 1,{2}} betegnél kisebb mintákból származtattak. Továbbá az eddig kifejlesztett gépi tanulási modellek egyike sem modellezte az eseményig eltelt időt (túlélést) [8]. Ehelyett a legtöbben azt a bináris eredményt használták, hogy nem sikerül-e vagy sem. A bináris megközelítés azonban az egy évet túlélő graftot egyenlően kezeli a két éven belül meghibásodott grafttal, ami a páciens és az egészségügyi rendszer szempontjából jelentősen eltérő kimenetelű. Ezek a modellek nem veszik figyelembe a nyomon követési veszteséget. Ezért az eseményhez kapcsolódó idő dinamikájának beépítése az előrejelzési modellbe klinikailag és gazdaságilag fontos további információkhoz jut [9]. Célunk az volt, hogy statisztikai és gépi tanulási prediktív modelleket fejlesszünk ki és validáljunk az elhalt donor utáni graft meghibásodásának előrejelzésére.veseátültetés,az eseményig tartó időadatok felhasználásával egy nagy nemzeti adatkészletben Ausztráliából.
Kulcsszavak:Kockázat-előrejelzés, gépi tanulás, graft-elégtelenség, veseátültetés, vese
MódEnnek a tanulmánynak a protokollját szakértői felülvizsgálták és közzétették [10]. Röviden, három gépi tanulási modellt (Túlélési fa[11], Véletlen túlélési erdő[12] és Túléléstámogató vektorgép[13]) és egy hagyományos regressziós (Cox-regresszió[14]) modellt az eseményig eltelt idő (túlélési idő) modelljére. generált. Ezt a tanulmányt az egyéni prognózis vagy diagnózis többváltozós előrejelzési modelljének (TRIPOD)[15] transzparens jelentésének módszertanával számolták be. A vizsgálati kohorsz Az adatforrás Ausztrália és Új-Zéland Dialízis és Transzplantációs Nyilvántartása (ANZDATA)[16]. Összegyűjti és beszámol a dialízis prevalenciájáról, előfordulásáról és eredményeiről, illveseátültetésbetegek egész Ausztráliában. Az adatkészlet 7365 donor és recipiens jellemzőket tartalmazottvesecsak elhunyt donorok átültetése 2007. január 1. és 2017. december 31. között Ausztráliában.

A CISTANCHE JAVÍTJA A VESE-/VESEBETEGSÉGET
EredményAz elsődleges eredmény a transzplantáció meghibásodásának ideje volt, a transzplantáció időpontjától kezdődően. Azok a betegek, akik egy működő grafttal haltak meg, bekerültek a listába, és haláluk időpontjában cenzúrázták őket. A vizsgált időszak végén működő grafttal rendelkező betegeket december 31-én, 2017-én jogszerűen cenzúrázták. Hatvanöt beteg (0,9 százalék) elveszett a nyomon követés miatt, és az utolsó ismert követési időpontjukon cenzúrázták őket. Független változók Célunk egy kockázati index kidolgozása volt a transzplantáció előtti döntéshozatalhoz, ezért csak a transzplantáció előtt rendelkezésre álló és az ANZDATA-ban közölt változókat használtuk minden betegcsoportra vonatkozóan. Összesen 67 lehetséges független változót azonosítottak, mind a recipiens, mind a donor jellemzőit[17].
Modellfejlesztésszekvenciális folyamat volt a következő öt lépésből: adat-előkészítés, az adathalmaz felosztása betanítási és érvényesítési adatkészletekre, változókiválasztás, modell betanítás és modellértékelés (1. ábra).
1. lépés: Adat-előkészítés A modellfejlesztés előtt az adatok feldolgozása a hiányzó értékek kezelésével, a kategorikus változók álkódolásával és a folytonos változók skálázásával történt. Az adathalmaz közel 500,{2}} adatpontot tartalmazott (7365 beteg × 67 független változó), és az adatpontok 2,5 százaléka hiányzott. A legtöbb változóból (64 százalék) kevesebb mint 1 százalék hiányzott. A hiányzó értékekkel rendelkező változók esetében többszörös imputációt alkalmaztak 14 kategorikus változóhoz és 17 folytonos változóhoz véletlenszerű hot deck-el és osztályozási és regressziós fákkal (CART) az R-csomag „szimuláció”[18] használatával, 7365 beteg teljes adatkészletével. Szakértői vélemény alapján 13 kategorikus változó hiányzó értékéhez külön „hiányzó” kategóriát rendeltünk, hogy elkerüljük az adatok elvesztését. A numerikus független változókat min-max skálázással normalizáltuk, hasonló skálára konvertálva őket a változók közötti összehasonlítás egyszerűsítése érdekében[19]. A kategorikus változókat névleges kategóriákba kódoltuk. Dummy kódolás után a független változók száma összesen 98 volt.
2. lépés: Képzési és érvényesítési adatokAz adatkészletet véletlenszerűen két részre osztottuk: egy tanítási adatkészletre és egy érvényesítési adatkészletre. A négy prediktív modell betanításához használt oktatókészlet az adatok 70 százalékát tartalmazta (n=5,156). Az érvényesítési halmazt (n=2,209) használtuk az egyes modellek prediktív erejének robusztus tesztelésére. A külön érvényesítő készlet reálisabb becsléseket adott a modellek előrejelzési pontosságára vonatkozóan, és segített elkerülni a túlillesztést.

3. lépés: Változó választásA modellépítési folyamat egyik fontos lépése a prediktorváltozók szűkös halmazának kiválasztása a rendelkezésre álló független változók nagy halmazából (n=98). Túl sok független változó a modellben a túlillesztés kockázatával jár, ami viszont csökkenti a prediktív képességet[20]. A független változók kiválasztásához fa módszereket használtunk: 1. Szakértői vélemény: A fában tapasztalt nefrológusok áttekintették a független változók lehetséges halmazát, és jelezték, hogy a változónak van-e klinikai jelentősége. Legalább két szakértő megállapodása megfelelőnek bizonyult ahhoz, hogy egy változót beépítsünk a modellbe. 2. A főkomponens-elemzés [21] csökkenti egy adathalmaz dimenzióját azáltal, hogy a változók közötti összefüggések alapján kisebb számú főkomponensre transzformálja. Ez az összetevőkészlet ideális esetben megtartja a szórások nagy részét, így nem veszít információt, de ezt kevesebb változó használatával teszi. A főkomponensek számát használtuk, amelyek megtartották az eredeti variancia 90 százalékát. 3. Rugalmas nettó kereskedések – a modell ft és összetettsége a takarékos modell megtalálásához. Számos modellt vizsgál meg büntetésekkel a túlillesztés elkerülése érdekében, amelyek a büntetés hiányától (Ridge-regresszió – L2) a szélsőséges büntetésig (Lasso-regresszió – L1) terjednek, hogy keresztellenőrzés segítségével megtalálják az ideális büntetés kompromisszumos pontot[22]. . A kereszt-validáció során a legalacsonyabb átlagos négyzetes hibát produkáló L1 és L2 értékeket használtuk a rugalmas háló modell ft-jéhez. Ezeket az egyedi változókiválasztási módszereket önmagukban és minden lehetséges kombinációban is alkalmaztuk, pl. szakértői vélemény, majd rugalmas háló. Ezért összesen hét változókiválasztási módszert alkalmaztunk hét különböző független változókészlet létrehozására.
4. lépés: ModellképzésNégy megközelítést alkalmaztunk az elsődleges eseményig, azaz a túlélési kimenetelig eltelt idő modellezésére. Cox-arányos regresszió[14]. Ezt a félparaméteres modellt széles körben használják az eredmények, például a túlélési adatok és a független változók közötti kapcsolat feltárására. A kiválasztott független változók modellezése után a változók számát tovább csökkentettük azzal, hogy csak azokat vettük be, amelyek statisztikailag szignifikánsak voltak (p<0.05). this="" made="" the="" model="" more="" parsimonious="" and="" also="" improved="" predictive="" power.="" survival="" tree[11].="" a="" survival="" tree="" is="" a="" tree-like="" structure,="" where="" leaves="" represent="" outcome="" variables,="" i.e.="" graft="" failure="" (1)="" or="" no="" graft="" failure="" (0),="" and="" branches="" are="" independent="" variables="" that="" influence="" the="" timing="" of="" the="" outcome.="" the="" complexity="" parameter="" was="" set="" to="" 0.00001="" and="" the="" following="" two="" hyper-parameters="" were="" regularized="" until="" the="" optimal="" tree="" was="" created:="" the="" minimum="" number="" of="" samples="" that="" must="" exist="" in="" a="" node="" in="" order="" for="" a="" split="" to="" be="" attempted,="" and="" the="" number="" of="" competitors="" splits="" retained="" in="" the="" output.="" random="" survival="" forest="" (rsf)="" [12].="" rsf="" is="" an="" ensemble="" method="" where="" numerous="" unpruned="" survival="" trees="" are="" developed="" via="" bootstrap="" aggregation[23,="" 24].="" te="" 'variable="" importance'="" was="" set="" to="" "permutation"="" and="" the="" splitting="" rule="" to="" "log-rank".="" te="" hyper-parameters,="" a="" number="" of="" variables="" to="" possibly="" split="" at="" each="" node,="" a="" number="" of="" trees="" and="" a="" minimum="" number="" of="" nodes="" were="" regularised="" to="" achieve="" the="" lowest="" out-of-bag="" prediction="" error.="" 'variable="" importance',="" a="" variable="" selection="" algorithm="" widely="" used="" in="" rsf,="" was="" used="" to="" avoid="" overfitting="" and="" to="" reduce="" the="" prediction="">
Túlélést támogató vektorgép[13]. Ez hipersíkokat használ független változók osztályainak létrehozására akár lineárisan (pl. lineáris kernelfüggvény), akár nem lineárisan elválasztható adatokkal (pl. polinomiális kernel)[26, 27]. A modell teljesítménye alapján az összes támogatási vektorgép-modellt lineáris kernelfüggvénnyel illesztettük egy „regressziós” típusú túléléstámogató vektorgép modellel. A hét független változókészletet a négy prediktív modell betanítására és validálására használták, amelyek 28 eredményt kaptak: hét változó kiválasztási módszer × négy prediktív modell. A megjósolt eredmény mind a négy modell esetében egy intervallumskálán lévő index volt, amelyet a következőnek jelölünkVeseátültetésKockázati index.

A CISTANCHE JAVÍTJA A vese-/veseelégtelenséget
5. lépés: A modellek értékeléseA modelleket Royston és Altman által javasolt módszerekkel értékeltük ki[28]. A modell teljesítményét két mérőszámmal értékelték: megkülönböztetés és kalibráció. A jó diszkriminációt mutató indexnek magasabb kockázati pontszámmal kell rendelkeznie a magasabb kockázatú betegek esetében, és fordítva. A kalibráció az előrejelzés pontosságát méri, mivel összehasonlítja az index alapján várható túlélés pontosságát a megfigyelt adatok túlélésével[29]. Vizsgálatunk számára az objektív diszkrimináció fontosabb, mint a kalibrálás, mivel célunk az, hogy útmutatót nyújtsunk a döntéshozatalhoz, amely azonosítja a viszonylag magas és alacsony kockázatú betegeket[28]. Ezért a legjobb modellt a konkordanciaindex (C-index)[30] segítségével választottuk ki, amely egy olyan index, amely a modell megkülönböztető képességét értékeli. A Te C-index a betegpárok azon hányada, ahol a hosszabb túlélési idővel rendelkező betegnek alacsonyabb a kockázati előrejelzési pontszáma is. A konkordancia tartomány nulla és egy között van, a magasabb érték jobb teljesítményt, a 0,5 pedig a véletlen diszkriminációt jelzi.
Royston és Altman értékelési módszereit alkalmazva a legjobban illeszkedő modellek indexeit négy csoportba soroltuk a 16., 50. és 84. centilisben, hogy négy prognosztikai csoportot alakítsunk ki: jó, meglehetősen jó, meglehetősen rossz és rossz. Az egyenlőtlen méretű csoportok alkalmazása javította a betegek megkülönböztetését a négy csoport között, és csoportosította a hasonló kockázatú betegeket[28]. E négy csoport túlélését Kaplan–Meier görbék segítségével hasonlították össze, amelyek ideális esetben nagy különbséget mutatnak a túlélésben a négy csoport között.
A kalibrációt vizuálisan értékelték a legjobban illeszkedő Cox-modell segítségével. Bootstrap-újramintákat használtak a torzítással korrigált előrejelzett és megfigyelt átlagos túlélés becslésére a transzplantációt követő 3 és 5 évben[31]. Az előre jelzett és a megfigyelt átlagos túlélés tökéletes egyezése tökéletesen kalibrált előrejelzési modellt jelez. A legjobb predikciós modellt a KDRI előrejelző képességével hasonlították össze, amely modell jelenleg számos klinikai döntéshozó által használt. A Te KDRI 14 donorral és transzplantációval kapcsolatos változóval rendelkezik, és Cox-regresszióval fejlesztették ki a graft teljes kudarcának előrejelzésére. A változókat a nem szignifikáns változók fokozatos törlésével választották ki[3], és ennek a modellkiválasztási módszernek számos, a szakirodalomban dokumentált korlátja van, beleértve a kollinearitást, a túl kicsi p-értékeket és a túl szűk konfidenciaintervallumokat[32]. A prediktív modellek kifejlesztéséhez a Te R programozási nyelvet (3.6.{13}} verzió), a „survivalism”, „ranger”, „survival” és „LTRCtrees” könyvtárat használták[33].
EtikaAz ANZDATA nyilvántartás tevékenységei teljes etikai jóváhagyást kaptak a Royal Adelaide Hospital Humán Kutatási Etikai Bizottságától. Ezt a tanulmányt a Queenslandi Műszaki Egyetem etikai jóváhagyásával engedélyezte.
Eredmények
AlapjellemzőkA recipiensek és donorok jellemzőit az 1. táblázat tartalmazza. A teljes vizsgálati mintában 7365 elhunyt donor volt.veseátültetések2007. január 1. és 2017. december 31. között végezték. A donorok medián életkora 52 év (interkvartilis tartomány 41-60), a recipienseké 47 év (interkvartilis tartomány 32-58). A legtöbb férfi volt (63 százalék). Az oltványok körülbelül 87 százaléka elsődleges graft volt.

Változókiválasztás 98 lehetséges független változó volt. A 2. táblázat összefoglalja a három megközelítés eredményét a független változók egy olyan részhalmazának kiválasztására, amelyek nem illeszkedtek túl, így hét független változókészletet kaptunk. A szakértői vélemény a független változókat 40 változóra, míg a rugalmas nettó 46 változóra csökkentette. Mindhárom változó kiválasztási módszer alkalmazása a 98 potenciális változót 23 főkomponensre csökkentette. A hét független változókészlet mindegyikét a modellek betanítására és tesztelésére használták. A modellépítés során a független változókat tovább csökkentették a cox-ban és az RSF-ben azáltal, hogy csak azokat vették be, amelyek statisztikailag szignifikánsak voltak (p<0.05) and="" including="" only="" those="" with="" positive="" 'variable="" importance'="" (a="" variable="" selection="" algorithm="" used="" in="" rsf),="" respectively.="" model="" development="" and validation="" te="" predictive="" performance="" of="" the="" models="" is="" compared="" in="" table 3.="" cox="" proportional="" regression="" and="" rsf="" outperformed="" the="" other="" two="" models="" (i.e.="" survival="" tree="" and="" support="" vector="" machine).="" the="" highest="" c-index="" (0.67)="" was="" from="" a="" cox="" proportional="" regression="" model="" which="" used="" expert="" opinion="" as="" the="" variable="" selection="" method="" and="" rsf="" which="" used="" the="" elastic="" net="" as="" the="" variable="" selection="" method.="" a="" c-index="" of="" 0.67="" indicates="" the="" moderate="" discriminative="" ability="" of="" death-censored="" graft="" failure.="" the="" discriminative="" ability="" of="" kdri="" in="" discriminating="" death-censored="" graft="" failure="" was="" 0.53,="" a="" lower="" prediction="" ability="" than="" our="" two="" best="" models.="" the="" cox="" model="" used="" 7="" independent="" variables="" while="" the="" rsf="" used="" 20="" variables="" (table 4).="" since="" the="" cox="" model="" was="" able="" to="" produce="" the="" same="" discriminatory="" power="" with="" a="" lower="" number="" of="" variables,="" it="" was="" considered="" as="" the="" best="" fitting="">


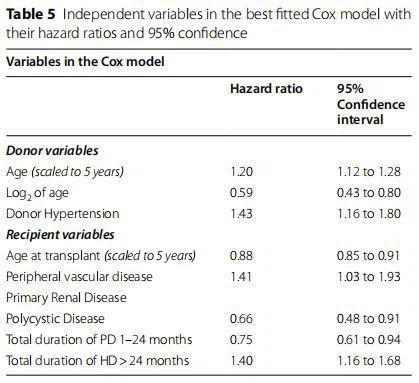
A legjobban illeszkedő Cox modellMivel a donor életkora erős előrejelzője volt a graft túlélésének, az életkor nem lineáris transzformációját (logaritmus bázis 2) hozzáadtuk a modellhez. Ez csak 0-kal növelte a C-indexet.{11}}03. Az indexet a donor medián (45 év) és a recipiens életkor (50 év) alapján skáláztuk. A Cox-modell indexét a 2. ábrán látható módon számítjuk ki. Alternatívaként egy Weibull-modellt is beépítettünk, amely feltételezi, hogy a veszély időfüggő[34]. A C-index azonban 0,0014-gyel csökkent, nem növelve a diszkriminációt, így megtartottuk a Cox-modellt. A donor hipertónia (HR 1,43; 95 százalékos CI 1,16-1,76) növelte a kockázatot policiszta eseténvesebetegségmivel az elsődleges vesebetegség csökkentette a kudarc kockázatát (HR {0}},66; 95 százalékos CI 0,48-0,91) (5. táblázat).
Az index összesített betegszámának megoszlása azt mutatja, hogy a kockázati csoportok pontszáma "jó" (< 16th="" centile)="" and="" "fairly="" good"="" (16th–50th="" centile),="" have="" a="" narrow="" separation,="" whereas="" the="" other="" two="" categories="" ("fairly="" poor"="" and="" "poor")="" are="" clearly="" separated="" (supplementary="" figure ="" 1).="" this="" indicates="" that="" the="" cox="" model="" does="" better="" at="" separating="" the="" higher="" risk="" groups.="" the="" cox="" model="" was="" able="" to="" discriminate="" the="" extreme="" categories="" of="" graft="" failure="" risk="" (good="" vs="" poor)="" with="" good="" discriminative="" power="" (c-index="0.73)." discrimination="" between="" other="" groups="" was="" moderate="" (c-index="">0.6) (6. táblázat). Kaplan–Meier túlélési görbéi, amelyek a halált cenzúrázva mutatjákveseA négy kockázati csoport graft-elégtelensége a 3. ábrán látható. Ahogy a kockázati csoportok „jó”-ról „gyenge”-re váltanak, a túlélési görbék a graft-elégtelenség jelentős megnövekedett kockázatát mutatják. Továbbá a „Jó” csoporthoz képest, ahogy a csoportok „meglehetősen jó”-ról „gyenge”-re váltanak, a kockázati arányok nőnek mind a képzési, mind az érvényesítési adatkészletekben (7. táblázat). Ezek az eredmények azt mutatják, hogy az index jó diszkriminatív erővel rendelkezik[28].
Az átlagos becsült túlélés az átlagos tényleges túléléshez képest 3-év és 5-év esetén a 4. ábrán látható. Egy tökéletesen kalibrált modellben az adatpontok a szaggatott vonal (tökéletes előrejelzési vonal) mentén helyezkednek el. , tökéletes előrejelzési pontosságot jelezve. Az átlagos tényleges túlélés következetesen alacsonyabb, mint a várható túlélés mind 3, mind 5 év után. A tökéletes predikciós vonal és az előrejelzési vonal közötti rés azonban mindkét időszakban csökken, ahogy az előre jelzett túlélés növekszik. Összességében a Cox-modell mérsékelt előrejelzési pontosságot mutat.
Vita
Vizsgálatunk egy kockázat-előrejelzési modellt fejlesztett ki a graft elégtelenségének előrejelzésére, nagy betegminta felhasználásával. Négy lehetséges előrejelzési modellt elemeztünk statisztikai és gépi tanulási módszerekkel. A legjobb modell a Cox regressziós kockázat-előrejelzési modell volt, amely csak hét független változó felhasználásával mérsékelt szintű diszkriminációval és előrejelzési pontossággal tudta előre jelezni a halál által cenzúrázott graft-elégtelenséget. A jelenlegi index diszkriminatív ereje felülmúlja a jelenleg rendelkezésre álló graft-kudarc kockázati előrejelzési modelljeit.


A kockázat-előrejelző modellt a transzplantáció előtti döntéshozatalra fejlesztették ki (pl.veseallokáció), ezért csak a transzplantáció előtt rendelkezésre álló változókat tekintettük független változónak. Belső validálást alkalmaztunk egy szűkszavú modell létrehozásához, mivel nagyszámú független változó használatával könnyen létrehozhatunk gyengén teljesítő modelleket, amelyek a túlillesztés miatt nem általánosíthatók [35]. A lépcsőzetes változókiválasztás, egy általánosan használt változókiválasztási módszer, amelyet a KDRI kifejlesztéséhez használtak, egy instabil módszer, amely olyan modelleket hozhat létre, amelyek rosszul teljesítenek a külső validálásban [28]. A jelenlegi tanulmányban hét különböző változó kiválasztási kombináció használata, amelyeket szakértői vélemény és statisztikák kombinációja azonosított, segített azonosítani
a legfontosabb változók, amelyek megmagyarázták az adatok legtöbb eltérését. A szerény modell olyan indexet eredményez, amely könnyebben használható klinikai környezetben. A végső legjobb Cox-modell hét változóból áll, ami kevesebb, mint ahány változót a leggyakrabban használt grafthiba-kockázat-előrejelző modellekben használnak [3, 36].
A Cox-modell felülmúlta a tanulmányban használt három gépi tanulási módszert. Az irodalom áttekintése azt mutatja, hogy az előrejelzési pontosság vegyes eredményeket adott a gépi tanulás és a hagyományos prediktív módszerek összehasonlításakor [8]. A jelenlegi tanulmány két fa-alapú gépi tanulási módszert használt, és ezeknek a módszereknek az adataink gyengébb teljesítménye arra utalhat, hogy az adatoknak nincs mögötte fastruktúra, ahol az eredményeket bináris felosztások határozzák meg. A graft túlélési kockázata inkább a folyamatos előrejelzőktől, például az életkortól függhet.
Modellünket a halál-cenzúrázott graft-elégtelenség előrejelzésére fejlesztettük ki, míg a teljes graft-elégtelenség magában foglalja a graft elégtelenségét, valamint a működő grafttal való halált. Adott donor túlélésének ismereteveseA transzplantáció előtti döntéshozatalban fontosabb, mint a graft teljes kudarca [2]. Vizsgálatunkban a halál által cenzúrázott graft-elégtelenség C-indexe 0,67 volt. Clayton et al. validálta az amerikai KDRI-t az ausztrál adatok [2] és a C-index segítségével a halál cenzúrázott megkülönböztetésében.

a graft meghibásodása {{0}}.63 volt, ami alacsonyabb diszkriminációt jelent, mint az itt kapott eredmények. Mindazonáltal a transzplantáció és a recipiens jellemzőinek (összesen 24 független változó) bevonása a KDRI-be a Clayton et al. tanulmány. Ezek a szerzők nem értékelték a kalibrációt (előrejelzési pontosságot), ami akadályozza a vizsgálatunk eredményeivel való átfogó összehasonlítást. Legjobb modellünk C-indexe mindössze hét változó esetében 0,67, míg az utóbbi 24 változójának C-indexe 0,70, és a klinikusok úgy ítélhetik meg, hogy ez a kis pontosságnövekedés nem éri meg a bonyolultság növelését. A sok változót tartalmazó előrejelzési modellek logisztikailag is bonyolultabbak, mivel több adatot igényelnek, és egyetlen változó hiánya miatt az előrejelzés nem becsülhető meg.
Ezen túlmenően a jelenlegi index diszkriminatív ereje felülmúlta néhány jelenleg elérhető indexet, köztük a korábban leírt KDRI-t. Kasiske et al. (2010), 11 donor és recipiens változót tartalmazó indexet dolgozott ki, amely a transzplantáció előtt elérhető volt, és C-indexe 0,649 [37] volt. Molnar és munkatársai egy újabb, 2018-as indexe 0,63-as C-indexet mutatott a graft-elégtelenségben szenvedő, magas kockázatú betegek megkülönböztetésében. Ez az index 10 donor és recipiens jellemzőt használt [38]. Ezért az ebben a cikkben ismertetett index kevesebb változóval kiváló diszkriminációs erőt tudott elérni. Mindazonáltal mérlegelnünk kell, hogy egy mérsékelt diszkriminációs képességű indexet (C-index 0,67) használó előrejelzés elfogadható-e az allokáció szempontjából.vese, mivel a modell messze van a tökéletes 1-es C-indextől, vagyis mi


nem lehet biztos abban, hogy az előre jelzett allokációk a legjobb eredményeket fogják hozni. Ha a predikciós modellben a transzplantáció idején hamisan magas indexet mutatnak, az eltántoríthatja a klinikust és a pácienst attól, hogy elfogadja a donort.vese. A donor hibás címkézésének megbélyegző hatásavesemivel a „marginális/alacsony minőséget már dokumentálták [39].
A graft kudarcának előrejelzése összetett jelenség, amely magában foglalja a donor jellemzőit, a donorszerv-kivételhez kapcsolódó jellemzőket, a recipiens jellemzőit, a transzplantációhoz kapcsolódó jellemzőket és a transzplantáció utáni tényezőket, például az immunszuppresszív gyógyszerek alkalmazását. kapcsolódó döntésekveseaz allokációt természetesen az átültetés előtt kell elvégezni; ezért a transzplantációs eljárási és a transzplantáció utáni tényezők nem állnak rendelkezésre a kezdeti döntéshozatal időpontjában. Ezért a legtöbb jelenleg rendelkezésre álló predikciós modellben nem számolt variabilitás forrása (amint azt a diszkriminációs képességük csak mérsékelt szintje bizonyítja) a transzplantációs eljárási vagy a transzplantáció utáni tényezők lehetnek. Lehetnek olyan donor vagy recipiens tényezők is, amelyeket nem rutinszerűen rögzítenek az adatbázisok, valamint előre nem látható sztochasztikus események, amelyek tökéletlen előrejelzésekhez vezetnek. Ez azt jelenti, hogy a tökéletes 1-es C-index valószínűleg lehetetlen egy olyan modellnél, amely transzplantáció előtti tényezőket használ. Nehéz megmondani, hogy mi a legmagasabb elérhető C-index, és ehhez külön modellezési gyakorlatra lenne szükség, amely ellenőrizhetetlen feltételezéseket tartalmaz 1) sztochasztikus események és 2) nem mért előrejelzők fontosságáról.

A CISTANCHE JAVÍTJA A VESE/VESE FERTŐZÉSÉT
A Te Cox modell képes volt megkülönböztetni a graft meghibásodási kockázatának szélsőséges kategóriáit (Jó vs. Rossz) jó diszkriminációs erővel (C-index=0.73), így az eszköz használhatósága a graft meghibásodási kockázat extrém kategóriái között jobb a többi kockázati kategóriához képest. Ezért az eszköz használatának csak ezekre a kockázati kategóriákra való korlátozása kiváló eredményeket hozhatveseátültetésDöntéshozatal. Robusztus belső validálást alkalmaztunk, de a külső validálás fontos lépés a kockázati index klinikai döntéshozatalba történő elfogadása felé, mivel egy modell teljesítményének csak belső validáción alapuló értékelése a teljesítmény túlságosan optimista értékeléséhez vezethet [28]. Ezenkívül a legtöbb klinikus nem hajlandó olyan eszközt használni, amelyet nem teszteltek különböző eszközökönvesepopulációk. Ezért azt javasoljuk, hogy ezt az indexet külsőleg validálják az általánosíthatóság értékelésére a klinikai gyakorlatban történő felhasználás előtt. Ha az index jó külső érvényességet mutat, akkor az indexnek lehetősége van arra, hogy jobb donort nyújtson a recipienseknek, javítva a jelenlegivesekiosztás. Mivel ez az index donor és recipiens jellemzőkkel is rendelkezik, megjósolhatja, hogy a rendelkezésre álló lehetőségek közül melyik donor-recipiens egyezés rendelkezik a legmagasabb transzplantáció utáni túlélési idővel.
Ennek a tanulmánynak számos korlátja van. A prediktív modell csak az ANZDATA által gyűjtött változókat használta, ezért előfordulhat, hogy nem vettük figyelembe a betegek teljes kockázati profilját. Csak négy módszert használtunk, és más olyan gépi tanulási módszereket is alkalmaztunk, amelyek modellezhetik az eseményig tartó időt, és jobb eredményeket hozhattak volna. A túlélési adatok gépi tanulási modelljei azonban nem eléggé kidolgozottak, ami korlátozza a legjobb alkalmazás modelltípusainak kiválasztását [35].
KövetkeztetésÖsszefoglalva, az új index közepesen jól megkülönbözteti azokat a betegeket, akiknél magasabb a graft-elégtelenség kockázata, és mérsékelt pontossággal ad graft-elégtelenség előrejelzéseket. Ez az ígéretes új index megéri a külső validálás következő lépését, hogy igazolja klinikai környezetben való használatát.

A CISTANCHE JAVÍTJA A VESE/VESE MŰKÖDÉSÉT
