Egérszövet-rezidens peritoneális makrofágok a homeosztázisban, javításban, fertőzésekben és tumoráttétekben 1. rész
Jul 27, 2023
1. Bemutatkozás
A peritoneális üreg, valamint a mellhártya és a szívburok üregei az embrionális coelomból, az embrionális testfal képződéséből származó üregből jönnek létre, amely a parietális lemez mezodermát és az ektodermát, valamint a zsigeri bélfalat tartalmazza. lemezes mezoderma és endoderma.
Az embrió coelom fontos szerkezet az embrióképződés folyamatában, megjelenése jelzi az embrionális fejlődést a blasztociszta stádiumba. A blasztociszta stádiumában az embrió egy folyadékkal teli zsákot fejleszt, amelyet coelomnak neveznek.
Az embrionális coelom nagyon fontos szerepet játszik az embrionális fejlődésben. Környezetet biztosít az embrió számára, hogy táplálkozzon és lélegezzen, és ki tudja üríteni a salakanyagokat. Ezenkívül az embrió coelom bizonyos védelmet nyújthat az embrió számára. Elmondható, hogy az embrió testürege nélkül az embrió nem tud normálisan fejlődni.
Másrészt az immunitás az emberi fejlődés egyik alapvető tényezője is. Az immunitás megvédheti a szervezetet a külső kórokozóktól, vírusoktól, és segíthet a különböző betegségek leküzdésében is. Az embriók esetében, mivel az immunrendszer még nem fejlődött ki teljesen, az embrió az anya immunrendszerére támaszkodik a védelem érdekében.
Bár az embrionális testüreg és az immunitás látszólag nincs összefüggésben, valóban van köztük bizonyos kapcsolat. Számos tanulmány kimutatta, hogy az embrionális coelom környezete szerepet játszik az immunitás kialakulásában. Például az embrió testüregében vannak olyan növekedési faktorok, amelyek elősegíthetik az immunrendszer fejlődését. Emellett az embrió testüregében lévő folyadék táplálékot és védelmet is nyújt az immunsejtek számára.
Összefoglalva, az embrió coelom és az immunitás közötti kapcsolat nagyon szoros. Az embrió coelomja jó környezetet biztosít az embrió fejlődéséhez, és kedvező feltételeket biztosít az immunrendszer fejlődéséhez is. Ezért ápolni kell az embrió coelomjának fontosságát, és immunitásunk védelmére és támogatására kell összpontosítanunk. Ebből a szempontból javítanunk kell az immunitásunkat. A Cistanche jelentősen javíthatja az immunitást, mivel a húshamu különféle biológiailag aktív összetevőket tartalmaz, mint például poliszacharidok, két gomba, Huang Li, stb. Ezek az összetevők stimulálhatják az immunrendszert A rendszer különféle sejtjei, fokozzák immunaktivitásukat.

Kattintson a Cistanche egészségügyi előnyei
Az embrionális coelom kialakulásának folyamatát a Protostomia és Deuterostomia primitív szuperfila konzerválta, így az Annelida, Mollusca, Echinodermata és Tunicata törzsek gerinctelenjei anatómiailag és fejlődésileg egyenértékűek az embrionális coelomával[2] amely az emlősök embrionális fejlődése során a peritoneális, a pleurális és a szívburok üregeit hozza létre.
A peritoneális üreget a peritoneum, a test legnagyobb savós membránja borítja, melynek felülete a bőréhez hasonló, és a mesotheliumból, egy mesodermális eredetű hámból, egy bazális membránból és egy szubmesotheliális kötőszövetből áll. 3]
A parietális peritoneum a hasfal belső felületét szegélyezi, míg a zsigeri hashártya integrálódik az intraabdominalis szervek szerózus rétegeivel.
A hashártya kettős ránca alkotja a mesenteriumot, amely összeköti a hasi emésztőszerveket a hasfallal, és az erek, az idegek és a nyirokerek vezetékeként szolgál. A mesothelsejtek által kiválasztott kis mennyiségű peritoneális folyadék kenőanyagként szolgál a peritoneális üregben, és megakadályozza a hasi szervek közötti mechanikai súrlódást. Egereknél a teljes peritoneális folyadék térfogatát két közelmúltbeli jelentés 50-100 μl körülire becsülte egyensúlyi állapotban,[4,5], és állításuk szerint különbözik a hímek és a nőstények között (≈20 μL vs. ≈100 μL), és az utóbbiban az ivarzási ciklus során megváltozni.[6] A peritoneális folyadéknak a nyirokrendszerbe történő elvezetése lehetővé teszi a peritoneális folyadék recirkulációját,[7] és a mesotheliumban lévő nyílásokon, az úgynevezett sztómákon keresztül érhető el, amelyek főleg a rekeszizomban és az omentumban találhatók.[3]
Az omentum egy zsigeri zsírszövet, amely a mesenterium túlnövekedésével fejlődik ki, és speciális érrendszerrel és szervezett limfoid szövettel rendelkezik, amelyről azt állítják, hogy fontos szerepet játszik a peritoneális fertőzések elleni védekezésben.[8] A rekeszizomon keresztül kifolyó peritoneális folyadék a subperitonealis nyirokrésekbe gyűlik össze, hogy elérje a rekeszizomba gyűjtő nyirokcsomókat, amelyek a mediastinalis nyirokcsomókba szivárognak, míg az omentumon keresztül kifolyó peritoneális folyadék a omentális nyirokrendszerben gyűlik össze, amelyek viszont a bél nyiroktörzsébe gyűlnek össze. a cisterna chyli-n keresztül kapcsolódik a mellkasi csatornához.[3] A peritoneális üreg elvezetése lehetővé teszi a peritoneális homeosztázis és a leukocita recirkuláció szabályozását, de növeli a kórokozók és az áttétes tumorsejtek terjedésének kockázatát.
A peritoneális üreg két fő patológiának van kitéve, a fertőzésnek és a daganatos áttétnek, amelyek általában magas mortalitással járnak, mivel a kórokozók vagy daganatsejtek könnyen terjednek az intraabdominalis szervekben, valamint a peritoneális üreg anatómiai jellemzői, amelyek nagymértékben akadályozzák a hatékony kezelések kidolgozása e betegségek ellen. Annak ellenére, hogy a peritoneális üreg egy zárt tér, nincs könnyen kitéve a behatoló kórokozóknak, például a bőrön, a tüdőn vagy a bélen áthatoló kórokozóknak, peritoneális fertőzések léphetnek fel a bélfal integritásának elvesztése miatt (fekélyek, sérvek fulladása miatt). , vakbélgyulladás vagy daganat növekedése), májcirrózis, véletlen hasi sérülések, hasi műtét vagy peritoneális dialízis.
A hasüreg is ki van téve a parietális vagy zsigeri peritoneumban trauma, fertőzés vagy hasi műtét által okozott sérüléseknek, amelyek peritoneális összenövésekhez vezethetnek. A peritoneális üreg további patológiái közé tartozik - a hashártya endometriózisa, amely magában foglalja az ektopiás vaszkularizált méhnyálkahártya szövet képződését a peritoneumban krónikus gyulladással összefüggésben - a peritoneális autoimmun szerozitist, a peritoneum krónikus gyulladását, amelyet autoimmun betegségek, például Crohn-betegség és műtét utáni peritoneális összenövések.[3,9,10]
A peritoneális fertőzés és a tumor áttétek elleni immunvédelem a helyi védelem első vonalán alapul, amelyet állandósult állapotban a peritoneális üregben jelen lévő állandó peritoneális immunsejtek támogatnak, és veleszületett immunitásérzékelő és reagáló tulajdonságokkal rendelkeznek. A peritoneális üregben az immunvédelem második vonalát a limfoid szövet funkcionális egységei biztosítják, amelyek az omentumban, a mesenteriumban vagy az ivarmirigyben elhelyezkedő zsírszövethez kapcsolódnak, ezeket zsírhoz kapcsolódó limfoid klasztereknek (FALC-knak) vagy tejszerű foltoknak nevezik az omentális FALC-k számára. [8] A FALC-k a másodlagos nyirokszervekhez hasonló szerkezeti felépítést tartalmaznak, beleértve a retikuláris sejtalapú stromát, a B- és T-sejt-kompartmenteket, valamint a speciális vér- és nyirokereket, lehetővé téve a leukocita migrációt a hasüregbe és onnan vissza.[8]
A rezidens peritoneális immunsejtek közé tartoznak a szövetekben rezidens peritoneális makrofágok, amelyeket általában nagy peritoneális makrofágoknak (LPM) és B1-sejteknek neveznek. A legújabb kísérleti bizonyítékok feltárták, hogy elsődleges fagocita funkciójukon kívül az LPM-ek különböző homeosztatikus, javító és immunológiai védelmi funkciókat töltenek be, amelyek egy korábban nem várt funkcionális plaszticitást tükröznek.[11] A peritoneális B1-sejtek veleszületett-szerű B-sejteknek számítanak, amelyek konstitutívan természetes IgM-et termelnek, helyi immunvédelmet biztosítva a kórokozók széles körével szemben.
Ezenkívül a B1 sejtek aktívan termelnek IgM-et vírusokra, baktériumokra, gombákra és parazitákra reagálva.[12] Az emlősök peritoneális üregében kialakuló immunitás első vonala, amely az LPM-ek és B1-sejtek által támogatott fagocita- és antitest-mediált védekezési mechanizmusokra támaszkodik, a gerinctelenek coelomikus üregében jelenlévő különböző coelomociták populációi által fenntartott primitív védekezési mechanizmusokra emlékeztet. 13–15] A cölomikus üregek immunvédelmi stratégiái ezért a gerinctelenektől a magasabb gerincesekig terjedő evolúció során erősen konzerváltak voltak.
Ebben az áttekintésben azokat a legújabb bizonyítékokat tárgyaljuk, amelyek bővítették ismereteinket az LPM-ek biológiájáról azáltal, hogy leírják a rezidens embrionális LPM-ek rezidens csontvelő-monocita eredetű LPM-ekkel (moLPM-ekkel) való helyettesítésének mechanizmusait, amelyek fenotípusos és funkcionális LPM-szexuális dimorfizmust eredményeznek. leleplezve, hogy az egyensúlyi állapotban folyékony környezetben szabadon felszabaduló LPM-ek hogyan látják el a javító és immunvédelmi funkciókat azáltal, hogy a peritoneális sérülésekre válaszul trombusszerű struktúrákat hoznak létre, és bakteriális fertőzés után a mezotéliumhoz kötött dinamikus LPM aggregátumokat.
Ezen túlmenően a legújabb kísérleti bizonyítékok alátámasztják, hogy a peritoneális daganatok felforgathatják az LPM-anyagcserét, ami tumor-elősegítő funkciók megszerzéséhez vezethet, amelyek azonban visszafordíthatók olyan kísérleti stratégiákkal, amelyek blokkolják az LPM-funkció tumor által kiváltott felforgatását, ami a fejlődés alapja lehet. a peritoneális tumor metasztázisok elleni új immunterápiás megközelítések makrofág-átprogramozásán alapuló módszerei.
2. Nagy peritoneális makrofág identitás
Az LPM-ek hosszú életű, szövetben rezidens makrofágok, amelyek az embrionális élet során alakulnak ki, fejlődésileg és funkcionálisan a peritoneális üregre korlátozódnak, ellentétben más peritoneális immunsejtpopulációkkal, amelyek a hasüregbe verbuválódnak, és egyensúlyi állapotban más helyekre keringenek vissza, és patológiás körülmények között. Ezek közé tartoznak egyensúlyi állapotban a B1-sejtek, amelyek az LPM-ekkel együtt a peritoneális mosással gyűjtött sejtek túlnyomó többségét alkotják, valamint a monocita eredetű SPM-ek (kis peritoneális makrofágok esetében), B2-sejtek, T-sejtek, NK-sejtek alacsony százalékát. , veleszületett limfoid sejtek és hízósejtek.[11]
Amint azt ebben az áttekintésben részletesen tárgyaltuk, az elmúlt években végzett kutatások megállapították, hogy az LPM-ek nemcsak peritoneális homeosztatikus funkciókat töltenek be, hanem részt vesznek a gyulladás és fertőzés által okozott szövetkárosodás helyreállításában és a mikrobiális fertőzések elleni védekezésben is. Ezenkívül az LPM-ek hozzájárulnak a legtöbb peritoneális patológiához, különösen a peritoneális tumor áttéthez, de a peritoneális endometriózishoz, az autoimmun szerositishez és a posztoperatív összenövésekhez is.
A rezidens embrionális LPM-ek CD11b plusz F4/80hi MHC-II− sejtek, amelyek a szövetekben rezidens makrofágokat jellemző markerek sorozatát expresszálják, mint például a CD14, CD64 és MerTK.[16,17]

Emellett a test savós üregeiben elhelyezkedő szövetben rezidens makrofágok, amelyek LPM-eket és a pleurális és perikardiális üregekben jelenlévő szövetben rezidens makrofágokat tartalmaznak, úgy tűnik, hogy osztoznak a GATA6 transzkripciós faktor, a Tim4 scavenger receptor és az M. -CSF receptor CFSR1.[11,18] Ezenkívül a rezidens embrionális LPM-eket számos sejtfelszíni receptor expressziója jellemzi, amelyek tükrözik az LPM homeosztatikus, javító, szabályozó és védekező funkcióit, beleértve az LPM adhéziójában és lokalizációjában szerepet játszó molekulákat, mint például az ICAM. -2 (CD102), CD11b, CD49f, CD73 és CD62P,[19] az elhalt sejtek felismerése és eltávolítása, például CD36, CD93, CD163, Tim4, MerTK, MARCO és MSR1,[4,16,20 –22] a makrofágok aktivációjának negatív szabályozása, biztosítva az apoptotikus sejtek nem gyulladásos kiürülését, mint például a 4-et tartalmazó V-set immunglobulin domén (VSIG4),[23] kórokozók megkötése, például CD14, CD36 és SIGN-R1 (CD209b) )[11,24] és a kórokozókra, például a TLR4-re és a TLR7-re adott válasz.[25,26] Az embrionális LPM-ek által kifejezett legreprezentatívabb sejtfelszíni molekulákat az 1. ábra foglalja össze.

Az LPM-ek a szövetben rezidens makrofágok családjába tartoznak, amelyek osztoznak az embrionális élet során meghatározott magvonalhoz kapcsolódó gének expressziójában, de szövetspecifikus transzkripciós és funkcionális jellemzőket sajátítanak el a szövetspecifikus mikrokörnyezeti jeleknek való kitettség során, a szövetek expressziója révén. -specifikus transzkripciós faktorok.[16,27] Ebből a szempontból a GATA6 transzkripciós faktor nélkülözhetetlen az LPM-specifikus génexpresszióhoz, proliferációhoz és az LPM-ek túléléséhez.[19,28,29] Ebből következően a homeosztatikus, javító és védekező LPM. A myeloid sejtekben GATA6-hiányos egerek funkciói károsodtak.[5,19,30] A GATA6 expressziója nem sejt autonóm módon fennmarad[27,31], és in vitro kísérletek alapján azt javasolták, hogy a Az A-vitamin metabolitja, a retinsav, a retinsav nukleáris receptorain keresztül.[19]
A GATA6 expresszióját így módosítaná a retinsav helyi elérhetősége, ami alátámasztja azt az elképzelést, hogy az LPM-ek GATA6-indukált transzkripciós programja reverzibilis,[17] ami az LPM-ek funkcionális plaszticitásának alapja lenne, ami lehetővé teszi Az LPM-ek szükség esetén átválthatnak homeosztatikusról javító vagy immunvédelmi funkciókra.
Ebben a tekintetben az alveoláris térbe átvitt LPM-ek leszabályozták a GATA6-ot, és alveoláris makrofág transzkripciós profilt nyertek.[27] Az LPM-ekben lévő GATA6-ot aktiváló retinsavról azt állították, hogy az omentális és a peritoneális stromasejtek termelik.[19] Ezekkel a megfigyelésekkel összhangban azt állították, hogy a Wilms-tumor 1 (WT1) transzkripciós faktorának mezoteliális és fibroblasztos stroma sejtjei expresszálják, amelyek a retinol metabolizmusát szabályozó két sebességkorlátozó enzim, a RALDH1 és a RALDH2 [32] expresszióját szabályozzák. szabályozza a GATA6 expresszióját az LPM-ekben és a GATA6 plusz a mellhártya és a szívburok üregében elhelyezkedő makrofágokban, mivel a WT1 plusz sejtek kimerülése ezekben a makrofág-alcsoportokban mélyreható csökkenést eredményezett, ami párhuzamosan a Raldh1 és Raldh2 transzkriptumok egyidejű csökkenésével[18]. tovább támasztja a retinsav szerepét a GATA6 expresszió fenntartásában, amit azonban még formálisan bizonyítani kell.
Az a tény, hogy GATA{0}}hiányos egerekben a CD11b plusz makrofágok a tejszerű tejfoltokban halmozódtak fel, míg a peritoneális üregben az LPM-ek csökkentek[19], alátámasztja azt a hipotézist, hogy az omentumban lévő stromasejtek által kiválasztott retinoidsav fenntartja a GATA{ {3}}vezérelt transzkripciós program az LPM-ekben, és azt jelentené, hogy az LPM-ek folyamatosan keringenek az omentumon keresztül, de ezt még formálisan bizonyítani kell.
A retinsav a retinoid X-receptorok (RXR-ek) liganduma, amelyek a ligand-függő transzkripciós faktorok nukleáris receptor szupercsaládjának tagjai, amelyek szabályozzák a lipid- és glükóz-anyagcserét, és kulcsszerepet játszanak a gyulladásos és autoimmun betegségekben.[33] Érdekes módon az RXR-ekben és -ben hiányos egerek az újszülöttkori LPM expanziójában és a felnőtt LPM-ek túlélési idejének csökkenésében mutatkoztak meg az apoptózist eredményező lipidfelhalmozódás miatt, ami feltárta, hogy az RXR-ek hozzájárulnak az LPM kiterjesztéséhez és fenntartásához.[34] Az ATAC-seq elemzések kimutatták, hogy a Gata6 lókusz csökkent kromatin-hozzáférhetőséget mutatott az RXR-hiányos LPM-ekben, ami korrelált a Gata6 gén alacsonyabb expressziójával, ami alátámasztja, hogy az RXR-ek szabályozzák a GATA6-függő LPM transzkripciós programot.
A makrofágkolónia-stimuláló faktor (M-CSF vagy CFS1) szabályozza a makrofágok vonala iránti elkötelezettséget, és ezért az LPM differenciálódása a CFS1-től függ, amint azt osteopetrosis (Csf1 op/op) egerekben kimutatták, amelyek mutációt hordoznak a Cfs1 génben, ami hibás LPM fejlesztés.[35] Ezen túlmenően, in vitro vizsgálatok alapján a mezoteliális sejtek CSF1-et szekretálnak, amely fenntartotta az LPM proliferációt a mesothel sejt-LPM kotenyészetekben; A transwell vizsgálatok kimutatták, hogy az LPM proliferációja szignifikánsan csökkent, ha a mesothel-LPM kölcsönhatásokat megakadályozták, ami arra utal, hogy a sejt-sejt érintkezés hozzájárult az LPM proliferációjához.[36] Azt az elképzelést, hogy mezoteliális eredetű CSF1 szükséges az LPM fenntartásához, tovább támasztja egy nemrégiben megjelent jelentés, amely szerint az LPM-ek nagymértékben csökkentek azokban az egerekben, amelyekben a WT1 plusz sejtek CFS1-hiányosak voltak.[37] Továbbra is meg kell vizsgálni, hogy a mezoteliális sejtekből származó CSF1 hozzájárul-e az LPM egyensúlyi állapotú önmegújulásához és/vagy az LPM proliferációjához a gyulladás során.
3. A nagy peritoneális makrofágok eredete és cseréje a homeosztázisban
Az LPM-ek az embrionális élet során differenciálódnak, és a felnőtt élet során in situ önmegújulás útján tartják fenn magukat. Állandósult állapotban az embrionális LPM-eket az embrionális fejlődés késői szakaszaitól fokozatosan, részben mégis felváltják a rezidens csontvelői moLPM-ek, amelyek rezidens embrionális LPM-azonosságot szereznek, de megőriztek eredetükhöz kapcsolódó transzkripciós és funkcionális jellemzőket.[38,39] ] Az embrionális LPM-ek eredete továbbra is vitatott, mivel a jelentések szerint vagy a tojássárgája-makrofágok és a magzati máj monocitáinak kettős hozzájárulásából,[40] vagy kizárólag a magzati májmonocitákból származnak.[41] Az LPM-ek eredetének és cseréjének integrált modellje a 2. ábrán látható.
Dr. F. Ginhoux laboratóriuma szerint az embrionális csontvelő-monocita eredetű szövetrezidens makrofágokkal való helyettesítését egyensúlyi állapotban minden szövetben rezidens makrofág populációban leírták, kivéve a mikrogliát, a Langerhans-sejteket és a Kupffer-sejteket. , az Ms4a3 gén expresszióján alapuló sors-térképezési modellekkel, amelyet specifikusan granulocita-monocita progenitorok expresszálnak.[42] Úgy tűnik, hogy a csontvelő-monocita-eredetű makrofágokkal való helyettesítés mértékét alapvetően a szűkös hozzáférés és elérhetőség határozza meg.[43] A szövetekben rezidens makrofágpopulációk egyike sem mutat teljes helyettesítést csontvelő-monocita eredetű makrofágokkal, ami arra utal, hogy minden egyes szervben létrejön az egyensúly a csontvelő-monociták toborzása, valamint az embrionális és csontvelő-monocita-eredetű rezidens makrofágok proliferációja és túlélése között. [42]

Ezért a felnőtt élet során a rezidens LPM-készlet állandó állapotban van fenntartva a rezidens embrionális LPM-ek önmegújulása és a rezidens moLPM-ek differenciálódása és önmegújulása kombinációjával. Következésképpen ebben a kéziratban, hacsak másként nem jelezzük, az LPM-ek kifejezés a felnőtt LPM-populációt jelenti, amely egyensúlyi állapotban rezidens embrionális LPM-eket és rezidens moLPM-eket tartalmaz. Érdekes módon a szexuális érettség után az embrionális LPM-csere aránya magasabb azoknál a férfiaknál, akiknek LPM-jei magasabb proliferációs aktivitást mutatnak, amint azt Dr. F. Ginhoux és Dr. S. Jenkins laboratóriumában végzett genetikai sorsfeltérképezési elemzések igazolják, és ennek ellenére különbségekről számoltak be a pótlások arányában.[39,42] Ginhoux és munkatársai[42] azt találták, hogy a 8 hetes és 20 hetes korukban nagyobb arányban fordulnak elő moLPM-ek a férfiaknál (≈25 százalék vs 10 százalék és ≈50 százalék vs 25 százalék). , illetve).
Ezzel szemben Jenkins és munkatársai[39] arról számoltak be, hogy a rezidens moLPM-ek ≈30 százalékát mutatták ki mind a férfiaknál, mind a nőstényeknél a 4. héten, míg a 16. héten a férfiaknál nagyobb arányban voltak jelen a rezidens moLPM-ek (≈60 százalék vs 30 százalék). A szexuális dimorf helyettesítést rezidens moLPM-ekkel a peritoneális mikrokörnyezet szexuális érés során bekövetkező változásaival szabályozták, függetlenül az ösztrogénszinttől és a peritoneális zsírosodástól [39], ami az LPM populáció heterogenitásának eltéréséhez vezet. Az LPM populáción belüli heterogenitás nemi eredetű eltérései, valamint a peritoneális mikrokörnyezet nemi különbségei jelentős transzkripciós és funkcionális különbségeket határoznak meg a hím és nőstény egerek LPM populációja között, bár az RNS-seq elemzések egysejtszinten feltárták ekvivalens klaszter-identitás a férfi és női LPM-ekben.
RNA-seq analyses, at the population level, of 10- to 12-week-old male and female mice LPMs indicated that 486 mRNA transcripts were differentially expressed (>1.5-fold) a női és férfi LPM-ek között. A 148 mRNS-transzkriptum, amely populációs szinten fokozottabban expresszálódik női LPM-ekben, lipidfelvétellel és -transzporttal kapcsolatos géneket, például Apoe-t, Apoc1-et, Saa2-t és Saa3-at, valamint immunvédelemmel kapcsolatos géneket tartalmazott. Utóbbiak közé tartozott a Timd4, Cxcl13, Tgfb2, a komplementkomponens C1qa, C3 és C4b gének, valamint a C-típusú lektinreceptor gének Cd209a, Cd209b és Clec4g. [39] Ezzel szemben a férfiaknál az LPM-ek által erősebben expresszált gének a proliferációhoz és a sejtciklushoz kapcsolódó folyamatokhoz kapcsolódnak, mint például a Cdk1, E2f2 és Mki67.
Érdekes módon a nőstény egerek ellenállóbbak voltak a B csoportba tartozó streptococcusok[44] vagy a Streptococcus pneumoniae fertőzés által kiváltott akut hashártyagyulladással szemben[39]. Mivel a CD209 (SIGN-R1) kritikus fontosságú a S. pneumoniae fertőzés utáni túlélés szempontjából, mivel elősegíti a hatékony bakteriális fagocitózist és kiürülést[24], a bakteriális hashártyagyulladással szembeni nemtől függő rezisztenciát a női LPM-ek magasabb expressziójának tulajdonítják. a CD209 és ezen kívül a komplement komponensek és a B1 sejteket toborzó CXCL13 kemokin.[39] Ebben a tekintetben a nők és a csecsemők vérrel terjedő fertőzésekkel szembeni nagyobb rezisztenciája összefüggést mutat a természetes antitestek B1-sejtek fokozott CXCL{12}}-függő termelésével.
4. Gyulladás által kiváltott nagy peritoneális makrofágok pótlása
Steril gyulladásos ingerek [5,39,42,45,46] hasi műtét[39] vagy bakteriális fertőzés[47] által kiváltott gyulladásos reakciók a hasüregben a jelentések szerint LPM-sejtpusztulást okoztak, ami a sejtek számának csökkenéséhez vezet. rezidens LPM-ek (beleértve a rezidens embrionális LPM-eket és a rezidens moLPM-eket), amelyek mértéke korrelál a gyulladás súlyosságával.[42,46] Az eredeti LPM-készlet helyreállítása a fennmaradó rezidens LPM-ek [45] elszaporodásával és a gyulladásból származó LPM-ekkel való helyettesítésével történik. monociták (továbbiakban ii-moLPM-ek a gyulladás által kiváltott moLPM-ekre), amint azt különböző kísérleti stratégiákkal, sors-térképezési modelleken [42], szövetvédett csontvelői kiméra egereken és adoptív transzfer kísérleteken alapulva mutatták be.[39,46]
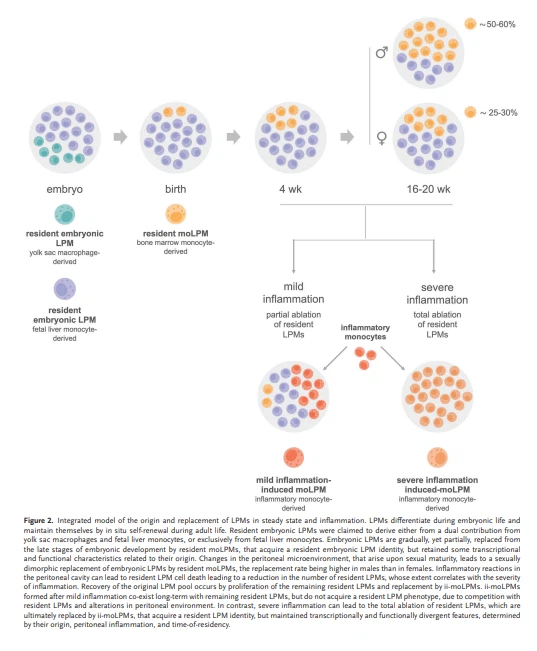
Kis dózisú zimozán (10 ug/egér), vagy nagy dózisú zimozán (1000 ug/egér) által okozott súlyos gyulladás (1000 ug/egér) által okozott enyhe gyulladás indukálására épülő kísérleti modell, valamint adaptív átviteli kísérletek alkalmazása a ii-moLPM-ek nyomon követésére. Jenkins és munkatársai azt javasolták, hogy a rezidens LPM-ek ii-moLPM-ekkel való helyettesítésének mértékét, valamint azt, hogy a későbbiekben milyen mértékben sajátítják el a rezidens LPM-ek azonosságát és funkcióját, a gyulladás súlyossága határozza meg, hogy a gyulladásos környezet hogyan szabályozza a differenciálódásukat. folyamat és az LPM halálozás nagysága[46] (2. ábra).
Az enyhe gyulladás után kialakult ii-moLPM-ek hosszú távon együtt léteztek a megmaradt rezidens LPM-ekkel, de a rezidens LPM-ekkel való versengés és a peritoneális környezetben bekövetkezett változások aberráns aktiválási állapotban tartották őket, és blokkolták a rezidens LPM-fenotípus megszerzését. Ezzel szemben a súlyos gyulladás a rezidens LPM-ek teljes ablációjához vezethet, amelyeket végső soron ii-moLPM-ek váltanak fel, amelyek ugyan rezidens LPM-azonosságot szereztek, de transzkripciósan és funkcionálisan eltérő jellemzőket tartottak fenn, amelyeket eredetük, peritoneális gyulladásuk és kialakulási idejük határoz meg. -rezidens.[46] Az ii-moLPM-ek fenotípusa az eredetük alapján meghatározott belső markerekből áll, mint például a CD62L és a Semaphorin 4a, amelyek expresszióját a rezidens LPM-ekkel való versengés szabályozza, de idővel újraprogramozzák, mint például a GATA6, MHCII és CCR5, és a tartózkodás idejére vonatkozó markerek, függetlenek a rezidens LPM-ekkel, például a Tim4, CD209b és VSIG4 versenytársától. Úgy tűnik, hogy a rezidens LPM-ek és ii-moLPM-ek által eltérően expresszált gének jelentős részét a retinsav jelátvitelének különbségei szabályozzák, akár közvetlenül, akár GATA{18}}függő módon.[46]
Az ii-moLPM-ek nagyobb proliferációs aktivitást mutatnak, mint a rezidens LPM-ek [38,46], amiről azt feltételezték, hogy az előbbiek megnövekedett proliferációs képességében mutatkozó különbségek a mezoteliális sejtek által termelt CSF1-re reagálva.[36] Ezenkívül az ii-moLPM-ek gyengébb képességet mutattak a baktériumok fagocitózására és a haldokló sejtek felvételére, és nem tudtak CXCL13-at termelni.[46] Míg a peritoneális B1-sejtek száma az életkorral növekszik a homeosztázisban, a peritoneális gyulladás a B1-sejtek hibás felhalmozódásához vezetett[46], mivel, amint fentebb rámutattunk, az LPM-ek CXCL13-termelése szabályozza a peritoneális üregbe tartó B1-sejteket.[48] Ezért az a tény, hogy az LPM-populáció fejlődési és funkcionális heterogenitása a nemtől és az életkortól függ, fontos következményekkel jár az LPM-eknek a helyreállításban, a védekezésben és a peritoneális tumor metasztázisában betöltött szerepének vizsgálatakor, amelyeket figyelembe kell venni a jövőbeni vizsgálatok során.
Fontos megjegyezni, hogy a nem fertőző peritoneális károsodással, fertőzéssel vagy metasztatikus daganatnövekedéssel kapcsolatos gyulladásos reakciók során a peritoneális üregbe toborzott monociták potenciálisan monocita eredetű sejtekké differenciálódhatnak, amelyek specifikus javító, védekező vagy tumor-elősegítő funkciókat látnak el. de előfordulhat, hogy nem szereznek fenotípusos vagy funkcionális LPM-jellemzőket, ezért nem tekinthetők ii-moLPM-nek. A gyulladt hashártyába toborzott monocitáktól megkülönböztetett sejtek azonosságának meghatározása azonban ellentmondásos lehet, mivel a legtöbb jelentés a peritoneális monocita eredetű sejtek funkcionális relevanciájára, a perzisztencia idejére és/vagy az LPM-jellemzők megszerzésére összpontosít. A monocita eredetű sejtekkel nem foglalkoztak, és fordítva, a gyulladás alatti rezidens LPM-pótlásról szóló jelentésekben az ii-moLPM-ek funkcióját nem vizsgálták mélyrehatóan.
Összhangban azzal a hipotézissel, hogy a sejtes és molekuláris mikrokörnyezeti tényezők által meghatározott fizikai résért folyó versengés határozza meg a monociták hozzájárulását a szövetekben rezidens makrofágokhoz[43], a peritoneális rezidens makrofágok számára biokémiai rés létezését javasolták.[46] ] Ennek megfelelően az LPM-ek túlélését, proliferációját és működését szabályozó jelekért és sejt-sejt kölcsönhatásokért folyó versengés szabályozza a rezidens LPM-ek és az ii-moLPM-ek közötti egyensúlyt, valamint az érett rezidens LPM-identitás iimoLPM-ek általi megszerzését.
5. A nagy peritoneális makrofágok szerepe a peritoneális homeosztázisban
Az LPM-ek alapvető szerepet töltenek be az apoptotikus sejtek kiürülésében egyensúlyi állapotban, ami a szövetben rezidens makrofágok jellemzője, amely kulcsfontosságú az öntolerancia fenntartásához[49] specifikus scavenger receptorok, köztük CD36, CD93, CD163 Tim4 expressziója révén. , és MerTK.[16,20–22] Érdekes módon az apoptotikus sejtek LPM-ek általi hatékony internalizálását az apoptotikus sejtek által kitett foszfatidil-szerin Tim4-hez való kezdeti kötődésén, majd MerTK-közvetített bekebelezésén alapulva javasolták.[20] Az LPM-eket a hashártya mikrokörnyezete úgy programozza, hogy hatékonyan eltávolítsák az apoptotikus sejteket, elkerülve a TLR által közvetített, saját eredetű nukleinsav felismerés által közvetített gyulladást, miközben fenntartják a fertőzésre való reagáló képességet.[25]
A Kruppel-szerű 2-es és 4-es transzkripciós faktorokról azt állították, hogy az LPM-programozást az apoptotikus sejtek immunológiailag csendes eltávolítására irányítják az apoptotikus sejtfelismerő receptor gének, például a Timd4, a Marco és az Olr1, valamint a negatív szabályozóként működő gének expressziójának szabályozásával. a TLR jelzések, mint például a Hes1, Socs3, Pdlim2, Ptpn6 és Tnfaip3, ami megnövekedett aktiválási küszöböt eredményez.[25] Ezekkel a megfigyelésekkel összhangban az LPM-ek a VSIG4-et, a B7 családhoz kapcsolódó receptort expresszálják, amely a jelentések szerint csökkenti a makrofágok aktivációját a mitokondriális piruvát oxidáció és a ROS termelés PDK{14}}közvetített újraprogramozása révén.[23]
Az LPM-ek kulcsszerepet játszanak a peritoneális B1-sejtek homeosztázisának fenntartásában. Valójában a peritoneális B1-sejtek, amelyek konstitutívan termelnek természetes IgM-et, és biztosítják a lokális első védelmi vonalat számos kórokozóval szemben[12], az LPM-ek és a stromasejtek által termelt CXCL13 kemokintől függenek a keringésből való toborzásuk és a bejuttatásuk során. a peritoneális üregbe; A CXCL13 szükséges a B1-sejteknek az omentumba való bejutásához is.[48] Ezenkívül a peritoneális B1-sejtek az intestinalis lamina propriába történő egyensúlyi migráció után természetes IgA antitesteket választanak ki, hogy biztosítsák a bélmikrobióta immunkontrollját.[12] Érdekes módon a peritoneális B1 sejtekben az IgA osztályváltást, és ennek következtében a B1 sejt által közvetített bél IgA szekréciót az LPM-ek retinsav/GATA{13}}függő TGF-𝛽 termelése szabályozza.[19] Ezzel a megfigyeléssel összhangban a retinsav és a TGF- in vitro szinergista hatást fejt ki az IgA osztályváltásra a peritoneális B1 sejtekben.[50]
Az LPM-ek további, a peritoneális homeosztázishoz kapcsolódó funkciója a steril hashártya-sérülések megfigyelése, amelyek, hacsak nem gyorsan javítják ki, peritoneális összenövések kialakulásához vezethetnek, amelyek súlyos peritoneális betegséggé alakulhatnak, beleértve a bélelzáródást és a nők meddőségét. 10] A peritoneális károsodás vagy fertőzés kimutatására irányuló felügyeletet alapvetően LPM-ek látják el, és aktív járőrözést igényel a peritoneális felszínen. Ezzel kapcsolatban egy friss jelentésben, amelyben a hasüreg ép hasfalán keresztül történő leképezését intravitális mikroszkóppal végezték, kimutatták, hogy az LPM-ek passzívan, légzésfüggően és véletlenszerűen mozognak egyensúlyi állapotban, sebességgel. 800 μm s-1-ig. [4] Az LPM-ek szerepét a peritoneális szövetek helyreállításában és adhézió kialakulásában a következő fejezet tárgyalja.
6. A nagy peritoneális makrofágok szerepe a peritoneális sérülések helyreállításában
A hasi vagy zsigeri peritoneum károsodását okozhatja véletlen trauma vagy hasi műtét által okozott steril sérülés, vagy peritoneális patológiák, például fertőzés, máj- vagy bélbetegségek, vagy áttétes daganatnövekedés. Az alábbiakban tárgyalt legújabb tanulmányok fényt derítettek a peritoneális steril sérülések helyreállításában szerepet játszó mechanizmusokra és az LPM-ek szerepére ebben a folyamatban.[10] Ezzel szemben, hogy a peritoneális fertőzés vagy a tumor áttét által károsított hashártya később hogyan áll helyre, még mélyrehatóan feltárandó.
A peritoneális nyálkahártya károsodásának érzékelése a veszélyhez kapcsolódó molekuláris mintázatok (DAMP) felismerésével érhető el, amelyeket a sérült sejtek, köztük a mezoteliális sejtek, a szubmesotheliális kötőszövetben található sejtek és potenciálisan az alatta lévő szöveteket alkotó sejtek bocsátanak ki. A DAMP-ok közé tartoznak a konstitutívan expresszált DAMP-ok, mint például a nukleáris és mitokondriális DNS, nukleáris és mitokondriális fehérjék (HMGB1, hisztonok, citokróm c), ATP, K plusz ionok vagy S100 kalciumkötő fehérjék, indukálható DAMP-ok, például hősokkfehérjék, defenzinek , galektinek és IL{5}}𝛼, valamint extracelluláris DAMP-ok, például hialuronán vagy heparán-szulfát.[51] A DAMP-aktivált mezoteliális sejtek peritoneális gyulladást váltanak ki proinflammatorikus citokinek és kemokinek felszabadulásával, amelyek elősegítik a leukocita toborzást a sérült területeken és komplement aktivációt, ami további gyulladást eredményez. Ez a gyulladásos reakció szöveti faktor-függő fibrinpolimerizációt vált ki a fibrinogenezis és a fibrinolízis közötti egyensúlyhiány eredményeként, ami fibrinmátrix kialakulásához vezet, amely a sebgyógyulás vázaként szolgál.
Ez utóbbi magában foglalja a javító funkciót ellátó leukociták, köztük az LPM-ek, neutrofilek, monociták és monocita eredetű makrofágok toborzását a szubmezoteliális kompartmentbe, a mezenchimális prekurzorok toborzását, az extracelluláris mátrix lerakódását, az idegek és a vérerek benőttségét, valamint a re-pithelializációt. a sérült peritoneumról.[10] A peritoneális gyulladás fennmaradása túlzott fibrinlerakódáshoz vezethet, és végső soron rostos hidak képződéséhez az egymással szemben lévő peritoneális felületek között, amelyek idegeket és ereket tartalmaznak, ezeket hasi összenövéseknek nevezzük.[52] Az összenövéseket túlnyomórészt hasi műtétek okozzák, de fertőzés, endometriózis, sugárterápia vagy peritoneális dialízis is okozhatja, és jelentős morbiditással jár, ami életveszélyes szövődményekkel járhat.[52]
A kísérleti sebészeti sérülés utáni peritoneális gyógyulás elektronmikroszkópos elemzése, amely kimutatta, hogy a makrofágok a sérülés után 24 órával a sérült szövethez tapadtak, majd a sebbe vándoroltak,[53] szolgáltatta az első bizonyítékot a makrofágok peritoneálisban betöltött lehetséges szerepére. sérülés javítása. Ezt a hipotézist a Dr. P. Kubes laboratóriumának intravitális mikroszkópos vizsgálatai is alátámasztották, amelyek kimutatták, hogy a májkapszula lézerrel kiváltott sérülése után az F4/80high GATA6 plusz LPM-eket a sérült területekre toborozták, és a mesotheliumon keresztül a májba vándoroltak. májsérülések, a lézerrel kiváltott sérülést követő 1 órán belül.[30]
Az LPM-ek a máj nekrotikus sejtek által a DAMP PX27 receptoron keresztül felszabaduló ATP felismerése révén érzékelték a sérült szövetet, és beszivárogtak a máj parenchymába a CD44- révén, közvetítve a sérült területeken jelen lévő hialuronánhoz való kötődést. Érdekes módon a sérült szövethez való toborzás kiváltotta az LPM-proliferációt és az alternatív aktivált/javító fenotípushoz kapcsolódó molekulák, mint például a CD206, CD273 és az argináz 1, felszabályozását. Ennek megfelelően a toborzott LPM-ek aktívan hozzájárultak a nekrotikus sejtek eltávolításához, amiről azt állították, hogy kritikus. revaszkularizációhoz és szövetek helyreállításához, amint azt azok a kísérletek is alátámasztják, amelyek azt mutatják, hogy a sérült területek gyógyulása késleltetett klodronáttal töltött liposzóma-mediált LPM-kimerült vagy GATA{8}}hiányos egerekben.[30]
Hasonló ATP-indukált toborzást és CD{1}}függő migrációt az F4/80 magas GATA6 plusz LPM-ek sérült területére írtak le egy bélhőkárosodás modelljében.[54] A klodronáttal töltött liposzómák által közvetített LPM-kiürítési kísérletek is alátámasztották azt az elképzelést, hogy az LPM-ek hozzájárultak a sérült bélrendszer helyreállításához ebben a kísérleti környezetben. Mindazonáltal, hogy a jelen jelentésben leírtak szerint az LPM-ek a bélhám károsodása után bekerülnek-e a bélszérumba, további vizsgálatot igényelne, mivel továbbra is lehetséges, hogy ez a jelenség műtermék volt, ha ezekben a kísérletekben a károsodás nem korlátozódott a bélhám károsodására. a bél luminális felszínén, de érintette a bélnyálkahártyát és a nyálkahártya alatti részeket, figyelembe véve a jelen vizsgálatban e probléma kezelésére alkalmazott kísérleti stratégiát.
Másrészt a klodronáttal kezelt liposzómákkal végzett kezelés LPM-kimerülésének kísérleteit illetően, amelyeket az LPM-eknek a máj vagy a bélrendszeri szerózus helyreállításában játszott szerepének vizsgálatára végeztek, [30,54], hogy a klodronáttal kezelt egereknél megfigyelhető-e a késleltetett sebgyógyulás. nem zárható ki, legalábbis részben a peritoneális monocita eredetű makrofágok és a szövetekben rezidens makrofág populációk kimerülése miatt, amelyek jelen vannak az omentumban, a peritoneális membránban vagy a máj tokjában. Valójában kimutatták, hogy a monociták a peritoneális sérült területekre toboroznak, ahol monocita eredetű makrofágokká differenciálódnak, amelyek elősegíthetik a szövetek helyreállítását.[55]
Ezekkel a megfigyelésekkel összhangban azt az elképzelést, hogy miután az LPM-ek a sérült mesotheliumhoz tapadnak, szerosális sérülésekbe vándorolnak, és kritikus helyreállító funkciót töltenek be, megkérdőjelezték egy nemrégiben megjelent jelentésben, amelyben a genetikai sorstérkép lehetővé tette a rezidens LPM-ek nyomon követését a máj steril sérülése után. [56] Ezek a vizsgálatok kimutatták, hogy a GATA6 plusz rezidens LPM-ek felhalmozódtak a máj sérült felületén, de minimálisan behatoltak a nekrotikus májparenchymába. Továbbá a diftéria toxin függő G6Mø-CreER használatával; R26-tdTomato/iDTR egérvonal, amely lehetővé tette a legtöbb GATA6 plusz rezidens LPM genetikai ablációját, a szerzők arra a következtetésre jutottak, hogy a GATA6 plusz rezidens LPM-ek hiánya nem befolyásolta jelentősen a májsebek gyógyulását, és így a GATA6 plusz rezidens Az LPM-ek nem voltak kritikusak a sérült szerózus szövetek regenerációjában. Ezért további kutatásokat kell végezni annak megállapítására, hogy az LPM-ek hozzájárulnak-e a peritoneális gyógyuláshoz, és végül hogyan.
Érdekes módon Dr. P. Kubes laboratóriumának egy közelmúltbeli jelentése, amely a peritoneális üreg lézer-indukált fokális termikus peritoneális sérülése utáni, az ép hasfalon keresztül történő intravitális mikroszkópos képalkotásán alapul, alátámasztja az LPM-ek közvetlen szerepét a szerózus helyreállításban. [4] Valójában a rezidens GATA6 plusz LPM-ek voltak az első olyan sejtek, amelyeket a mesotheliális sérülések miatt toboroztak, amely folyamat peritoneális folyadék nyíróáramlást igényelt. Az LPM-ek a sérült hashártyához tapadtak, és 15 perccel a sérülés után teljesen lefedték az elváltozásokat, trombusszerű struktúrákat képezve egy olyan folyamatban, amely tükrözte a véredény sérülésére adott válaszként a vérlemezke-aggregációt. Az LPM aggregációja nem a kanonikus adhéziós molekuláktól vagy a fibrin polimerizációtól függött, hanem a scavenger receptor ciszteinben gazdag (SRCR) domént tartalmazó scavenger receptoroktól, mint például a MARCO vagy az MSR1, amelyek nagyszámú polianionos ligandumhoz kötődnek, és amelyek az evolúció során erősen konzerváltak. gerinctelenektől. Valójában tüskésbőrűeknél, például tengeri sünnél a cölomikus üreg sérülése az SRCR-t tartalmazó homológokat expresszáló cölomociták aggregációjához vezetett, amelyek lezárták a sérült területeket. peritoneális léziók a peritoneális sérülések fizikai lezárásával, mivel a makrofágok aggregációjának blokkolása a sérült parietális peritoneum késleltetett gyógyulásához vezetett.[4]
Ezzel szemben a műtéti steril sérülés által kiváltott peritoneális adhézió kialakulásának kísérleti modelljét használva, amely magában foglalja a peritoneális gomb kialakulását a peritoneális fal egy részének varrásával, nagyszámú LPM-et vontak be a gombokba a műtét után 3 órán belül. [4] Ebben az iatrogén környezetben a makrofágok kiterjedt aggregátumokat képeztek, amelyek elősegítették a fibrin lerakódását és a hegszövet növekedését, ami a műtét után 7 napon belül peritoneális összenövések kialakulásához vezetett.

Érdekes módon a peritoneális adhéziók száma és kialakulása jelentősen csökkent azokban az egerekben, amelyekben az LPM-ek a műtét előtt 24 órával kimerültek, ami alátámasztja, hogy az LPM-ek hozzájárultak a peritoneális adhézió kialakulásához. Érdekes módon a kísérleti adhéziós képződés hasonló modelljét használva kimutatták, hogy az LPM-ek sejtgátat képeznek a sérült mezoteliális területeken képződött fibrinrögök felett, ami adhézió kialakulásához vezet, ha a makrofág gát nem volt elegendő a fibrinrög lefedéséhez, de kizárta az adhézió kialakulását, ha a makrofág gát teljesen leárnyékolta a fibrinrögöket.[59] Valójában a makrofág gát IL-4-közvetítette megerősítése megakadályozta az adhézió kialakulását, és alapja lehet a posztoperatív összenövések megelőzésére szolgáló innovatív kezelések kifejlesztésének. Ezért, bár úgy tűnik, hogy a kezdeti makrofágok toborzása és aggregációja, valamint a fibrinlerakódás szükséges a megfelelő szerózus helyreállításhoz, ez patogén hegesedést is okozhat, ami adhézió kialakulásához vezet, ami összefüggésben áll az alacsony mesothel fibrinolitikus aktivitással.[52] ]
Összefoglalva, az LPM-ek szerepét a steril peritoneális károsodások helyreállításában nagymértékben a sérülés súlyossága határozza meg. Az LPM-ek elősegítik az adhézió kialakulását nagy peritoneális sérülés után, de alapvető funkciót töltenek be a fokális mesotheliális sérülések gyors helyreállításában, emlékeztetve az evolúció során megőrzött primitív javítási mechanizmusokra (3. ábra). Másrészt az LPM-ek azon képessége, hogy mélyen károsodott szubmesotheliális szövetet behatoljanak, és hozzájáruljanak annak helyreállításához a monocita eredetű makrofágokkal és neutrofilekkel együtt, még mindig ellentmondásos, ezért további vizsgálatra van szükség. Ebben a tekintetben, amint azt más makrofág populációknál leírtuk, az LPM-ek termelnek-e mélyreható gyógyító mediátorokat, mint például a vérlemezkékből származó növekedési faktor, az inzulinszerű növekedési faktor 1, a TGF-𝛽1 vagy a VEGF-𝛼 [60], még feltárásra vár. .
For more information:1950477648nn@gmail.com
